免疫疗法领域的试验更新和新生物标志物
派姆单抗(pembrolizumab)的 长期发现:KEYNOTE-001
KEYNOTE-001是证明PD-1抑制剂派姆单抗在初治或先前治疗的晚期NSCLC患者中的活性的首项试验[1]。值得注意的是,在此项多队列IB期研究中,派姆单抗随着PD-L1肿瘤比例评分(TPS)的增加而显示更高的活性。在2012年5月至2014年7月间,共有550名晚期NSCLC患者参与了4个非随机队列和2个随机队列。其中101人是初治的,449人接受过治疗。Garon等人在2019年ASCO大会上报告了KEYNOTE-001的5年疗效和安全性结果[2]。在数据截止时,100名患者存活。最新的分析代表了在晚期NSCLC条件下迄今为止对派姆单抗治疗最长的随访。
在初治NSCLC患者中,23.2 %在5年时存活;在预先治疗的队列中,15.5 %在5年时存活。作者指出,与之相比,于2008年至2014年间在美国使用标准治疗细胞毒性化疗获得的5年OS率为5.5 %[3]。在PD-L1 TPS≥ 50 %的患者中,初治和预先治疗条件下的5年OS率分别为29.6 %和25.0 %。TPS为1 %至49 %的患者5年生存率较低(分别为15.7 %和12.6 %)。在所有组中,初治和预先治疗患者的ORR分别为41.6 %和22.9 %,DCR分别为83.2 %和58.6 %。60名接受派姆单抗治疗≥2年的患者中有46名在数据截止时存活。对于初治和预先治疗队列(分别为n = 14和n = 46),这60名患者的估计5年OS率分别为78.6 %和75.8 %。客观缓解的发生率分别为86 %和91 %,中位缓解持续时间分别为52.0个月和未达到。
更新的安全性数据与派姆单抗的已知特征一致。没有证据显示累积的免疫介导毒性或迟发的3至5级毒性。总体而言,这些数据继续证明了派姆单抗治疗对于初治和经预先治疗的晚期NSCLC患者而言在改善长期结果方面的潜力。
KEYNOTE-189:更新结果与PFS2
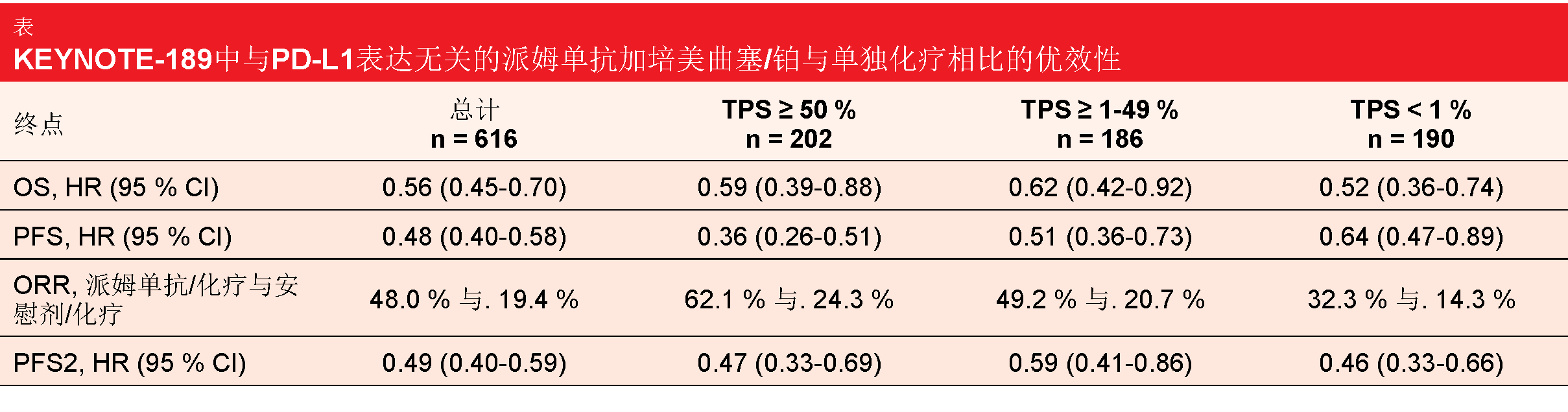
随机化双盲III期KEYNOTE-189试验在转移性非鳞状NSCLC中证明了一线派姆单抗与培美曲塞/铂双药的组合相比于安慰剂加培美曲塞/铂的优效性[4]。获得了有关OS、PFS和ORR的获益;与此同时,安全性特征证明是可控的。Gadgeel等人基于更长时间的随访介绍了更新的疗效结果,并首次介绍了PFS2,PFS2定义为从随机化到在下一治疗线条件下发生客观肿瘤进展或者任何原因导致死亡的时间,以先发生者为准[5]。PFS2可用于量化交叉对OS评估的影响,并确定一条治疗线是否对下一治疗线的活性产生正面或负面影响。
在ITT人群中,410名患者接受了基于派姆单抗的组合,而206名患者使用安慰剂加化疗治疗。分别向44.6 %和59.2 %的患者给予至少一种后续治疗。13 %与54 %的患者接受≥ 1种后续PD-1或PD-L1抑制剂。在对照组接受治疗的患者中有40.8 %进行了研究内交叉。
派姆单抗加培美曲塞和铂继续引发显著的生存获益(中位OS,22.0与10.7个月;HR,0.56)。两组的24个月OS率为45.5 %与29.9 %。同样,PFS大致翻倍(9.0与4.9个月;HR,0.48),24个月PFS率为20.5 %与1.5 %。此外,分析显示基于派姆单抗的方案在PFS2方面有显著获益(17.0与9.0个月;HR,0.49)。实验组中的ORR也较高(48.0 %与19.4 %)。尽管较高比率的患者接受后续治疗并进行研究内交叉,所有这些终点中都观察到添加派姆单抗的获益,并且与PD-L1表达无关(表)。在延长的随访后,基于派姆单抗的方案的安全性和耐受性仍然可控。根据作者的结论,这些数据证实,派姆单抗应作为一线治疗的一部分给予,以最大限度地改善表达PD-L1和不表达PD-L1的转移性非鳞状NSCLC患者的结果。
绝对PD-L1水平的重要性
仍然缺少用于选择最佳患者从而进行免疫检查点抑制剂治疗的预测性生物标志物,而PD-L1表达仍然作为主要的临床适用测试。作为多中心回顾性研究的一部分,Aguilar等人分析了具有IV期NSCLC且PD-L1 TPS ≥ 50 %的患者,以回答这一范围内的某些亚组是否更有可能获益于PD-1抑制剂治疗的问题[6]。整个队列包括172名接受一线派姆单抗的患者。在PD-L1 TPS为50 %至74 %(n = 68)与75 %至100 %(n = 104)的患者以及50 %至89 %(n = 99)与90 %至100 %(n = 73)的患者中,将临床病理特征和临床结果进行比较。
事实上,研究发现表明,较高的≥ 75 %和≥ 90 %的PD-L1 TPS水平与改善的临床结果相关。在针对从未吸烟者、鳞状组织学和突变状态进行调整后,这些患者显示比具有较低PD-L1表达水平的对应者得到更大的生存获益(HR分别为0.63和0.50)。比较还显示PD-L1 75 %至100 %与50 %至74 %相比(HR,0.61)和90 %至100 %与50 %至89 %相比(HR,0.52)均产生显著的PFS延长。类似地,ORR有利于具有较高PD-L1表达的人群。缓解者的PD-L1 TPS高于非缓解者。达到部分或完全缓解患者的平均TPS为82.1 %;在那些显示疾病稳定和疾病进展的患者中,这一比例为73.7 %(p = 0.001)。研究人员指出,当在一线派姆单抗单药治疗与派姆单抗加铂双药化疗之间进行决定时,应考虑这些结果。此外,在设计和解读针对PD-L1 TPS≥50 %的NSCLC的临床试验中,这些结果值得关注。
其他标志物:STK11和KEAP1
已经发现STK11/LKB1基因组改变是“冷”肿瘤免疫微环境的中介物,并且是非鳞状NSCLC中PD-1抑制的原发性耐药的主要驱动因子[7]。STK11是该疾病中最常见的失活肿瘤抑制基因之一。其编码在细胞生长和代谢的调节中起作用的蛋白质LBK1。此外,KEAP1基因在遗传上和功能上与STK11连锁,这两个基因往往共同突变[8,9]。
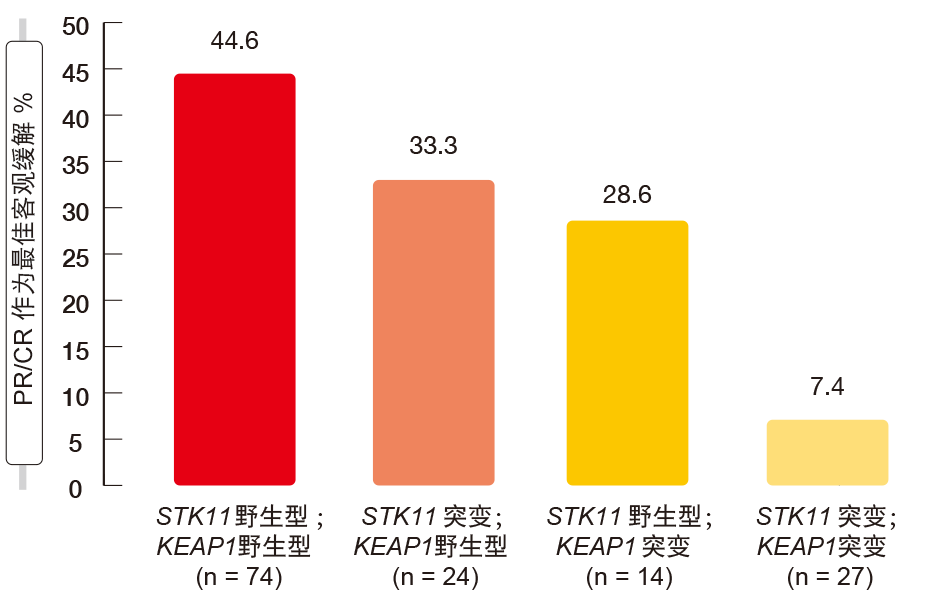
由Skoulidis等人进行的回顾性国际化研究解决了这些标志物作为派姆单抗加培美曲塞和铂在转移性非鳞状NSCLC的一线条件下获得的临床结果的分子决定因素的影响[10]。STK11和KEAP1基因组改变显示与化学免疫疗法的不良结果显著相关。这适用于每种改变,但特别适用于共同突变的情况。双野生型人群的中位PFS为8.4个月,而双突变群体的中位PFS仅为2.7个月(p < 0.0001);对于中位OS,中位PFS为20.4与6.6个月(p = 0.005)。同样,当随着突变的数量增加进行观察时,ORR显示逐渐恶化(图1)。在患有原发性难治性疾病的患者组中,多达76.5 %的患者具有STK11和/或KEAP1畸变。此外,这些突变的存在与在培美曲塞加铂之外添加派姆单抗缺乏明显的PFS或OS获益相关。STK11和KEAP1畸变对使用化学免疫疗法所带来临床结果的负面影响在高肿瘤突变负荷和PD-L1阳性肿瘤的患者中最为突出。同时,在具有STK11突变和/或KEAP1突变肿瘤的患者中,肿瘤突变负荷和PD-L1表达不影响结果。
基于这些发现,作者提出将STK11和KEAP1突变整合到复合基因组标志物中,预测化学免疫疗法的不良临床结果。这将捕获由大约25 %的NSCLC患者构成的亚组,他们亟待新型策略用于建立有效的抗肿瘤免疫力。
图1:在STK11和KEAP1定义的亚组中用派姆单抗加化疗获得的客观缓解率
NLR、PLR和 LDH
Russo等人证明,中性粒细胞与淋巴细胞比(NLR)、血小板与淋巴细胞比(PLR)和乳酸脱氢酶(LDH)等容易确定的参数可能有助于免疫疗法的患者选择[11]。研究人员评估了这些炎症标志物随时间的动态变化以及用纳武单抗或派姆单抗治疗的71名连续性NSCLC患者的结果。NLR ≥ 5,PLR≥ 200,LDH水平≥正常上限(UNL)被认为偏高。
事实上,NLR ≥ 5与较低的PFS和OS相关,从基线到第12周的预测值增加。基线和第12周时PLR ≥ 200与较短的OS显著相关,但与PFS无关。对于基线时LDH水平≥ UNL,分析显示与较短的PFS和OS相关;第12周时LDH水平与基线值相比降低预示着OS改善。研究人员总结认为,NLR、PLR和LDH的基线水平以及第12周时LDH水平的动态变化对接受单药免疫检查点抑制剂治疗的患者的结果具有显著的预测作用
自身免疫病是否妨碍治疗?
具有自身免疫病史的患者通常被排除在测试免疫治疗方法的临床试验之外。然而,轶事和早期证据表明,即使在这些患者中,免疫检查点抑制剂也被用于晚期NSCLC的常规治疗[12]。基于这些观察,进行了回顾性观察性队列研究,以描述在美国的49项主要基于社区的肿瘤学实践中,具有和不具有先前自身免疫病史的、已接受过至少一剂经批准免疫检查点抑制剂的晚期NSCLC患者的现实特征和结果,包括AE[13]。在免疫疗法起始前一年内接受过包括III期疾病的手术和放化疗在内的局部治疗是一项排除标准。分析中包括2,402名患者的记录。其中22 %(n = 531)有自身免疫病史。与没有自身免疫病史的队列相比,除了女性比例较高之外,两者表现出相似的患者和疾病特征(54.6 %与43.5 %)。
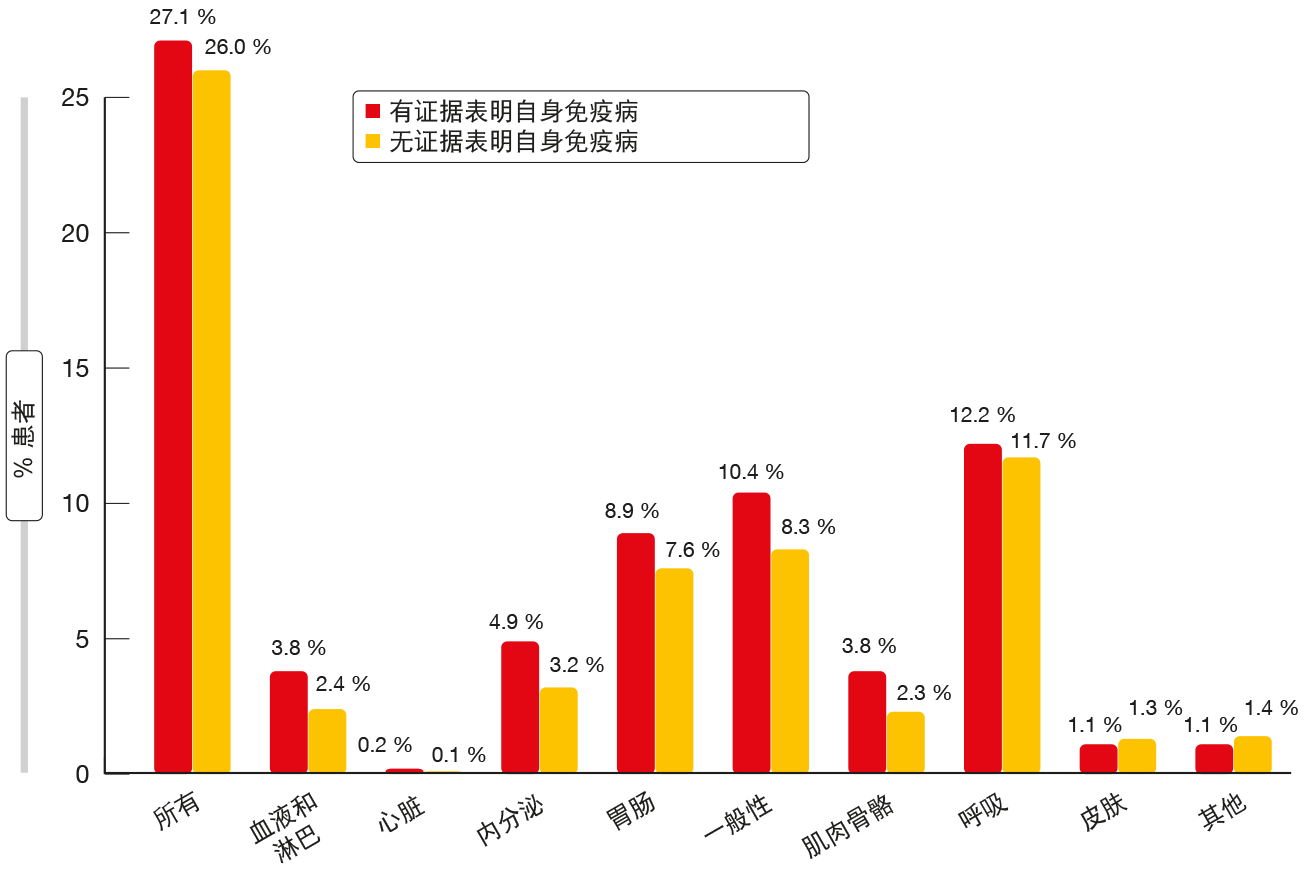
研究人员指出,与没有自身免疫病史的患者相比,有自身免疫病史的患者具有相似的疗效。对于OS、现实PFS、至治疗中止的时间和至下一次治疗的时间,Kaplan-Meier曲线是可叠加的,并且统计数据未产生任何显著差异。就耐受性而言,具有自身免疫病史的患者表现出免疫相关AE的发生率增加。对于内分泌、胃肠、血液和淋巴疾病以及一般性疾病尤其如此(图2)。需要进一步研究以深入了解自身免疫病对免疫相关AE的发生率和患者结果的影响。
图2:有无自身免疫病史的免疫检查点抑制剂治疗的患者中免疫相关AE的发生率
参考文献
- Garon EB et al., Pembrolizumab for the treatment of non-small-cell lung cancer. N Engl J Med 2015; 372(21): 2018-2028
- Garon EB et al., 5-year long-term overall survival for patients with advanced NSCLC treated with pembrolizumab: results from KEYNOTE-001. J Clin Oncol 37, 2019 (suppl; abstr LBA9015)
- Leighl NB et al., Pembrolizumab in patients with advanced non-small-cell lung cancer (KEYNOTE-001): 3-year results from an open-label, phase 1 study. Lancet Respir Med 2019; 7(4): 347-357
- Gandhi L et al., Pembrolizumab plus chemotherapy in metastatic non-small-cell lung cancer. N Engl J Med 2018; 378(22): 2078-2092
- Gadgeel S et al., KEYNOTE-189: updated overall survival and progression after the next line of therapy with pembrolizumab plus chemotherapy with pemetrexed and platinum vs placebo plus chemotherapy for metastatic nonsquamous non-small-cell lung cancer. J Clin Oncol 37, 2019 (suppl; abstr 9013)
- Aguilar EJ et al., Comparison of outcomes with PD-L1 tumor proportion score (TPS) of 50-74% vs 75-100% in patients with non-small cell lung cancer (NSCLC) treated with first-line PD-1 inhibitors. J Clin Oncol 36, 2018 (suppl; abstr 9037)
- Skoulidis F et al., STK11/LKB1 mutations and PD-1 inhibitor resistance in KRAS-mutant lung adenocarcinoma. Cancer Discov 2018; 8(7): 822-835
- Skoulidis F et al., Co-occurring genomic alterations define major subsets of KRAS-mutant lung adenocarcinoma with distinct biology, immune profiles, and therapeutic vulnerabilities. Cancer Discov 2015; 5(8): 860-877
- Galan-Cobo A et al., LKB1 and KEAP1/NRF2 pathways cooperatively promote metabolic reprogramming with enhanced glutamine dependence in KRAS-mutant lung adenocarcinoma. Cancer Res 2019 Apr 30. pii: canres.3527.2018. doi: 10.1158/0008-5472.CAN-18-3527. [Epub ahead of print]
- Skoulidis F et al., Association of STK11/LKB1 genomic alterations with lack of benefit from the addition of pembrolizumab to platinum doublet chemotherapy in non-squamous non-small cell lung cancer. J Clin Oncol 37, 2019 (suppl; abstr 102)
- Russo A et al., Dynamic changes of neutrophil-to-lymphocyte ratio (NLR), platelet-to-lymphocyte ratio (PLR), and lactate dehydrogenase (LDH) during treatment with immune checkpoint inhibitors (ICIs) in non-small cell lung cancer (NSCLC). J Clin Oncol 37, 2019 (suppl; abstr 2596)
- Darvin P et al., Immune checkpoint inhibitors: recent progress and potential biomarkers. Exp Mol Med 2018; 50(12): 165
- Khozin S et al., Real-world outcomes of patients with advanced non-small cell lung cancer (aNSCLC) and autoimmune disease receiving immune checkpoint inhibitors. J Clin Oncol 37, 2019 (suppl; abstr 110)
More posts
小细胞肿瘤:二线条件下的改善
小细胞肿瘤:二线条件下的改善 Lurbinectedin单药疗法 对于复发性小细胞肺癌(SCLC)患者,仅可获得有限的治疗选择。拓扑替康(topotecan)是唯一经FDA
罕见突变:使治疗更进一步
罕见突变:使治疗更进一步 GEOMETRY mono-1:MET失调NSCLC中的capmatinib 据报道,3 %至4 %的NSCLC患者具有MET外显子14跳跃突变(
ALK阳性疾病基于血液的检测
ALK阳性疾病基于血液的检测 Rafał Dziadziuszko,MD,PhD,波兰格但斯克,格但斯克医学院肿瘤及放射学系 在现今的肺癌诊断和治疗环境中,我们可以对循环
免疫疗法领域的试验更新和新生物标志物
免疫疗法领域的试验更新和新生物标志物 派姆单抗(pembrolizumab)的 长期发现:KEYNOTE-001 KEYNOTE-001是证明PD-1抑制剂派姆单抗在初治或
EGFR突变肺癌的新一线选择和其他见解
EGFR突变肺癌的新一线选择和其他见解 RELAY:添加雷莫芦单抗(ramucirumab) 尽管EGFR TKI治疗通常对EGFR突变肺癌患者有效,但耐药性在治疗开始后8
早期NSCLC:有前景的(新)辅助方法
早期NSCLC:有前景的(新)辅助方法 NEOSTAR试验 可切除非小细胞肺癌(NSCLC)患者需要有效的治疗选择,因为超过半数的I期至III期疾病患者经历复发[1]。Ch