EGFR突变肺癌的新一线选择和其他见解
RELAY:添加雷莫芦单抗(ramucirumab)
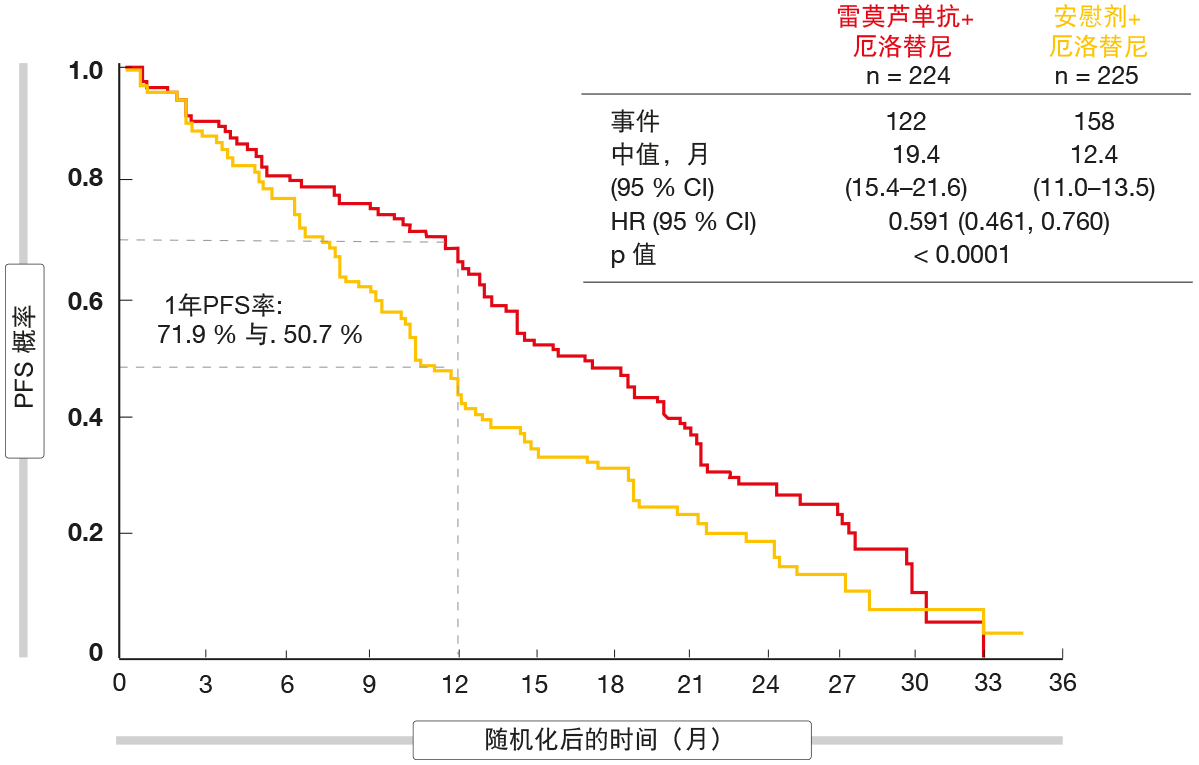
尽管EGFR TKI治疗通常对EGFR突变肺癌患者有效,但耐药性在治疗开始后8到12个月内不可避免地出现,导致治疗失败。因此,对延长EGFR靶向疗法活性的选项存在未满足的需求。VEGF和EGFR信号传导途径的双重阻断代表这方面的一种潜在方法。 全球性随机化安慰剂对照的III期RELAY试验在IV期EGFR突变阳性(即,外显子19缺失、外显子21 L858R突变)NSCLC患者中测试了第一代EGFR TKI厄洛替尼(erlotinib)与抗VEGFR-2抗体雷莫芦单抗的组合作为一线策略 [1]。具有脑转移的患者被排除在外。治疗包括150mg/d厄洛替尼加每2周10mg/kg雷莫芦单抗(n=224)或者150 mg/d厄洛替尼加安慰剂(n = 225)。治疗继续到直至发生进展或不可接受的毒性。研究人员评估的PFS构成主要终点。13个国家的数百个中心参与了研究。在两组中均有77 %的患者是亚洲人。 雷莫芦单抗的添加导致显著的7个月的PFS改善,这转化为统计上高度显著的41 %的风险降低(19.4与12.4个月;HR,0.591;p < 0.0001;图)。Kaplan Meier曲线从开始即分离。在1年时,71.9 %与50.7 %的患者无进展。独立盲中央审查显示一致的PFS获益(HR,0.671;p = 0.0022)。雷莫芦单抗加厄洛替尼在大多数亚组中产生了PFS获益。值得注意的是,具有外显子19缺失和外显子21 L858R突变的患者获得了类似的获益(HR分别为0.651和0.618)。
图:RELAY试验中在厄洛替尼之外添加雷莫芦单抗的7个月PFS改善
次要终点
两组的总体缓解率相当(76 %与75 %),疾病控制率也是如此(95 %与96 %)。然而,基于雷莫芦单抗方案的缓解持续时间显著更长(18.0与11.1个月;HR,0.619)。OS结果仍不成熟。对于PFS2,即从随机化到第二次疾病进展的时间,分析显示组合具有显著优势(HR,0.690;p = 0.03)。这意味着无进展以及OS获益。在基线和一个月后使用液体活检评估EGFR T790M耐药性突变的发生率。虽然两组中在基线处均未检测到T790M突变,但经历进展的患者在30天时的突变率相似,分别为43 %和47 %。 安全性结果与厄洛替尼和雷莫芦单抗已确定的概况一致。≥ 3级治疗出现的AE在组合组中的发生更为频繁(72 %与54 %)。然而,所有研究治疗中由于AE导致的中止率并无差异(13 %与11 %)。任何级别以及严重的高血压在实验组中更为普遍,但没有4级高血压病例。同样,雷莫芦单抗治疗的患者更常发生转氨酶升高,但大多数事件被评定为1级或2级。出血事件也是如此。总体而言,这些发现表明厄洛替尼加雷莫芦单抗是EGFR突变转移性NSCLC患者初治的新选择。
吉非替尼(Gefitinib)加化疗
延迟或预防对一线EGFR TKI治疗的获得性耐药的另一种策略是口服TKI与化疗的组合。在2019年ASCO大会上,Noronha等人介绍了随机化开放标签III期试验的结果,该试验在非进展性疾病患者中对第一代EGFR TKI吉非替尼与吉非替尼加培美曲塞/卡铂四个周期然后维持培美曲塞进行了比较[2]。具有IIIB或IV期EGFR突变NSCLC的患者接受组合(n = 174)或一线姑息意图的吉非替尼单药疗法(n = 176)直至进展。每组中超过20 %的患者具有ECOG PS 2。分别有17 %和19 %存在脑转移。纳入了具有罕见EGFR异常,诸如外显子18和外显子20突变,的患者。 在PFS和OS方面,组合方法与吉非替尼单药相比引起显著改善。被定义为主要终点的中位PFS翻倍(16与8个月;HR,0.51;p < 0.0001)。所有亚组均发生显著PFS获益。关于OS,死亡风险降低了55%(未达到与17个月;HR,0.45;p < 0.0001)。组合组中的患者还显示更明显的缓解(ORR,75.3 %与62.5 %;p = 0.01)和中位缓解深度(-56.4与-43.5;p = 0.002)。临床相关的≥ 3级毒性翻倍,从25.3 %增加到50.6 %(p <0.001)。其中大多数是血细胞减少症。除肾毒性和低钾血症外,其他类型的毒性在两组中没有显著增加。 这些结果将吉非替尼加培美曲塞/卡铂确定为EGFR突变NSCLC患者的额外一线选择。研究人员指出,这是在此条件下延长OS的少数几种方案之一。PFS获益类似于使用第三代EGFR TKI奥希替尼(osimertinib)进行的FLAURA试验所获得的PFS获益,但在本研究中纳入了PS 2的患者,而FLAURA仅招募PS ≤1的患者[3]。根据作者的结论,有效疗法的顺序对于最大限度地提高生存率是重要的。由于奥希替尼在T790M突变阳性肿瘤中具有活性,因此其可能更适合于复发条件。
TAK-788对于外显子20插入有效
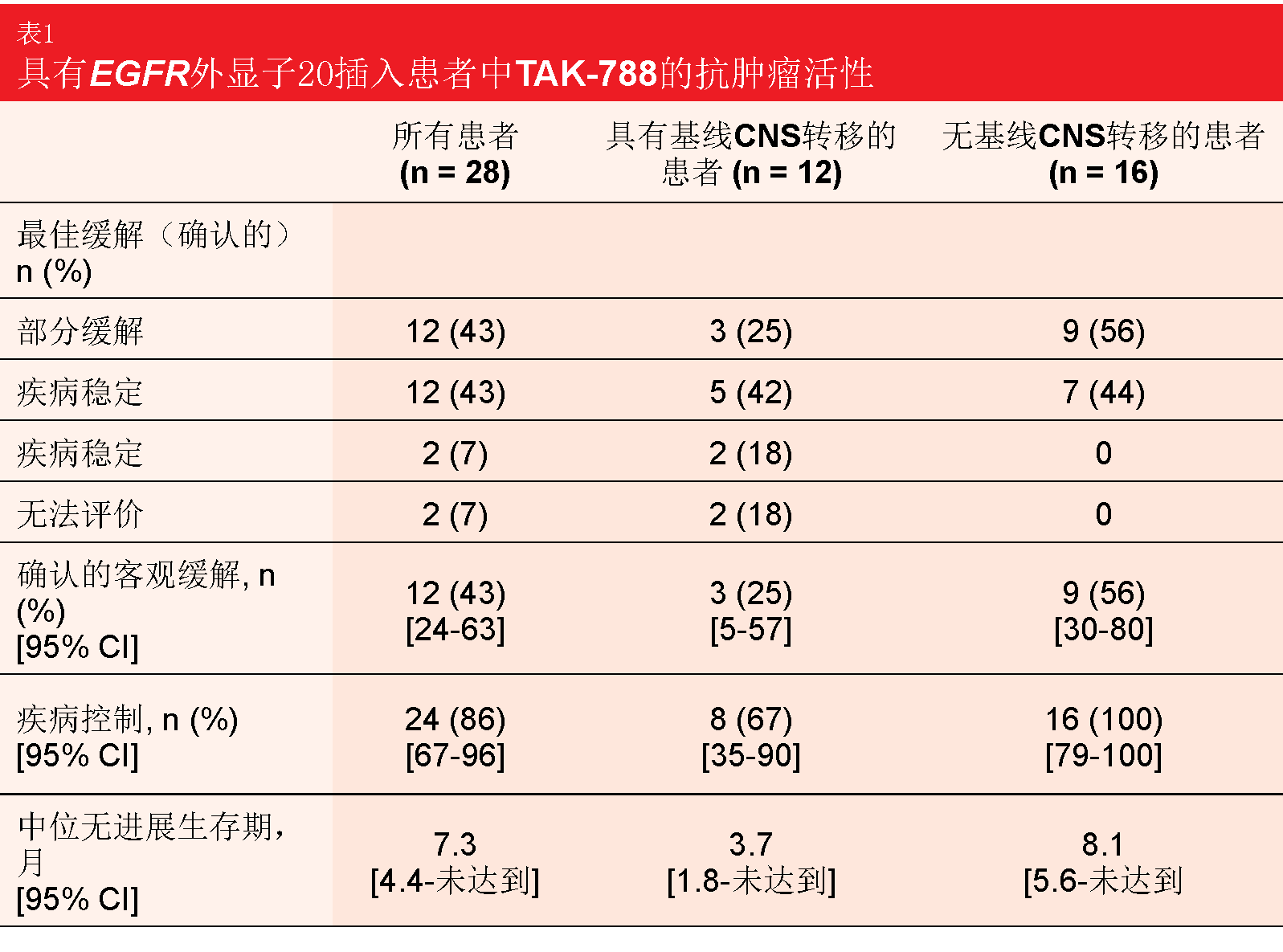
当前批准的EGFR TKI已显示在具有常见激活EGFR突变(包括外显子19缺失和外显子21 L858R突变)的肺部肿瘤中的功效,但在具有EGFR外显子20插入的患者中很大程度上无效。在大约6 %的病例中存在这些畸变,但缺乏针对具有这些异常的患者的靶向选择[4]。实验性EGFR TKI TAK-788显示有效抑制外显子20突变,对其的选择性高于野生型EGFR。正在II期试验中对TAK-788进行评价,该试验在患有NSCLC和其他肿瘤类型的7个患者队列中以160 mg/d进行测试。在2019年ASCO大会上,Jänne等人报告了具有难治性外显子20阳性肺癌以及活跃或可测量CNS转移(但不同时两者兼具)的队列1中的发现[5]。入选要求一种或多种先前的全身治疗方案;如果没有缓解,则允许先前的TKI治疗。疗效人群包括28名患者。治疗的中位时间为7.9个月,并且在分析时有50 %仍在研究当中。 160mg/d TAK-788表现出抗肿瘤活性,确认的ORR为43 %(表1)。基线CNS转移患者的缓解率为25 %,而没有基线CNS转移的患者的缓解率为56 %。在总人群中,DCR和PFS分别达到86 %和7.3个月。在具有包括769_ASV和773_NPH在内的各种外显子20插入变体的患者中均发生缓解。AE证明是可控的并与其他EGFR TKI的AE一致,腹泻、恶心和皮疹报告为最常见的毒性。大多数治疗相关AE为1级和2级并且是可逆的。在队列1至7(n = 72)的剂量递增或扩展期间,用至少一剂160 mg/d TAK-788治疗的患者组中治疗相关≥ 3级AE的发生率为40 %,并且剂量减少在25 %的情况下是必要的。在14 %的情况下,治疗由于毒性而中止。 全球性EXCLAIM扩展队列正在接受过1至2种先前化疗的91名携带EGFR外显子20插入的局部晚期或转移性NSCLC患者中进一步研究160mg/d TAK-788直至进展。在该群体中允许经治疗的CNS转移。根据独立审查委员会确认的ORR构成主要终点。
使用阿法替尼的现实经历
在88名中国患者中获得的观察性现实数据证实了使用第二代EGFR TKI 阿法替尼进行一线治疗的疗效和耐受性[6]。ORR和DCR分别为54.5 %和92.0 %,中位PFS为14.2个月。阿法替尼的活性不受存在脑转移、剂量或治疗线的影响。在阿法替尼治疗后发生进展的患者中,65.4 %携带T790M突变。其中大多数接受了第三代EGFR TKI治疗。27名患者在肿瘤进展后继续接受阿法替尼治疗;这种策略延缓了疾病症状的进展。至临床症状进展的中位时间为16.3个月。 包括在几家西班牙医院接受一线阿法替尼治疗的45名患者的回顾性现实研究显示,ORR为68.9 %,CR和PR率分别为13.3 %和55.6 %[7]。疾病稳定的发生率为17.8 %。中位PFS为27个月,因此超过了临床试验中获得的结果,并且尚未达到OS。作者推测,有利的PFS结果可能是由于存在较大比例的携带外显子19缺失肿瘤的患者,他们对阿法替尼具有极佳的应答。 对相同队列的患者进行了针对高龄组中阿法替尼活性的分析[8]。中位年龄为71.2岁,其中24名患者(53.3 %)≥ 70岁。当然,与年轻患者相比,老年人需要治疗中断和剂量调整的频率更高,但这似乎并未损害安全性或疗效。阿法替尼剂量在47.6 %的< 70岁患者和75 %的年龄≥ 70岁患者中减少。由于AE而必要的治疗中止分别为14.3 %与20.8 %。使用阿法替尼获得的ORR分别为76 %与62.5 %,疾病控制率分别为90.3 %与83.3 %。中位PFS在年轻组中为20个月,但在老年患者中尚未达到。
某些突变的临床意义
一项台湾分析回顾性评价了269名EGFR突变NSCLC和脑转移患者的结果[9]。EGFR突变被分类为外显子19缺失、L858R突变和罕见突变。结果表明,突变相关差异涉及疾病的自然史和脑转移患者的预后,其中罕见突变导致较差的结果。外显子19缺失、L858R突变和罕见突变患者的中位PFS分别为10.4、10.0和3.2个月(p = 0.03)。OS分别为18.1、17.4和12.5个月(p=0.05)。与吉非替尼相比,使用阿法替尼进行治疗证明是对于PFS(HR,0.57;p=0.03)和OS(HR,0.48;p = 0.03)有利的预后因素。 在意大利进行的一项观察性研究的目标是根据EGFR T790M耐药性突变存在的临床特征和进展模式[10]。该队列包括219名在使用吉非替尼、厄洛替尼或阿法替尼一线治疗后发生进展的EGFR突变NSCLC患者。49 %的患者获得T790M突变。T790M的出现显示与年龄< 65岁(p = 0.05)和外显子19缺失的存在(p = 0.04)相关。通过多变量分析证实了这种关联(分别为p = 0.010和p = 0.006)。在进展时,T790M阳性组更常显示新的进展位点(p = 0.005)以及肝转移(p<0.001)。多变量分析证实了该观察结果的统计显著性(分别为p = 0.01和p = 0.008)。单变量和多变量分析均显示T790M阳性患者较长的中位OS(根据单变量分析,53与22个月;p < 0.0001)。
早期ctDNA清除:一线奥希替尼……
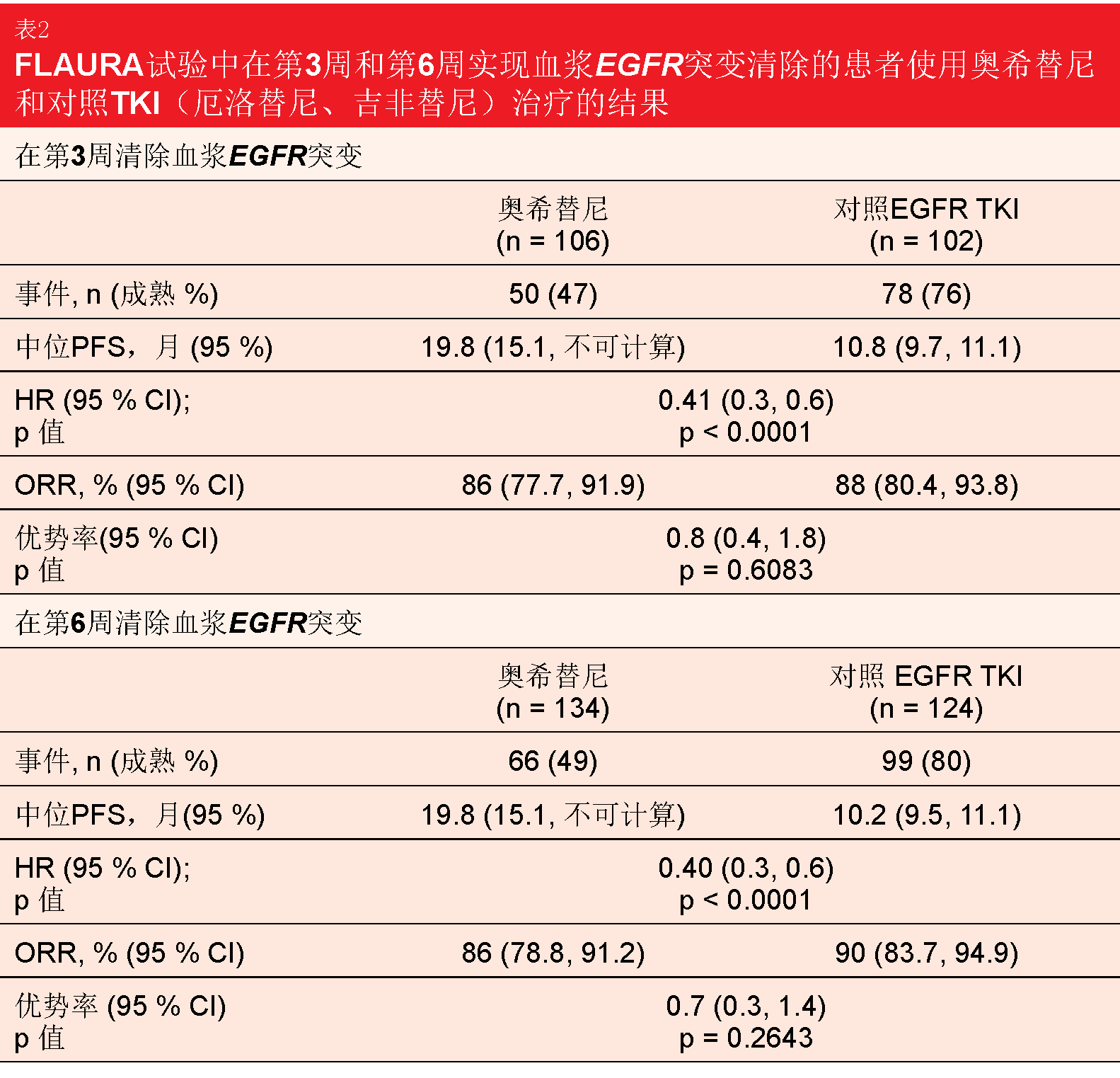
在双盲随机化III期FLAURA试验中,使用奥希替尼的一线治疗相比于使用厄洛替尼或吉非替尼的EGFR TKI治疗在EGFR阳性晚期NSCLC患者中带来更高的PFS[3]。在AURA试验中发现循环肿瘤DNA(ctDNA)的早期清除与PFS改善相关[11,12]。Zhou等人介绍了FLAURA中在治疗开始后3周或6周对EGFR突变检测相关的临床结果的探索性分析,以确定早期ctDNA清除是否预测PFS和ORR[13]。奥希替尼和对照组中分别有244和245名患者在基线和第3周和/或第6周时可获得可评估的ctDNA结果。 事实上,血浆EGFR突变的早期清除似乎是结果改善的预后因素。在第3周(13.5与9.5个月;HR,0.57;p< 0.0001)和第6周(13.5与8.2个月;HR,0.51;p<0.0001),显示EGFR突变清除的患者相比于未显示EGFR突变清除的患者的PFS显著延长。在经历EGFR突变清除的患者组中,接受奥希替尼的患者在第3周(19.8与10.8个月;HR,0.41;p< 0.0001)和第6周(19.8与10.2个月;HR,0.40;p < 0.0001;表2)均显示显著更长的PFS。同样,在第3周未实现清除的情况下,奥希替尼治疗的患者在PFS方面的表现显著优于第一代EGFR TKI治疗的患者(11.3与7.0个月;HR,0.50;p = 0.001)。在第6周时,分析显示有利于奥希替尼的趋势。在治疗开始前,持续存在EGFR突变指示较差的结果,中位PFS为11.1个月,而获得清除的患者为19.1个月。ORR在各组之间通常相似,没有任何统计学意义,范围从73 %到90 %。 总体而言,这些数据表明,可以早期鉴别使用一线奥希替尼治疗而具有较高快速进展或死亡风险的患者。目前正在对治疗过程中的其他时间点进行一系列分析。进一步分析正在研究具有可检测EGFR突变的患者在EGFR TKI治疗后具有高风险较早发生进展背后的机制。
……和后线奥希替尼
类似地,Song等人展示在预先治疗条件下奥希替尼治疗起始后50天内的ctDNA清除可作为预测和预后标志物[14]。研究人员在52名患者中对ctDNA随时间的变化进行了评估,这52名患者来自ASTRIS研究患有T790M阳性晚期NSCLC,且在EGFR TKI治疗后发生进展。根据分析,在奥希替尼治疗起始后50天内的首次随访时具有不可检测ctDNA的患者相比于具有可检测ctDNA的患者拥有显著更长的PFS和OS(PFS,p = 0.022;OS,p = 0.009)。 此外,发现揭示了ctDNA在疾病进展早期检测中的潜力。34 %的患者在放射学进展之前发生分子进展,平均提前时间为2.5个月。这些患者在放射学进展时更可能携带拷贝数扩增(CNA)和TP53突变,其中CNA的存在表明PFS和OS相比于不存在CNA的患者有所缩短。考虑到这些进一步了解,首次随访时对ctDNA清除的评估可能值得推荐。
参考文献
- Nakagawa K et al., RELAY: A multicenter, double-blind, randomized phase 3 study of erlotinib in combination with ramucirumab or placebo in previously untreated patients with epidermal growth factor receptor mutation-positive metastatic non-small cell lung cancer. J Clin Oncol 37, 2019 (suppl; abstr 9000)
- Noronha V et al., Phase III randomized trial comparing gefitinib to gefitinib with pemetrexed-carboplatin chemotherapy in patients with advanced untreated EGFR mutant non-small cell lung cancer (gef vs gef+C). J Clin Oncol 37, 2019 (suppl; abstr 9001)
- Soria JC et al., Osimertinib in untreated EGFR-mutated advanced non-small-cell lung cancer. N Engl J Med 2018; 378(2): 113-125
- Kobayashi Y, Mitsudomi T. Not all epidermal growth factor receptor mutations in lung cancer are created equal: Perspectives for individualized treatment strategy. Cancer Sci 2016; 107(9): 1179-1186
- Jänne PA et al., Antitumor activity of TAK-788 in NSCLC with EGFR exon 20 insertions. J Clin Oncol 37, 2019 (suppl; abstr 9007)
- Li Y et al., Afatinib in the treatment of advanced NSCLC with EGFR mutation: An observational real-world study. J Clin Oncol 37, 2019 (suppl; abstr e20518)
- Busto SA et al., Real-world clinical experience of the Galician Lung Cancer Group: Afatinib in patients with EGFR positive mutation. J Clin Oncol 37, 2019 (suppl; abstr e20654)
- Busto SA et al., Galician lung cancer group: Afatinib data as first-line treatment for elderly patients. J Clin Oncol 37, 2019 (suppl; abstr e20662)
- Kuan FC et al., Real-world outcome analysis of EGFR-mutated lung adenocarcinoma with brain metastases. J Clin Oncol 37, 2019 (suppl; abstr e13588)
- Pasello G et al., Clinical features and progression pattern of T790M+ compared with T790M-EGFR mutant NSCLC. J Clin Oncol 37, 2019 (suppl; abstr e20612)
- Thress KS et al., Complete clearance of plasma EGFR mutations as a predictor of outcome on osimertinib in the AURA trial. J Clin Oncol 2017; 35 (Suppl 15): 9018
- Shepherd FA et al., Early clearance of plasma EGFR mutations as a predictor of response to osimertinib in the AURA3 trial. J Clin Oncol 2018; 36 (Suppl 15): 9027
- Zhou C et al., Early clearance of plasma EGFR mutations as a predictor of response to osimertinib and comparator EGFR-TKIs in the FLAURA trial. J Clin Oncol 37, 2019 (suppl; abstr 9020)
- Song Y et al., Predictive and prognostic values of circulation tumor DNA clearance in osimertinib-treated advanced non-small cell lung cancer cohort. J Clin Oncol 37, 2019 (suppl; abstr 3036)
More posts
小细胞肿瘤:二线条件下的改善
小细胞肿瘤:二线条件下的改善 Lurbinectedin单药疗法 对于复发性小细胞肺癌(SCLC)患者,仅可获得有限的治疗选择。拓扑替康(topotecan)是唯一经FDA
罕见突变:使治疗更进一步
罕见突变:使治疗更进一步 GEOMETRY mono-1:MET失调NSCLC中的capmatinib 据报道,3 %至4 %的NSCLC患者具有MET外显子14跳跃突变(
ALK阳性疾病基于血液的检测
ALK阳性疾病基于血液的检测 Rafał Dziadziuszko,MD,PhD,波兰格但斯克,格但斯克医学院肿瘤及放射学系 在现今的肺癌诊断和治疗环境中,我们可以对循环
免疫疗法领域的试验更新和新生物标志物
免疫疗法领域的试验更新和新生物标志物 派姆单抗(pembrolizumab)的 长期发现:KEYNOTE-001 KEYNOTE-001是证明PD-1抑制剂派姆单抗在初治或
EGFR突变肺癌的新一线选择和其他见解
EGFR突变肺癌的新一线选择和其他见解 RELAY:添加雷莫芦单抗(ramucirumab) 尽管EGFR TKI治疗通常对EGFR突变肺癌患者有效,但耐药性在治疗开始后8
早期NSCLC:有前景的(新)辅助方法
早期NSCLC:有前景的(新)辅助方法 NEOSTAR试验 可切除非小细胞肺癌(NSCLC)患者需要有效的治疗选择,因为超过半数的I期至III期疾病患者经历复发[1]。Ch