Opciones terapéuticas en expansión para los pacientes con CPNM con mutaciones raras: ALK, ROS1, MET, BRAF
En el 4 % a 5 % de todos los pacientes de raza blanca y asiáticos con cáncer de pulmón no microcítico (CPNM) avanzado se producen reordenamientos del gen ALK. Crizotinib fue el primer inhibidor de ALK autorizado y representa el estándar de tratamiento de primera línea actual para el CPNM con ALK positivo. Sin embargo, a pesar de observarse respuestas iniciales al tratamiento con inhibidores de la tirosina kinasa (ITK), todos estos pacientes presentan recidivas a largo plazo. Ello obedece principalmente a mutaciones secundarias en los dominios kinasa de ALK o ROS1, o a una penetración escasa del fármaco en el SNC. Se han observado mutaciones secundarias en aproximadamente el 25 % de los pacientes con resistencia a crizotinib [1, 2]. La investigación se está centrando en el desarrollo de nuevas opciones para los contextos de primera línea y resistente.
Ensayo en el contexto de primera línea J-ALEX: alectinib frente a crizotinib
Alectinib es un inhibidor de ALK sumamente selectivo y potente con actividad en el sistema nervioso central (SNC) y contra mutaciones de resistencia en ALK. En el estudio fase III J-ALEX se comparó alectinib 300 mg dos veces al día (n = 103) con crizotinib 250 mg dos veces al día (n = 104) en pacientes con CPNM estadio IIIB/IV o recurrente con ALK positivo no tratados previamente con inhibidores de ALK [3]. Pudieron participar pacientes con metástasis cerebrales tratadas o asintomáticas.
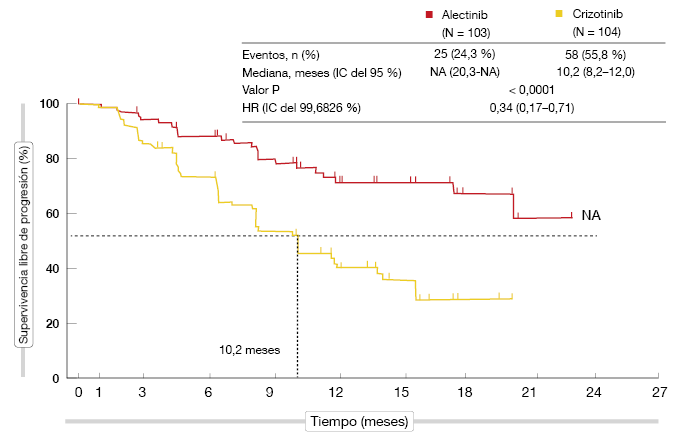
El estudio J-ALEX ya ha cumplido su objetivo principal, la supervivencia libre de progresión (SLP), en un análisis interino previsto de antemano, según lo evaluado por un centro de revisión independiente. Estos resultados sugirieron la existencia de una diferencia muy significativa a favor de alectinib (mediana de SLP, no alcanzada frente a 10,2 meses; hazard ratio [HR], 0,34; p > 0,0001; Figura). Casi todos los pacientes obtuvieron un beneficio en SLP del tratamiento con alectinib, según un análisis de subgrupos. La tasa de respuestas objetivas (TRO) evaluada por el centro de revisión independiente fue del 91,6 % y 78,9 % con alectinib y crizotinib, respectivamente. Los gráficos en cascada indicaron una mayor contracción tumoral en el brazo de alectinib.
Alectinib fue bien tolerado y mostró un perfil favorable de acontecimientos adversos (AA). Se notificaron estreñimiento, nasofaringitis, disgeusia, náuseas, fiebre, diarrea y vómitos en pacientes de ambos brazos. Todos estos AA se produjeron con menor frecuencia con alectinib que con crizotinib y, en ocasiones, con una diferencia muy notable. También sucedió así con la elevación de las enzimas hepáticas. Las tasas de AA grado 3/4 se redujeron a la mitad con alectinib en comparación con crizotinib (26,2 % frente al 51,9 %) y las tasas de AA que motivaron la discontinuación del tratamiento o interrupciones de la administración fueron sustancialmente menores en el brazo experimental que en el brazo control. En conjunto, estos resultados sugieren que alectinib tiene el potencial de convertirse en un nuevo estándar de tratamiento de primera línea para los pacientes con CPNM con ALK positivo.
Figura: Estudio-J-ALEX: superioridad de alectinib respecto a crizotinib en cuanto a SLP (población IT)
Brigantinib en pacientes refractarios a crizotinib: ALTA
Brigantinib es un ITK de ALK de última generación en investigación, que se diseñó para tener una actividad potente y amplia frente a mutaciones de resistencia en ALK. Los datos de fase II presentados en el congreso de la ASCO demostraron la actividad de este fármaco tras la progresión con crizotinib. En el ensayo de evaluación de dosis, internacional y aleatorizado ALTA se evaluó brigantinib en pacientes con CPNM localmente avanzado o metastásico con ALK positivo [4]. Los pacientes recibieron brigantinib, a dos dosis distintas, de forma aleatorizada: 180 mg una vez al día (n = 110), precedida de una preinclusión de 7 días con 90 mg, o 90 mg una vez al día (n = 112). El objetivo principal fue la TRO según los criterios RECIST.
Los pacientes de los grupos de brigantinib 180 y 90 mg presentaron una TRO confirmada del 54 % y 45 %, respectivamente. La mayoría experimentó una respuesta parcial (RP). Se produjeron respuestas completas (RC) confirmadas en 4 y 1 pacientes, respectivamente. Las TRO no difirieron según los antecedentes de quimioterapia. La mayoría de los pacientes de ambos grupos presentaron reducciones del tamaño del tumor. Se logró el control de la enfermedad en el 86 % y 82 % de los pacientes, respectivamente. La mediana de SLP fue superior a un año en el grupo de 180 mg (12,9 meses), mientras que fue de tan solo 9,2 meses en el de 90 mg. Al cabo de un año, el 54 % y 39 % de los pacientes seguían vivos y libres de progresión, respectivamente. La mediana de supervivencia global (SG) aún no se había alcanzado en ninguno de los grupos. Las proporciones de pacientes vivos al cabo de un año fueron del 80 % y 71 %, respectivamente.
Actividad frente a lesiones cerebrales
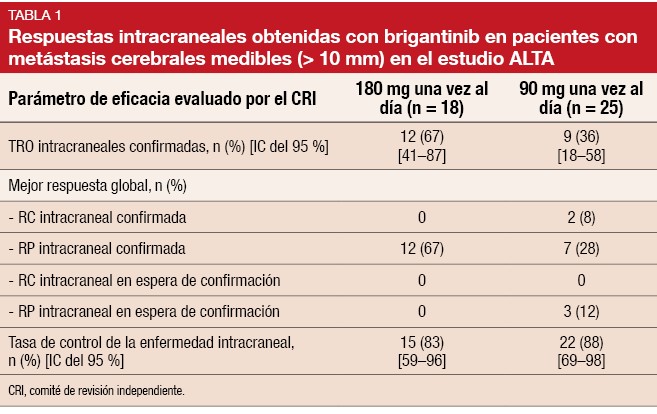
Se produjeron respuestas intracraneales en ambos grupos de dosis, de acuerdo con la evaluación de un comité de revisión independiente. En los pacientes con lesiones medibles (≥ 10 mm), las TRO intracraneales confirmadas fueron del 67 % y 36 % con las dosis de 180 y 90 mg, respectivamente. Se obtuvo el control de la enfermedad intracraneal en el 83 % y 88 % de los pacientes, respectivamente (Tabla 1). Los pacientes con metástasis cerebrales activas y medibles (sin radioterapia previa o con progresión después de la radioterapia) en el momento basal lograron TRO intracraneales del 73 % y 37 %, respectivamente. La mediana de SLP intracraneal no se había alcanzado con la pauta de 180 mg y fue de 15,6 meses con la de 90 mg.
Brigantinib presentó un perfil aceptable de seguridad en ambos brazos. Los AA notificados con mayor frecuencia fueron náuseas, diarrea, cefalea, tos y cansancio. Las tasas de AA grado 3/4 fueron bajas. Los autores llegaron a la conclusión de que brigantinib tiene el potencial de convertirse en una nueva opción terapéutica para los pacientes con CPNM con ALK positivo resistente a crizotinib. Los resultados de eficacia y seguridad respaldan la elección de la pauta de 180 mg para futuros ensayos. En un estudio fase III aleatorizado se está comparando actualmente brigantinib 180 mg con crizotinib en pacientes no tratados previamente con inhibidores de ALK.
Nuevo compuesto inhibidor de ALK y ROS1: lorlatinib
Lorlatinib es un nuevo inhibidor de ALK macrocíclico que es capaz de penetrar en el SNC. Ha mostrado actividad contra una amplia gama de mutaciones que confieren resistencia a los inhibidores de ALK y también es un inhibidor potente de ROS1.
Solomon y cols. presentaron el componente de escalada de dosis de un estudio fase I/II en curso en el que se evalúa lorlatinib una o dos veces al día en 54 pacientes con CPNM avanzado con ALK/ROS1 positivos [5]. Estos pacientes no habían sido tratados previamente o habían experimentado progresión de la enfermedad después de recibir, como mínimo, un ITK de ALK/ROS1 previo. Se permitió cualquier tipo de quimioterapia previa. Tenía que haber presencia de enfermedad extracraneal medible. Se permitió la existencia de metástasis asintomáticas en el SNC (tratadas o no tratadas); el 72 % de los pacientes tenía metástasis cerebrales. La actividad intracraneal de lorlatinib se evaluó de manera prospectiva mediante resonancia magnética (RM).
Lorlatinib mostró una actividad clínica sólida en pacientes con ALK y ROS1 positivos. Este tratamiento produjo tres RC y 16 RP, lo que deparó una TRO del 46 %. Los pacientes que ya habían recibido un ITK de ALK presentaron una TRO del 57 %, mientras que los ya tratados con al menos dos ITK de ALK lograron una TRO del 42 %. La mayoría mostró una reducción del tamaño de las lesiones diana. En 20 pacientes, las respuestas seguían en curso en la fecha de corte de los datos. La mediana de SLP fue de 11,4 meses en la cohorte completa. Al cabo de un año, el 41 % se encontraban libres de progresión. Al igual que con la TRO, el grupo que ya había recibido un único ITC de ALK mostró una mejor evolución en cuanto a SLP que los que habían sido tratados con dos o más ITK (SLP, 13,5 frente a 9,2 meses). El tratamiento con lorlatinib desencadenó respuestas intracraneales significativas. Según la evaluación intracraneal prospectiva, se produjeron cinco RC y dos RP confirmadas en 18 pacientes con enfermedad intracraneal medible, lo que supuso una tasa de respuestas intracraneales confirmadas del 39 %. Tres de los cuatro pacientes con ROS1 positivo y enfermedad intracraneal medible experimentaron reducciones tumorales. También se observaron respuestas en pacientes con afectación leptomeníngea.
La hipercolesterolemia fue el AA relacionado con el tratamiento más frecuente, aunque fue asintomática y se controló fácilmente con estatinas. Con la dosis recomendada para la fase II de 100 mg una vez al día se observaron otros AA, como edema periférico, hipertrigliceridemia y ralentización del habla. La parte de fase II de este estudio se está llevando a cabo en 57 centros de todo el mundo.
Crizotinib en el CPNM con alteraciones en MET
En el 3 % a 4 % de los pacientes con CPNM no epidermoide se producen mutaciones en el protoncogén conocido MET que originan una disminución de la degradación de MET. Las alteraciones en el exón 14 de MET representan un grupo heterogéneo de mutaciones. Aunque muchas de ellas producen saltos del exón 14 de MET, determinadas mutaciones puntuales o deleciones ocasionan la misma biología sin causar saltos exónicos. En el 15 % a 20 % de los casos se identifica una amplificación simultánea de MET.
Crizotinib se desarrolló en un principio como inhibidor de MET y se está evaluando actualmente en pacientes con CPNM avanzado con alteraciones en el exón 14 de MET en el estudio fase I, abierto y multicéntrico PROFILE 1001. Los resultados presentados en el congreso de la ASCO demostraron que, en estos pacientes, crizotinib presenta actividad antitumoral y, en general, un perfil tolerable de AA, algo consistente con lo ya descrito en pacientes con CPNM con ALK positivo o reordenamiento de ROS1 [6].
Participaron 21 pacientes que recibieron crizotinib a dosis inicial de 250 mg dos veces al día. Ninguno de los tumores tenía alteraciones simultáneas en ALK o ROS1. El tratamiento con crizotinib deparó una TRO del 44 % en el estudio PROFILE 1001. En casi todos los pacientes se logró una contracción del tumor. Las respuestas se observaron normalmente desde etapas tempranas y la mayoría de los pacientes continuaron en el estudio; la respuesta persistente más prolongada fue de aproximadamente un año. No pudo calcularse la mediana de SLP y SG, ya que en la fecha de corte de los datos no se habían producido muertes ni casos de progresión de la enfermedad.
Los AA relacionados con el tratamiento predominantes fueron edema, náuseas, diarrea y trastorno de la visión y la mayoría de ellos se consideraron de grado 1 o 2. Según los autores del ensayo, están justificados nuevos estudios de crizotinib en esta población de pacientes.
Mutación en BRAF como diana
En el 1 % a 2 % de los pacientes con adenocarcinoma de pulmón se observan mutaciones V600E en BRAF. Entre estas mutaciones, el 70 % son del tipo V600E. El CPNM con mutación V600E de BRAF tiene características histológicas indicativas de un tumor agresivo y los pacientes tienen un pronóstico menos favorable cuando reciben quimioterapia basada en platino.
Una estrategia dirigida eficiente en este grupo consiste en utilizar dabrafenib, un inhibidor de BRAF de molécula pequeña, en combinación con trametinib, otra molécula pequeña que actúa como inhibidor alostérico de MEK1 y MEK2. En conjunto, estos fármacos provocan una inhibición dual de la vía de MAPK. En el estudio fase II, abierto, no aleatorizado y con varias cohortes BRF113928, en el que participaron 78 pacientes con CPNM estadio IV con mutación V600E de BRAF, la monoterapia con dabrafenib deparó una TRO del 33 % y una mediana de SLP de 5,5 meses tras el fracaso de más de un tratamiento previo basado en platino para la enfermedad avanzada (cohorte A) [7]. En el congreso de la ASCO, Planchard y cols. presentaron el análisis principal de la cohorte B de este estudio; estos pacientes fueron tratados con la combinación de dabrafenib 150 mg dos veces al día y trametinib 2 mg una vez al día tras haber recibido un mínimo de una quimioterapia basada en platino y no más de tres líneas previas de tratamiento [8]. El objetivo principal fue la TRO según la evaluación del investigador.
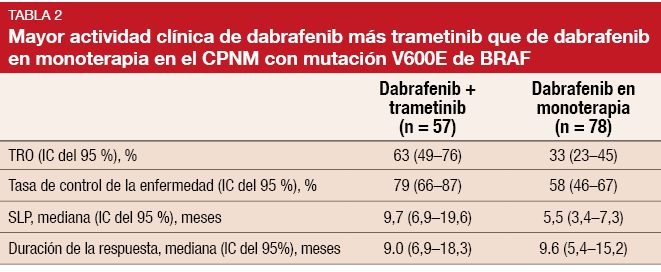
Cincuenta y siete pacientes fueron evaluables en cuanto a respuesta, todos ellos con histología no epidermoide. En este grupo, la TRO fue del 63 %, con una tasa de control de la enfermedad del 79 %. La mediana de duración de la respuesta fue de 9,0 meses y la mitad de las respuestas confirmadas seguían presentes en el momento del análisis. El análisis deparó una mediana de SLP de 9,7 meses. En comparación con la monoterapia con dabrafenib (cohorte A del estudio BRF113928), el tratamiento con dabrafenib más trametinib mostró una mayor actividad clínica (Tabla 2).
El perfil de AA fue controlable y semejante al observado anteriormente en el tratamiento de pacientes con melanoma. Los AA comprendieron fiebre, náuseas, vómitos, diarrea, astenia, pérdida de apetito, escalofríos, edema periférico y sequedad cutánea. En conjunto, la combinación de dabrafenib y trametinib constituye una opción terapéutica importante para los pacientes con CPNM con mutación V600E de BRAF.
BIBLIOGRAFÍA
- Doebele RC et al., Mechanisms of resistance to crizotinib in patients with ALK gene rearranged non-small cell lung cancer. Clin Cancer Res 2012; 18: 1472-1482
- Zou HY et al., PF-06463922 is a potent and selective next-generation ROS1/ALK inhibitor capable of blocking crizotinib-resistant ROS1 mutations. PNAS 2015; 112: 3493-3498
- Nokihara H et al., Alectinib versus crizotinib in ALK inhibitor naïve ALK-positive non-small cell lung cancer: primary results from the JALEX study. J Clin Oncol 34, 2016 (suppl; abstr 9008) REFERENCES
- Kim D-W et al., Brigatinib in patients with crizotinib- refractory ALK+ non-small cell lung cancer: first report of efficacy and safety from a pivotal randomized phase 2 trial (ALTA). J Clin Oncol 34, 2016 (suppl; abstr 9007)
- Solomon BJ et al., Safety and efficacy of lorlatinib (PF-06463922) from the dose-escalation component of a study in patients with advanced ALK+ or ROS1+ non-small cell lung cancer (NSCLC). J Clin Oncol 34, 2016 (suppl; abstr 9009)
- Drilon AE et al., Antitumor activity and safety of crizotinib in patients with advanced MET exon 14-altered non-small cell lung cancer. J Clin Oncol 34, 2016 (suppl; abstr 108
- Planchard D et al., Dabrafenib in patients with BRAF(V600E)-positive advanced non-smallcell lung cancer: a single-arm, multicentre, open-label, phase 2 trial. Dabrafenib plus trametinib. Lancet Oncol 2016; 17(5): 642-650
- Planchard D et al., An open-label phase 2 trial of dabrafenib in combination with trametinib in patients with previously treated BRAF V600E– mutant advanced non-small cell lung cancer (BRF113928). J Clin Oncol 34, 2016 (suppl; abstr 107)