Los inhibidores de ALK de la siguiente generación destacan después del fracaso de crizotinib
Se observa cáncer de pulmón con gen de fusión ALK-positivo en un 5 % de los pacientes con CPNM avanzado [1] El inhibidor de ALK crizotinib tiene una eficacia inicial significativa en pacientes con CPNM avanzado ALK-positivo.
Sin embargo, la mayoría de los pacientes presentan finalmente resistencia, y el sistema nervioso central (SNC) es uno de los lugares más frecuentes de la primera progresión. Alrededor de la mitad de estos pacientes presentan metástasis en el SNC durante el tratamiento con crizotinib. Los inhibidores de ALK de la siguiente generación son opciones eficaces en los pacientes cuya enfermedad progresa durante el tratamiento con crizotinib.
ASCEND-5
Ceritinib es un inhibidor de ALK de la siguiente generación con una potencia 20 veces mayor que crizotinib [2]. Los efectos antitumorales de ceritinib en pacientes tratados previamente se demostraron en los ensayos ASCEND-1 y ASCEND-2 [3-5]. En ASCEND-2, el tratamiento con ceritinib obtuvo respuestas duraderas en toda la población con CPNM ALK-positivo que habían progresado durante la quimioterapia y crizotinib, incluidos pacientes con metástasis cerebrales [5].
En el Congreso de la ESMO, Scagliotti y cols. presentaron el estudio de confirmación en fase III ASCEND-5, en el que se comparó ceritinib con quimioterapia de segunda línea en el contexto de tratamiento previo con crizotinib [6]. En este ensayo internacional, aleatorizado y abierto se aleatorizó a 231 pacientes con CPNM ALK positivo localmente avanzado o metastásico procedentes de 99 centros de 20 países. Antes de incorporarse al estudio habían recibido una o dos pautas de quimioterapia para enfermedad avanzada, así como crizotinib (en cualquier momento). El tratamiento consistió en ceritinib 750 mg/día o quimioterapia con pemetrexed o docetaxel. La SSP se definió como el criterio de valoración principal del estudio. En cada grupo, más de la mitad de los pacientes tenían enfermedad metastásica cerebral, y se había administrado radioterapia en el SNC en un tercio de los casos.
Amplios efectos beneficiosos del tratamiento con ceritinib
El tratamiento con este inhibidor de ALK resultó ser muy eficaz, con mejorías significativas de la SSP, tanto desde el punto de vista estadístico como clínico, según el comité independiente de revisión enmascarado (CIRB; 5,4 frente a 1,6 meses; HR, 0,49; p < 0,001). Este efecto fue sólido y constante en diversos subgrupos. El efecto beneficioso clínico fue corroborado por la TRO (39,1% frente al 6,9 %) y la TCE (76,5 % frente al 36,2 %). Los datos de la SG eran inmaduros en la fecha de corte de los datos. El perfil de seguridad fue equivalente al de las observaciones en estudios anteriores de ceritinib y caracterizado principalmente por diarrea, náuseas, vómitos y elevación de las transaminasas.
El análisis de los resultados comunicados por los pacientes demostró que, en comparación con la quimioterapia. ceritinib había mejorado significativamente los síntomas específicos del cáncer de pulmón y el estado general de salud. Aunque la mayoría de los síntomas evaluados con el cuestionario QLQ-C30 mejoraron con el tratamiento de ceritinib, se observó cierto deterioro con el inhibidor de ALK en dos escalas de síntomas digestivos (es decir, diarrea, náuseas y vómitos). Los autores llegaron a la conclusión de que estos resultados sitúan a ceritinib como opción terapéutica preferente en pacientes con CPNM ALK-positivo resistente a crizotinib.
Seguimiento a largo plazo de ASCEND-3: datos destacables
Felip y cols. presentaron el seguimiento a largo plazo del estudio internacional en fase II, de un solo grupo y abierto ASCEND-3, en el que se evaluó ceritinib en 124 pacientes con CPNM metastásico ALK-positivo que no habían recibido antes inhibidores de ALK [7]. Había pacientes sin quimioterapia previa (aunque solo dos) o tratados con hasta tres líneas de quimioterapia y que habían experimentado progresión durante o después de la última pauta. Se permitió la existencia de metástasis cerebrales asintomáticas o neurológicamente estables en el momento basal. El 40 % de los pacientes tenía lesiones cerebrales en el momento de la incorporación al estudio; se había aplicado radioterapia local en el 53,1 %. El criterio de valoración principal fue la TRO según el investigador.
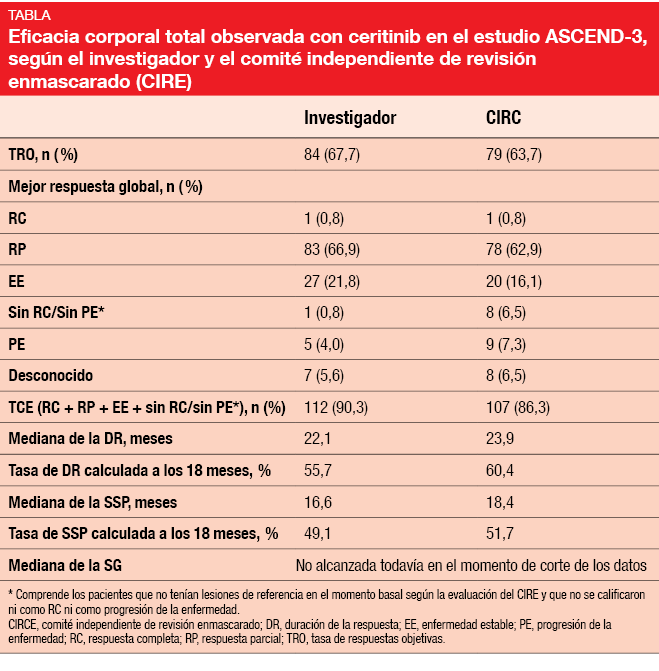
Después de una mediana de seguimiento de 25,9 meses, permanecían con tratamiento el 48,4 % de los pacientes. Con respecto a la eficacia corporal total, el análisis proporcionó datos sólidos de TRO, del 67,7 % según el investigador y del 63,7 % según el CIRE (Tabla). Se produjeron disminuciones de la masa tumoral con respecto al momento basal en el 94,7 % de los pacientes. Se logró el control de la enfermedad en el 90,3 % y el 86,3 %, según el investigador y el CIRE, respectivamente. El estudio reveló resultados destacables en la mediana de la SSP (16,6 y 18,4 meses según el investigador y el CIRE, respectivamente) y en la SG: a los 24 meses estaban vivos el 67,5 % de los pacientes y todavía no se había alcanzado la mediana de la SG. Ceritinib también mostró actividad en pacientes con metástasis cerebrales. Los pacientes con lesiones en el SNC en el momento basal obtuvieron una TRO corporal total del 57,1 % y una mediana de la SSP de 10,8 meses. Se observaron respuestas intracraneales globales en el 61,5 %.
Los resultados actualizados comunicados por los pacientes en un seguimiento de hasta 29 ciclos fueron concordantes con los publicados anteriormente. Los pacientes experimentaron mejorías de los síntomas con respecto al momento basal, con una variación media de la puntuación global de la Escala de síntomas en el cáncer de pulmón que osciló entre – 3,39 y – 14,83. La calidad de vida se mantuvo durante el tratamiento.
Alectinib: actualización de datos fundamentales
Alectinib, un inhibidor oral de ALK muy potente y selectivo, ha sido aprobado por la FDA para el tratamiento de los pacientes que progresan durante el tratamiento con crizonitib o no lo toleran. Esta aprobación se basa en dos estudios fundamentales en fase II, el ensayo NP28673 internacional y el ensayo NP28761 norteamericano [8 – 11]. Participaron en estos estudios 225 pacientes con CPNM ALK-positivo localmente avanzado o metastásico y tratados anteriormente, que habían progresado después del tratamiento previo con crizotinib. Todos los pacientes recibieron alectinib 600 mg por vía oral dos veces al día.
El análisis actualizado de la seguridad y la eficacia del estudio NP28673 se presentó en la ESMO 2016 y demostró una gran eficacia y una buena tolerabilidad de alectinib, tanto sistémica como en el SNC [12]. La TRO de los pacientes evaluables respecto a la respuesta fue del 50,8 % según el comité de revisión independiente. Los pacientes sin quimioterapia previa experimentaron un efecto beneficioso mayor que los tratados anteriormente con quimioterapia (TRO, 73,1 % y 44,8 %, respectivamente). La TCE fue del 78,7( %) en los pacientes con respuesta evaluable. La mediana de la SSP fue de 8,9 meses en la población por intención de tratar y la mediana de la SG, de 26,0 meses. Los pacientes con enfermedad mensurable en el SNC en el momento basal tuvieron una TRO en el SNC del 58,8 %.
En un análisis exploratorio se evaluó el tiempo transcurrido hasta la respuesta tanto en NP28673 como en NP28761 [13]. La determinación de la rapidez con que los pacientes obtienen un efecto beneficioso con alectinib se calificó como importante tanto para los pacientes asintomáticos como para los pacientes a punto de presentar síntomas, sobre todo en el SNC. Además, la rapidez de la respuesta es importante para los pacientes con enfermedad activa en el SNC, como un campo con una gran necesidad médica no cubierta. Los datos demuestran que el tratamiento con alectinib puede lograr una respuesta rápida. La mayoría de los pacientes de todas las poblaciones obtuvo una respuesta RECIST en la primera evaluación (8 semanas en NP28673 y 6 semanas en NP28761). Esto se aplicó también al tiempo hasta la respuesta del SNC en pacientes con enfermedad mensurable o no mensurable en el SNC en el momento basal, con independencia de la radioterapia previa. Se necesitan nuevas investigaciones acerca del beneficio clínico precoz (< 6 semanas), a fin de evaluar alectinib como tratamiento inicial de las metástasis del SNC, con la posibilidad de evitar la radioterapia.
Notable actividad antitumoral de brigatinib
En un estudio en curso en fase I/II, de un solo grupo, multicéntrico, de aumento escalonado de la dosis y de ampliación de la dosis se está evaluando brigatinib, un inhibidor de ALK de la siguiente generación en fase de investigación, en pacientes con neoplasias malignas avanzadas, lo que incluye 79 pacientes con CPNM ALK-positivo. El 90 % de ellos habían recibido anteriormente tratamiento con crizotinib.
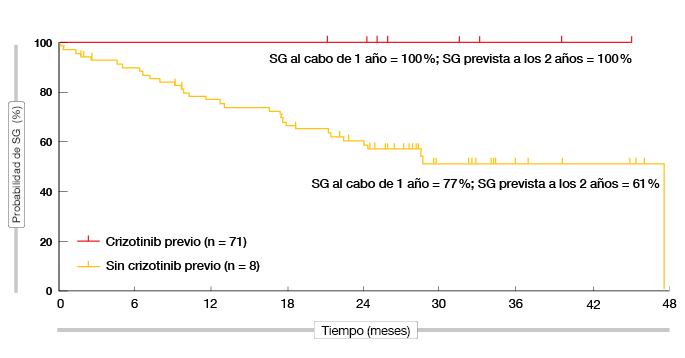
Datos actualizados sobre la actividad y seguridad de brigatinib en pacientes con CPNM ALK-positivo después de una mediana de tratamiento de 20 meses demuestran que con brigatinib se obtuvieron reducciones del tumor en casi todos los casos [14]. El 33 % de 72 pacientes evaluables experimentó una disminución del 100 % de las lesiones diana. La TRO confirmada alcanzó el 62 % con todas las dosis de brigatinib. El 100 % de los pacientes no tratados previamente con crizotinib consiguieron respuestas objetivas confirmadas, incluidas tres remisiones completas. Se logró el control de la enfermedad en el 87 %. La mediana de la SSP todavía no se había alcanzado en la población sin tratamiento previo con crizotinib y fue de 12,9 meses en los pacientes tratados anteriormente con crizotinib. En cuanto a la SG, las tasas al cabo de 1 año fueron del 100 % y del 77 % en estos dos grupos, respectivamente (Figura). Según el análisis de pacientes con metástasis cerebrales (n = 50), brigatinib fue muy activo en el SNC. La TRO intracraneal fue del 67 % en los pacientes con enfermedad basal mensurable. Los acontecimientos adversos más frecuentes surgidos durante el tratamiento consistieron en náuseas, cansancio, diarrea, cefalea y tos.
Los resultados de este estudio en fase I/II respaldan la realización de nuevas investigaciones con brigatinib en dosis de 90 mg/día y 180 mg/día. ALTA, un ensayo internacional y aleatorizado de evaluación de la dosis, demostró que brigatinib tiene potencial como nueva opción terapéutica en el contexto de resistencia a crizotinib [15]. Se ha iniciado un ensayo aleatorizado en fase III de brigatinib comparado con crizotinib en pacientes con CPNM ALK-positivo no tratados anteriormente con inhibidores de ALK (ALTA-1L; NCT02737501).
Figura: Supervivencia global lograda con brigatinib (Población por IT)
BIBLIOGRAFÍA
- Dearden S et al., Mutation incidence and coincidence in non small-cell lung cancer: meta-analyses by ethnicitiy and histology (mutMap). Ann Oncol 2013; 24(9): 2371-2376
- Friboulet L et al., The ALK inhibitor certinib overcomes crizotinib resistance in non-small lung cancer. Cancer Discov 2014; 4: 662-673
- Shaw AT et al., Ceritinib in ALK-rearranged non-small-cell lung cancer. Engl J Med 2014; 370: 1189-1197
- Kim DW et al., Activity and safety of ceritinib in patients with ALK-rearranged non-small-cell lung cancer (ASCEND-1): updated results from the multicentre, open-label, phase 1 trial. Lancet Oncol 2016; 17: 452-463
- Crinò L et al., Multicenter Phase II Study of Whole-Body and Intracranial Activity With Ceritinib in Patients With ALK-Rearranged Non-Small-Cell Lung Cancer Previously Treated With Chemotherapy and Crizotinib: Results From ASCEND-2. J Clin Oncol 2016; 34: 2866-2873
- Scagliotti G et al., Ceritinib versus chemotherapy in patients with advanced ALK+ NSCLC previously treated with chemotherapy and crizotinib: results from the confirmatory phase III ASCEND-5 study. ESMO 2016, abstract LBA_42
- Felip E et al., Phase II study of ceritinib in previously treated ALKi-naïve patients with ALK+ NSCLC: whole-body efficacy in all patients and in patients with baseline brain metastases. ESMO 2015, abstract 1208O
- Ou SH et al., Alectinib in crizotinib-refractory ALK-rearranged non-small-cell lung cancer: A phase II global study. J Clin Oncol 2016; 34: 661-668
- Barlesi F et al., Updated efficacy and safety results from a global phase 2, open-label, single-arm study (NP28673) of alectinib in crizotinib-refractory ALK+ non-small-cell lung cancer (NSCLC). Eur J Cancer 2015; 51(Suppl. 3): abstr 3101
- Shaw AT et al., Alectinib in ALK-positive, crizotinib-resistant, non-small-cell lung cancer: a single-group, multicentre, phase 2 trial. Lancet Oncol 2016; 17: 234-242
- Shaw AT et al., J Thorac Oncol 2015; 10 (Suppl. 2): abstr 1261
- Barlesi F et al., Updated efficacy and safety from the global phase II NP28673 study of alectinib in patients with previously treated ALK+ non-small-cell lung cancer (NSCLC). ESMO 2016, abstract 1263P
- Gandhi L et al., Time to response in patients with ALK+ NSCLC receiving alectinib in the phase II NP28673 and NP28761 studies. ESMO 2016, abstract 1209PD
- Bazhenova LA et al., Brigatinib in patients with anaplastic lymphoma kinase-positive non-small cell lung cancer in a phase 1/2 trial. ESMO 2016, abstract 1207PD
- Kim D-W et al., Brigatinib in patients with crizotinib-refractory ALK+ non-small cell lung cancer: first report of efficacy and safety from a pivotal randomized phase 2 trial (ALTA). J Clin Oncol 34, 2016 (suppl; abstr 9007)