16 ALK陽性疾患:治療の可能性が広がる
ALEX試験で確認されたアレクチニブのCNSおよび非CNSの有効性
ALK陽性進行非小細胞肺がん患者の標準治療には、第1世代ALK阻害薬クリゾチニブ、さらに最近では、セチニブおよびアレクチニブのような第2世代ALK TKIが含まれる。第III相ALEX試験では、ステージIIIB / IV ALK陽性非小細胞肺がん患者が投与されたクリゾチニブと比較して、CNS活性型ALK阻害剤アレクチニブを一次治療薬として使った。この試験では、無症候性脳転移が認められた。一次解析によれば、アレクチニブ治療によってPFSが改善した(推定不可能 vs. 11.1ヶ月; HR, 0.47; p < 0.0001) [1]。PFSは、独立審査委員会も優れていると推定した。(IRC; 25.7 vs. 10.4 ヶ月)さらに、被験群には、延長したDOR (推定不可能vs. 11.1 ヶ月; HR, 0.36)および改善した安全性プロファイルが認められた。
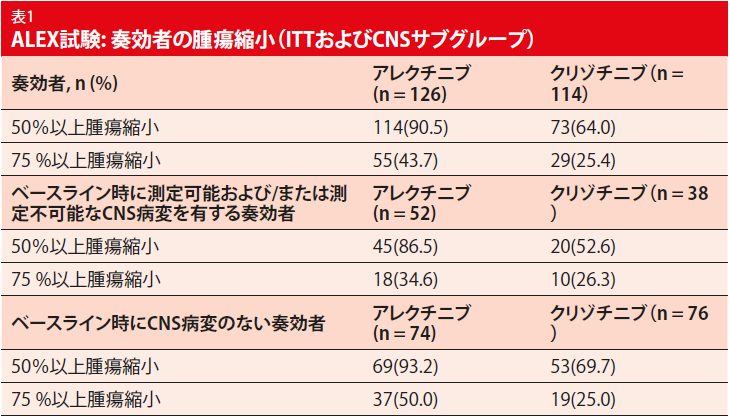
2018年ASCO学会で発表されたALEX試験の有効性と安全性に関する最新解析では、評価されたPFS (34.8 vs. 10.9 ヶ月; HR, 0.43) [2] に関して、アレクチニブのクリゾチニブに対する優位性が確認された。PFSベネフィットは、ベースラインのCNS転移の存在に関係なく発生した。PFS中央値は、脳病変の患者では27.7 vs 7.4 ヶ月 (HR, 0.35)であり、脳病変を有しない患者では34.8 vs. 14.7 ヶ月 (HR, 0.47)であった。両群では類似したORRにもかかわらず、(82.9 % vs 75.5 %)CNS転移の有無にかかわらず、アレクチニブで治療した患者は、より長い持続時間およびより大きな奏効の深さを示した。総体的に、奏効は、アレクチニブおよびクリゾチニブでそれぞれ33.1ヶ月 vs 11.1 ヶ月持続した。ITT集団では、アレクチニブおよびクリゾチニブ43.7 % vs 25.4 %でそれぞれ治療した奏効者が、75%以上の腫瘍縮小を示した (表 1)。CNS病変の有無関係なしに実験群の患者は顕著な腫瘍縮小を経験した。
アレクチニブは、より長い治療期間にもかかわらず、クリゾチニブと比較して一貫して良好な忍容性を示した。OSデータはまだ未完成です。これらのデータは、アレクチニブ投与をALK陽性非小細胞肺がんを有する患者の標準ファーストライン治療と裏付ける。
ALTA試験:ブリガチニブ最新情報
一方、第二世代の薬剤はあれども、がんの耐性と進行の出現は続くのでさらなる薬剤の開発を必要とする。現在進行中の無作為化第II相 ALTA試験では、過去にクリゾチニブを投与されたものの病勢進行した進行性ALK陽性非小細胞肺がん患者222人を対象に、次世代ALK阻害剤ブリガチニブを投与している。患者は、ブリガチニブ90mg QDの投与(A群)またはブリガチニブ90mg投与の後に180mgのQD(B群)を投与される。2018年ASCO学会で発表されたALTA試験の最新データおよび探索的解析は、この治療の継続的有効性を強調した[3]。
試験担当医が主要エンドポイントをORRとし、A群46%およびB群56%であった。病勢コントロール率は、それぞれA群81%およびB群86%であった。ベースラインCNS標的病変が1以上の患者では、ORRがA群43%およびB群61%であった。IRCによるPFSはA群9.2ヶ月およびB群16.7ヶ月であった。1年時点で、A群45%およびB群61%は進行がなく、生存していた。OS解析では、A群29.5ヶ月およびB群34.1ヶ月の中間結果が得られた。2年OSはA群55%とB群66%であった。
この治療は、CNSおよび非CNSの両方の標的病変において類似した奏効の深さを示した。測定可能なベースラインで脳転移を有する患者では、IRCあたりそれぞれ53%と67%の頭蓋内奏効率が確認され、頭蓋内病勢コントロール率は85%および83%であった。頭蓋内奏効率はそれぞれ9.4ヶ月および16.6ヶ月持続した。ベースラインで脳転移を有する患者では、頭蓋内PFSは12.8ヶ月および18.4ヶ月であった。
B群の16.7ヵ月のPFS中央値は、ブリガチニブの第I/II相試験において、同じレジメンを受けた過去にクリゾチニブ治療を受けたALK陽性非小細胞肺がん患者で見られる16.3ヶ月のPFSに非常に匹敵することに留意したい[4]。クロストライアルの比較は患者の特性と評価方法の違いによって制限されるが、現在まで報告されている次世代ALK阻害剤のクリゾチニブに続く薬剤として、最長のPFS中央値をもつ。ALK阻害剤未治療進行ALK陽性非小細胞肺がん患者に投与したクリゾチニブと比較したブリガチニブ180mg(リードイン期間と共に)を評価している無作為化第III相ALTA-1L試験は、すでに終了している。
ロルラチニブ:第II相深く耐性のある治療効果
現在進行中の多施設非盲検単施設第I/II相試験では、ALKまたはROS1陽性転移性非小細胞肺がん患者を対象に第3世代ALKおよびROS1 TKIロルラチニブを投与している。ロルラチニブはCNS活性である。第1世代および第2世代TKI治療中に生じる最もよく知られているALK耐性変異に対して広範囲の効力を示す。この試験では、ベースライン時の未治療の無症候性または治療済CNS転移が認められている。第I相では、ロルラチニブは、ALK陽性疾患を有する患者の間で臨床的に有意で持続性のある奏効(ORR, 46 %; DOR, 12.4ヶ月)を示したが、その多くは以前の ALK TKI療法のあとにCNS病変および病勢進行を経験していた。[5]
Besseらは、 ALK TKI 1剤以上による治療歴があるALK陽性非小細胞肺がん患者(n = 198)を対象にロルラチニブを検討した第II相部分において最新の有効性の結果を報告した[6]。患者198人のうち、131人(66%)がCNSを発生した。治療を受けた第II相患者、すなわち、ALK陽性とROS1陽性の両方の疾患を有する過去に治療を受けたことがある患者と未治療の患者を含めた患者(n = 275)についての安全性データを提示した。
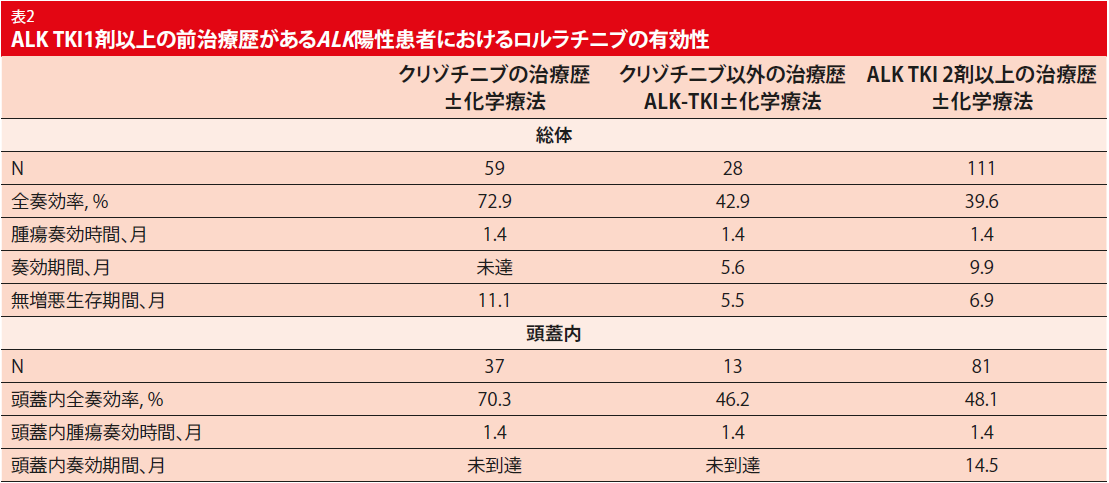
ロルラチニブは、クリゾチニブ、第2世代ALK TKIの1剤またはALK TKIを最大3剤までの治療歴がある患者を含む、過去に治療を受けたことがある患者に臨床的に有意な効果をもたらした(表 2)。迅速で、深く、持続性のある全身および頭蓋内奏効が観察された。解析は、45人の患者が1以上の検出可能なALK 転移性キナーゼドメインを有することを示した。ロルラチニブは、G1202R/del 変異を含むさまざまなALK転移性耐性キナーゼドメイン変異にとって抗腫瘍活性が最も頻繁に出ると示した。奏効はまた、検出可能なALK キナーゼドメイン変異のない患者にも認められた。治療は全般的に忍容性があり、毒性による治療の完全中止率は低い。AEは用量変更および/または支持療法によって管理可能であった。
参考文献
- Peters S et al., Alectinib versus crizotinib in untreated ALK-positive non-small-cell lung cancer.N Engl J Med 2017; 377: 829-838
- Camidge DR et al., Updated efficacy and safety data from the global phase III ALEX study of alectinib (AL) versus crizotinib (CZ) in untreated advanced ALK+ NSCLC.J Clin Oncol 36, 2018 (suppl; abstr 9043)
- Huber RM et al., Brigatinib in crizotinib-refractory ALK+ non-small cell lung cancer: efficacy updates and exploratory analysis of CNS ORR and overall ORR by baseline brain lesion status.J Clin Oncol 36, 2018 (suppl; abstr 9061)
- Bazhenova L et al., Brigatinib in anaplastic lymphoma kinase (ALK)-positive non-small cell lung cancer: long-term efficacy and safety results from a phase 1/2 trial.Ann Oncol 2017; 28 (suppl_5): v460-v496
- Shaw AT et al., Lorlatinib in non-small-cell lung cancer with ALK or ROS1 rearrangement: an international, multicentre, open-label, single-arm first-in-man phase 1 trial.Lancet Oncol 2017; 18: 1590-1599
- Besse B et al., Lorlatinib in patients with previously treated ALK+ advanced non-small cell lung cancer (NSCLC): updates efficacy and safety.J Clin Oncol 36, 2018 (suppl; abstr 9032)
More posts
非浸潤がん検出を可能にする血漿セルフリーDNAの包括的なシーケンシング
非浸潤がん検出を可能にする血漿セルフリーDNAの包括的なシーケンシング 肺がんの早期発見は、未だ医学において解決されていない。低線量コンピュータ断層撮影法(LDCT)は、高
小細胞がんの治療に関する最新ベンチマーク
小細胞がんの治療に関する最新ベンチマーク KEYNOTE-158 進展型小細胞肺がん(ED-SCLC)は一次治療によく反応するが、早期再発も多く起こり、予後は不良である。今
16 ALK陽性疾患:治療の可能性が広がる
16 ALK陽性疾患:治療の可能性が広がる ALEX試験で確認されたアレクチニブのCNSおよび非CNSの有効性 ALK陽性進行非小細胞肺がん患者の標準治療には、第1世代AL
「シーケンシングの課題」
「シーケンシングの課題」 インタビューカナダ、バンクーバー Barbara Melosky、MD、FRCPC、University of British Columbia
第3世代EGFRチロシンキナーゼ阻害薬(TKI)最新データ
第3世代EGFRチロシンキナーゼ阻害薬(TKI)最新データ エルロチニブ+ベバシズマブ EGFR TKI治療は、進行性EGFR遺伝子変異陽性の非小細胞肺がん患者のための標準
免疫チェックポイント遮断:治療成功の成功のカギを握る要素
免疫チェックポイント遮断:治療成功の成功のカギを握る要素 PD-L1発現以外にもさまざまな臨床的要素が、免疫チェックポイント阻害の有効性の予測因子として検討されている。特に