关于跨 3 个世代的 EGFR 靶向 TKI 的新数据
厄洛替尼加贝伐单抗
EGFR TKI 治疗已成为晚期、
EGFR 突变阳性 NSCLC 患者的标准一线治疗策略。药物包括第一代药物吉非替尼和厄洛替尼,第二代药物阿法替尼和达克替尼,以及第三代 TKI 奥希替尼。
EGFR TKI 与其他药物的组合可以优化预后,例如抗血管生成药物额外用药,如贝伐单抗和雷莫芦单抗。
NEJ026 试验是研究一线厄洛替尼联合抗 VEGF 抗体贝伐单抗的一项 III 期研究[1]。在 II 期试验中,随机化 JO25567 试验已表明厄洛替尼加贝伐单抗与厄洛替尼单药治疗相比具有显著的 PFS 获益[2]。为证实这些结果,开展了 NEJ026 研究。非鳞状、IIIB/IV 期或术后复发的具有敏感 EGFR 突变的 NSCLC 日本患者接受贝伐单抗 15mg/kg Q3W 加每日一次厄洛替尼 150mg (QD; n = 112) 或单独接受厄洛替尼(n = 112)治疗。病情进展后,试验组患者接受铂类药物和培美曲塞治疗,然后接受培美曲塞维持治疗,对照组接受铂类药物加培美曲塞和贝伐单抗治疗,然后接受培美曲塞和贝伐单抗维持治疗。允许无症状的中枢神经系统(CNS)转移,并且每组中存在 32.1% 的转移。
独立审查的 PFS 是主要疗效指标。根据预先计划的 PFS 中期分析,联合贝伐单抗导致 PFS 显著延长(16.9 个月对比 13.3 个月;
HR,0.605;p = 0.01573)[1]。该联合使有外显子 19 缺失和外显子 21 L858R 突变的患者获益。独立审查的 ORR 在治疗组中没有显著差异(72.3% 对比 66.1%)。贝伐单抗组更常发生高血压、蛋白尿和出血,但可控。正如研究人员指出的那样,厄洛替尼加贝伐单抗代表了 EGFR 突变 NSCLC 的新标准一线治疗。生物标志物分析和 OS 随访正在进行中。
吉非替尼和化疗的联合使用
在 NEJ002 试验中,与标准化疗相比,吉非替尼治疗有PFS获益(10.8 个月对比 5.4 个月;HR,
0.30;p <0.001)[3],但 OS 没有显著差异。此外,吉非替尼组中只有 70% 的患者接受铂类药物-双联化疗,这是接受 TKI 治疗后的标准治疗方案。因此,预计 EGFR TKI 治疗和化疗的全面使用将有助于改善 OS。
事实上,II 期 NEJ005 研究表明,与顺序方案相比,同时使用吉非替尼和化疗取得了较好的疗效[4]。III 期 NEJ009 试验评估了 4 至 6 个周期的吉非替尼 QD 加卡铂和培美曲塞临床联合用药[5]。诱导期后的维持治疗为每日吉非替尼加培美曲塞 Q3W 直至发生疾病进展。另一方面,对照组患者接受吉非替尼 QD 直至病情恶化;进展后,建议采用以铂类药物为基础的二线方案。
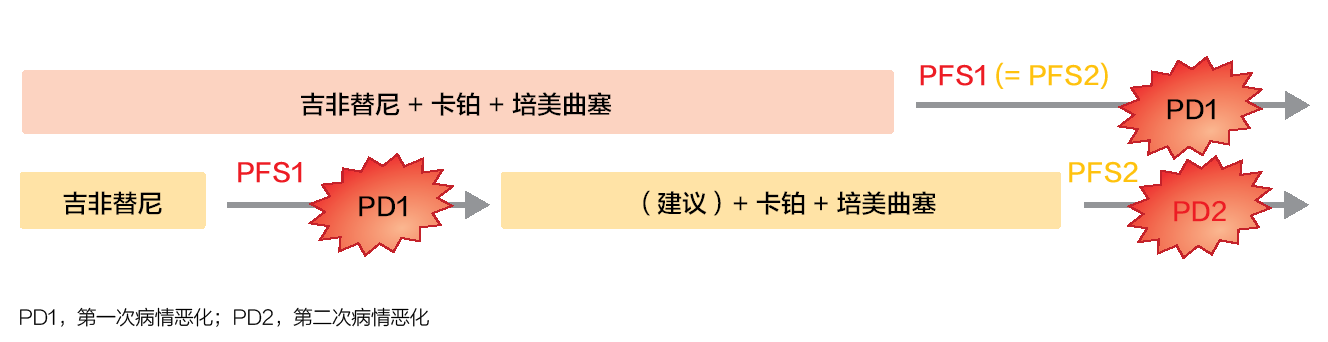
评估了多个主要疗效指标,包括 PFS、PFS2(即对照组中第二次疾病进展[PD2]和试验组中的第一次进展[PD1]时的 PFS 比较;图)和 OS。在日本,有 345 名非鳞状、初治 IIIB/IV 期或复发性 NSCLC 患者在 47 所机构进行登记。
图:PFS 结果如 NEJ009 研究中的定义
第一次恶化的时间很重要
正如预期的那样,对于 PFS1(20.9
个月对比 11.2个月;HR,0.494;
p <0.001)和 ORR(84.0% 对比 67.4%),联合治疗优势明显。这些影响很可能是由于试验组中相对较长的吉非替尼治疗暴露(730 天对比 462 天)。在 PD1 时,患者的临床状态(即,ECOG PS、转移器官的数量、脑转移)在试验组中是相当的。但是,PD2 的情况并非如此;在这里,按顺序接受治疗的患者情况要差得多。PFS2 分析得出两种方案之间没有差异的结论(20.9 个月对比 20.7 个月;HR,0.966;p = 0.774)。
OS 分析表明组合方案的显著优势(52.2 个月对比 38.8 个月;
HR,0.695;p = 0.013)。PD1 的存活率没有差异(19.3 个月对比 23.0 个月;HR,1.037;p = 0.812),尽管单独使用吉非替尼的大多数患者在第一次进展后接受了铂类药物治疗。这表明本研究中的 OS 与 PFS1 密切相关,而非与 PFS2 密切相关。作者得出结论,延长至第一次恶化的时间对于有 EGFR 突变 NSCLC 的患者至关重要,并且 PFS 是 OS 的良好替代标志。
血液学 AE 在联用组中更常见。然而,在两个治疗组中,只有少数患者由于毒性而停止治疗。总体而言,在初治的晚期 EGFR 突变 NSCLC 中加入卡铂和培美曲塞显著改善了 PFS 和 OS,并具有可接受的毒性。因此,在这种情况下,联合治疗方案可能是有效的一线选项。
ARCHER 1050 的 OS 结果
在 III 期、随机、开放性 ARCHER 1050 研究中研究了第二代不可逆 EGFR TKI 达克替尼。Wu 等人报告使用达克替尼显著改善 PFS,对比使用吉非替尼作为 EGFR 突变、晚期 NSCLC 患者的一线治疗方案取得的结果(14.7 个月对比 9.2 个月;HR,0.59;p <0.0001)[6]。共有 452 名患者接受达克替尼 45 mg QD 或吉非替尼 250 mg QD。该试验不允许预先存在的 CNS 转移,因为在研究纳入时,达克替尼在脑损伤患者中的功效是未知的。两组中的群体中有 70% 至 80% 是亚洲人。大约 60% 的人年龄小于 65 岁。
在 ASCO 2018 大会上介绍的 ARCHER 1050 的预先设定最终 OS 分析表明,这是第一项比较两个一线 EGFR TKI 以证明 OS 改善的随机 III 期试验[7]。达克替尼和吉非替尼的中位 OS 结果分别为 34.1 个月对比 26.8 个月(HR,0.76;p = 0.0438)。在 30 个月时,存活患者比例为 56.2% 对 比46.3%。亚组分析得出在外显子 19 缺失(HR,0.88;p = 0.4862)或外显子 21 L858R 突变(HR,
0.707;p = 0.0805)的患者接受的两种治疗之间没有 OS 差异,尽管该研究无法记录这些亚组的生存差异。同样,亚洲患者的 OS 分析未表明存在显著的治疗获益(HR,0.812;p = 0.1879)。接受达克替尼治疗并继续接受第三代 EGFR TKI 治疗的患者的中位 OS(占群体的 9.7%)为 36.7 个月。作为后续治疗的其他 EGFR TKI 的 OS为 34.7 个月。
达克替尼的 EGFR 抑制活性增强导了致典型的 AE;≥3 级的痤疮性皮炎,发生率为 13.7%;≥3 级的腹泻。发生率为 8.8%;≥3 级的甲沟炎,发生率为 7.5%。另一方面,吉非替尼仅为 ≥3 级的肝酶升高略有提高。因 AE 经常在试验组中进行必要的剂量调整
(使用吉非替尼时为 66.5% 对比 8.0%)。作者得出结论,达克替尼应作为 EGFR 突变晚期 NSCLC 患者的一线治疗新选择。
正确解读 ARCHER 1050 数据
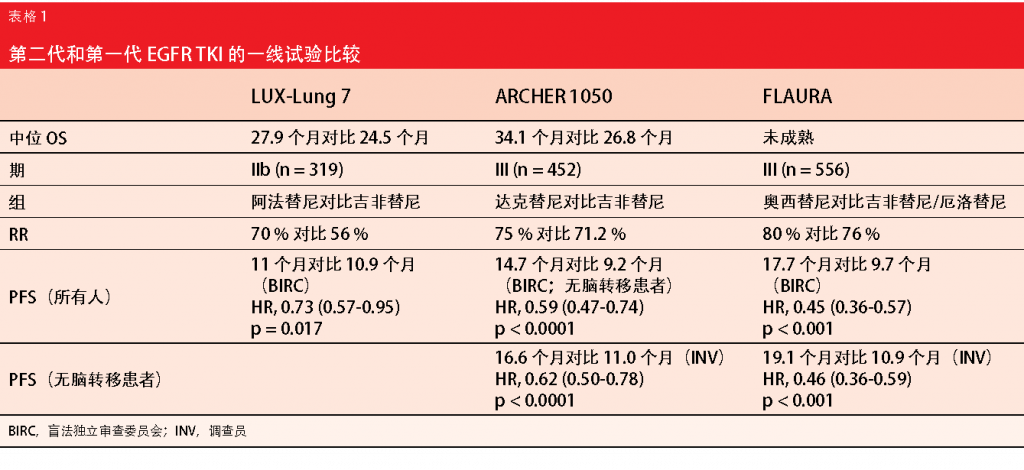
正如新加坡国立癌症中心的 Daniel Tan 博士在讨论 ARCHER 1050 和 NEJ009 数据时指出的那样,尽管问题仍然存在,这是两项 III 期试验,最终证明了相比标准 EGFR TKI 的 OS 益处[8]。所有之前的 EGFR TKI 被批准用于一线治疗有 PFS 获益,但在 OS 中未发现显著差异,这可能是由于交叉引起的。比较 ARCHER 1050 与调查第二代和第三代 EGFR TKI 的其他关键一线试验时,Tan 博士指出,LUX-Lung 7 研究(对照吉非替尼测试阿法替尼对[9])的样本量 (n = 319) 小于 ARCHER 1050 (n = 452;表 1)。此外,这是一项 IIb 期研究,可能会限制其检测 OS 差异的能力。虽然脑转移患者包括在 LUX-Lung 7 中,但 ARCHER 1050 并非如此。达克替尼的长期耐受性是一个潜在问题,因此需要确定最佳的药理学活性剂量。另一个未解决的问题是第二代和第三代 TKI 的定序。
此外,在何种情况下使用奥希替尼仍是一个问题。来自 FLAURA 试验的 OS 数据尚未成熟,并且阻力机制仍未完全特征化,具有不确定的成药性。Tan 博士强调,EGFR 突变型肺癌是一种临床和基因组异质性疾病。初始前期治疗可以增强其自然史;因此,为使前期治疗合理化,确定疾病进展的个体风险越来越重要。根据 Tan 博士的说法,有必要辩证地评估这些潜在治疗标准的风险-收益比,并根据个体患者偏好进行调整。
关于阿法替尼的实际循证
阿法替尼的耐受性指导剂量调整降低了 AE 的发生率和严重程度,并且未影响 LUX-Lung 研究中的疗效。Halmos 等人报告阿法替尼剂量改变对该治疗在现实环境中的疗效和安全性的影响[10]。来自 13 个国家的 228 名接受一线阿法替尼治疗的患者被纳入这项非介入性、观察性研究。
与 LUX Lung 试验一样,阿法替尼剂量调整可降低 AE 的频率和强度而不影响疗效。无论改变剂量或减少起始剂量,治疗时间和恶化时间都相似。起始剂量 ≥ 40 mg 的患者中有 67% 减少了剂量,其中 86% 的患者在前 6个月内减少剂量。12% 的患者剂量有所增加。AE 是更改剂量的主要原因。女性、老年患者、东亚患者和体重较轻者的剂量调整更为频繁。分析结果表明没有新的安全信号。这些结果突出了基于个体患者特征和 AE 来定制阿法替尼剂量,以优化结果的益处。
在实际操作中,使用阿法替尼获得的临床结果是日本分析 128 名患者的重点,其中 76 名患者接受一线阿法替尼,而 52 名患者在再次激发环境中接受治疗[11]。使用阿法替尼产生了与先前试验相当甚至更好的结果。在一线环境中,PFS 和 OS 分别为 17.8 个月和 39.5 个月。尽管 AE 导致 58 名患者 (76.3 %) 需要减少剂量,但这并未影响 OS 结果(减少组为 39.5 个月,对比未减少组尚未达到月数;p = 0.37)。此外,比起并非这种情况的患者,剂量减少的患者甚至经历了更长的 PFS(18.0 对比 7.9 个月;p = 0.016)。ORR 为 64%。在再次激发环境中,分析得出 24% ORR 的结果。
阿法替尼用于罕见 EGFR 突变
一项回顾性、多中心研究评估了阿法替尼在西班牙临床实践中治疗有罕见 EGFR 突变的肺腺癌患者的疗效[12]。对 2012 年至 2017 年期间在 23 家西班牙机构接受阿法替尼治疗的 67 例 NSCLC 患者的医疗记录进行了审查。80%
的患者接受阿法替尼作为一
线治疗。作为复杂突变(A 组;n = 20),外显子 20 插入(B 组;n = 23)或单突变(C 组;n = 24)来分析罕见 EGFR 突变。
三组均未发现临床特征差异。18% 的患者以较低剂量开始使用阿法替尼,24% 的患者需要减少剂量。对阿瓦替尼的反应,A 组和 C 组(分别为 70% 和 54%)明显高于 B 组(13%;成对比较分别为 p < 0.001 和
p = 0.013)。整个同期群的中位 OS 为 19.9 个月,A 组对比 C 组的 HR 分别为 0.27(p = 0.009)和 0.40(p = 0.037)。正如作者在其结论中所述,在临床实践中,阿瓦替尼在具有罕见的 EGFR 突变(特别是在复杂和单突变)的 NSCLC 中具有活性。但是,需要为外显子 20 插入的患者制定进一步策略。
使用新辅助疗法:ASCENT 试验
II期 ASCENT 研究,评估了新辅助疗法中的阿法替尼治疗 III 期 EGFR 突变 NSCLC 患者(其疾病负荷可承受放化疗)[13]。用阿法替尼 40mg QD 治疗 2 个月后,患者接受放化疗,接着接受切除手术或 2 年的阿法替尼 40mg QD 辅助治疗,前提是使用新辅助 TKI 时未发生疾病进展。手术后,可选择辅助化疗,然后接受阿法替尼辅助治疗。
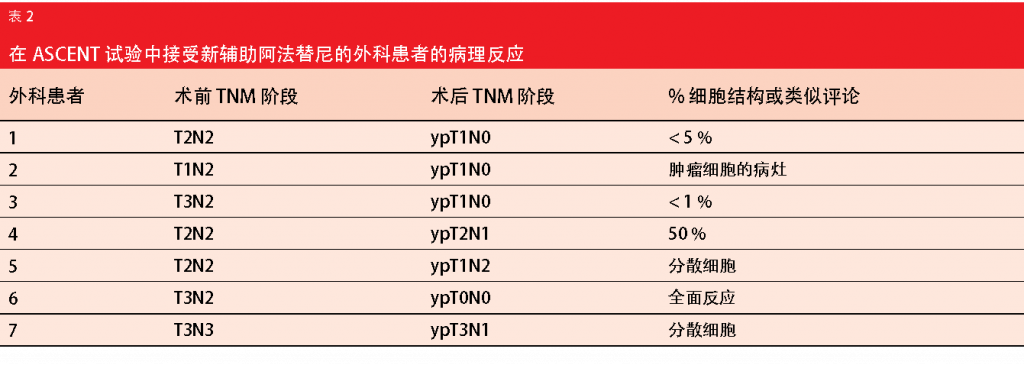
虽然在该分析中仅有 13 名患者,但分析结果显示有利的新辅助疗法反应率为 75%。使用新辅助阿法替尼不会妨碍放化疗(无论有没有接受手术)。接受手术的 7 名患者当中,有 6 名出现临床上显著的病理反应(即,缺乏细胞,<5% 的细胞性;表 2)。中位 PFS 为 34.8 个月,其中 7 例患者在分析时无复发。该结果优于 PACIFIC 研究[14]的免疫治疗组中观察到的 16.8 个月的 PFS 结果,并支持基因型靶向方法。PACIFIC 在局部晚期、不可切除的 III 期 NSCLC 中测试了 PD-L1 抑制剂 durvalumab 对比安慰剂的顺序治疗。研究人员指出,在 2 个月的新辅助治疗中使用阿法替尼的可行性可能超过使用辅助 TKI。ASCENT 试验入组正在继续。
TMB 对于抗 EGFR 治疗的意义
肿瘤突变负荷 (TMB) 可能具有多种生物学意义,这取决于具体的治疗和疾病背景。对于免疫疗法,已经描述了 TMB 与改善疗效之间的关系。Offin 等人假设 TMB 可能与靶向治疗环境中的结果有明显(和反向)关系,其中 TMB 可能是存在抗性路径的替代物[15]。研究人员确定接受第一代和第二代 EGFR TKI 治疗的 153 例 EGFR 突变(外显子 19 缺失和外显子 21 L858R 突变)肺癌患者,并通过对预治疗组织执行肿瘤分析多重组 MSK-IMPACTTM 进行了二代测序。在单变量和多变量分析中,根据 TMB 评估了 OS 和初始 EGFR TKI 治疗的终止治疗时间 (TTD)。
结果表明 EGFR 突变肺癌具有广泛的分子异质性,即使在此特定的致癌基因定义疾病中也具有广泛的 TMB。正如研究人员推测的那样,TMB 与 EGFR TKI 治疗的疗效呈负相关。根据多变量分析(分别为 p = 0.025 和 0.009),
OS 和 TTD 在显示高 TMB 的组中最短,HR 分别为 0.49 和 0.57。这种关系与通过免疫疗法形成的关系相反,后者突出了 TMB 的多变性和背景特异性影响。
对奥希替尼的抗性:有什么新发现?
与第一代或第二代 EGFR TKI 治疗进展后有 T790M 阳性 NSCLC 的患者接受的铂类-培美曲塞化疗相比,第三代 EGFR TKI 奥希替尼在 III 期 AURA3 研究中表现出显著的临床活性[16]。此外,与一线厄洛替尼或吉非替尼相比,奥希替尼在 III 期 FLAURA 试验中有显著的 PFS 益处[17]。
尽管奥希替尼在治疗 NSCLC 中的作用越来越大,但与该药物的耐药机制有关的数据有限。然而,仍需要全面了解这些机制,以制定克服奥希替尼耐药性的
策略。因此,Le 等人基于 MD Anderson Lung Cancer Moon Shot GEMINI 数据库和 Moffitt 电子健康记录,临床基因组行动委员会数据库和焦磷酸定序数据库,对有 EGFR T790M 突变的 NSCLC 患者进行分析,分离了那些接受奥希替尼治疗的患者[18]。共有 118 名患者符合研究标准。几乎所有人 (95 %) 都曾接受过 EGFR TKI 治疗,主要是厄洛替尼治疗。
基因组分析表明,抗性机制各有不同,T790M 保存和 T790M 丢失各占大约一半的病例。在 T790M 保存的样本中,发现了 C797S/L792H 突变 (58 %),以及 MET 扩增。这意味着 EGFR 的三级突变是该组的常见机制。在 T790M 丢失的样本中,抗性机制主要是 EGFR 非依赖性和非癌基因驱动介导的(即 PIK3CA 突变,MET 扩增,SCLC 转变)。细胞周期基因改变表明与较差的临床结果有关。
Zhang 等人在分析与 110 例有激活 EGFR 突变且临床上具有奥西替尼耐药性的患者的突变谱有关的差异时,观察到更可能在缺失组 19 中而非有 L8585R 突变的患者中识别出导致奥西米替尼耐药性的必要突变(62.5% 对比 39.1%;p = 0.015)[19]。
对奥西替尼反应的预测
之前在 AURA 计划中进行的纵向分析表明,接受奥西替尼的 T790M 阳性晚期 NSCLC 患者
的血浆 EGFR 突变的早期清除
是改善 PFS 的预后标志物[20]。
Shepherd 等人研究了开始使用奥西替尼治疗后的 3 周和 6 周,来自 AURA3 的患者的血浆 EGFR 突变是否与临床结果相关[21]。
结果显示,接受奥西替尼治疗的患者,在其基线血浆样本中具有可检测到的 EGFR 突变,这是肿瘤脱落的特征,在 PFS(8.3 对比 14.0 个月)和 ORR(68% 对比 75%)方面,其预后比无肿瘤脱落的患者更差。研究人员得出结论,可检测到的肿瘤脱落可能反映了疾病负荷的增加,并可能成为较差预后的预后生物标志物。
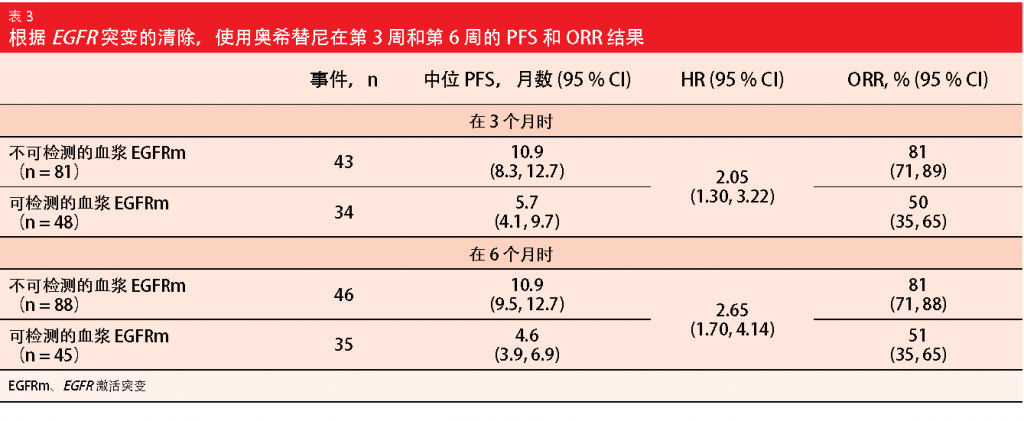
此外,血浆 EGFR 突变的早期动态变化可能会预测接受 T790M 阳性 NSCLC 治疗的患者的 PFS,因为在第 3 周和第 6 周持续存在 EGFR 突变的循环肿瘤 DNA
(ctDNA) 与较差的 PFS 和 ORR 结果相关(表 3)。因此,最早可以在开始使用奥西替尼的 3 周后识别可能经历次佳临床预后的 T790M 阳性 NSCLC 患者。监测 EGFR 突变的 ctDNA 可修改治疗方案以达到优化预后的目的。
预测对奥西替尼反应的另一个潜在的早期标志物是 18F-氟脱氧葡萄糖(FDG)PET。Yoon 等
人对 25 名患者进行了一项前瞻性、开放式、单中心前导性研究,该研究表明第一代 EGFR TKI 治疗的疾病进展[22]。ORR 为 76%,代谢反应(定义为 ≥ 20 %
ΔSUVmax疾病)与中位 PFS 和 ORR显著相关。即使在没有 T790M 突变的患者中,奥西替尼也显示出抗肿瘤活性。
雷莫芦单抗作为组合伴侣
持续进行的 I 期 JVDL 试验在一线 EGFR TKI 治疗进展后评估了奥西替尼与 EGFR 突变、T790M 阳性 NSCLC 中的单克隆抗 VEGFR-2 抗体雷莫芦单抗的组合。在对 25 名患者进行分析后,Planchard 等人认为该组合的安全性与作为单药治疗的每种药物的安全性一致,并且无额外毒性[23]。高血压、腹泻、口腔炎、皮疹和血小板减少症是最常见的 AE。只有 4% 的患者因 AE 导致停药。
此外,结果表明存在刺激性抗肿瘤活性。完全或部分反应达到 76%,疾病控制达到 92%。在分析时尚未达到中位 DOR,这也适用于中位 PFS。在 12 个月时,57.5% 的患者存活且无恶化。
新面孔:纳扎替尼
纳扎替尼是试验性第三代、不可逆 EGFR TKI 选择性药剂,用于激活 EGFR 突变和 T790M 突变,同时保留野生型 EGFR。根据多中心、开放性 I/II 期首次人体研究的初步 II 期结果,纳扎替尼在 EGFR 突变、IIIB/IV 期 NSCLC 初治患者中表现出可接受的安全性和较好的疗效[24]。40% 的患者在筛查时有脑转移。
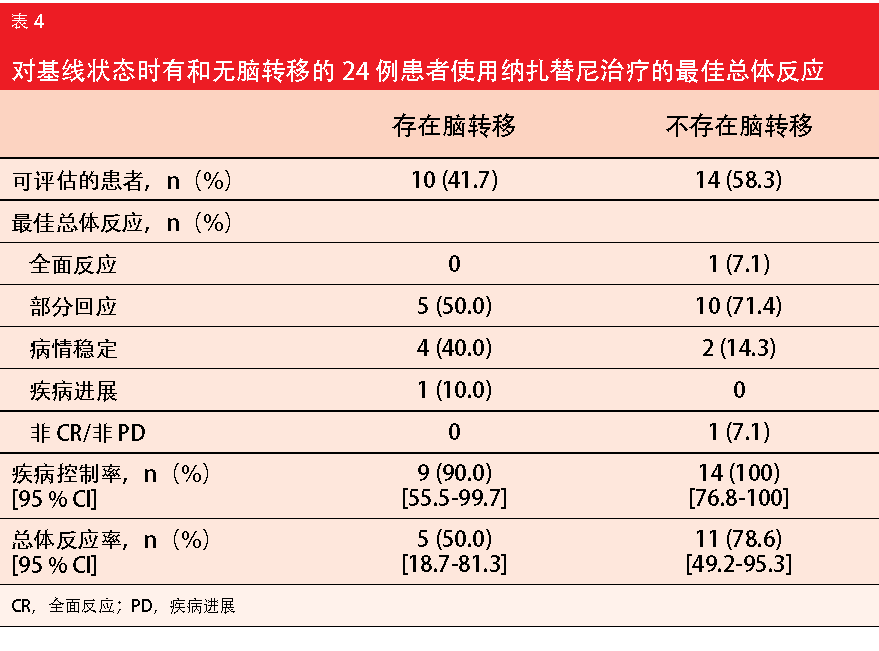
纳扎替尼耐受性良好,大多数 AE 为 1 级或 2 级。总体而言,安全性在所有典型毒性方面都显得有利,例如腹泻、痤疮样皮疹、皮肤干燥、口腔炎和甲沟炎。斑丘疹是最常见的 AE,但被证明是可控的。尽管在基线状态下脑损伤患者的比例很高,但根据盲法独立审查委员会的说法,新 TKI 引起的 ORR 为 66.7%。疾病控制的比例为 95.8%。大多数患者的目标病灶尺寸减少。纳扎替尼对有和无脑转移的患者均有效 (表 4)。在数据截止时,PFS 和 DOR 数据仍然不成熟。预计在治疗初期调查纳扎替尼的 III 期研究将于 2018 年 7 月开始。
参考
- Furuya N et al., Phase III study comparing bevacizumab plus erlotinib to erlotinib in patients with untreated NSCLC harboring activating EGFR mutations: NEJ026. J Clin Oncol 36, 2018 (suppl; abstr 9006)
- Seto T et al., Erlotinib alone or with bevacizumab as first-line therapy in patients with advanced non-squamous non-small-cell lung cancer harbouring EGFR mutations (JO25567): an open-label, randomised, multicentre, phase 2 study. Lancet Oncol 2014; 15(11): 1236-1244
- Maemondo M et al., Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med 2010; 362(25): 2380-2388
- Sugawara S et al., Randomized phase II study of concurrent versus sequential alternating gefitinib and chemotherapy in previously untreated non-small cell lung cancer with sensitive EGFR mutations: NEJ005/TCOG0902. Ann Oncol 2015; 26(5): 888-894
- Nakamura A et al., Phase III study comparing gefitinib monotherapy to combination therapy with gefitinib, carboplatin, and pemetrexed for untreated patients with advanced non-small cell lung cancer with EGFR mutations (NEJ009). J Clin Oncol 36, 2018 (suppl; abstr 9005)
- Wu YL et al., Dacomitinib versus gefitinib as first-line treatment for patients with EGFR-mutation-positive non-small-cell lung cancer (ARCHER 1050): a randomised, open-label, phase 3 trial. Lancet Oncol 2017; 18(11): 1454-1466
- Mok TS et al., Improvement in overall survival in a randomized study comparing dacomitinib with gefitinib in patients with advanced non-small cell lung cancer harboring EGFR-activating mutations. J Clin Oncol 36, 2018 (suppl; abstr 9004)
- Tan DSW, Shifting Sands: improving on first-generation EGFR TKIs. ASCO 2018 Congress, Discussion of abstracts 9004 and 9005
- Park K et al., Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomised controlled trial. Lancet Oncol 2016; 17(5): 577-589
- Halmos B et al., Real-world dose adjustment study of first-line afatinib in pts with EGFR mutation-positive (EGFRm+) advanced NSCLC. J Clin Oncol 36, 2018 (suppl; abstr e21060)
- Tanaka H et al., Real world study of afatinib in first-line or re-challenge setting for patients with EGFR mutant non-small cell lung cancer. J Clin Oncol 36, 2018 (suppl; abstr e211713)
- Domine M et al., Clinical activity of afatinib in a cohort of patients with lung adenocarcinoma harbouring uncommon EGFR mutations: A Spanish retrospective multicentre study. J Clin Oncol 36, 2018 (suppl; abstr e21028)
- Sequist LV et al., The ASCENT trial: a phase II study of neoadjuvant afatinib, chemoradiation and surgery for stage III EGFR mutation-positive NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 8544)
- Paz-Ares L et al., PACIFIC: a double-blind, placebo-controlled Phase III study of durvalumab after chemoradiation therapy (CRT) in patients with stage III, locally advanced, unresectable NSCLC, ESMO 2017, abstract LBA1_PR
- Offin M et al., Tumor mutation burden and efficacy of EGFR-tyrosine kinase inhibitors in patients with EGFR-mutant lung cancers. J Clin Oncol 36, 2018 (suppl; abstr 9042)
- Mok TS et al., Osimertinib or platinum-pemetrexed in EGFR T790M-positive lung cancer. N Engl J Med 2017; 376: 629-640
- Soria JC et al., Osimertinib in untreated EGFR-mutated advanced non-small-cell lung cancer. N Engl J Med 2018; 378(2):113-125
- Le X et al., Landscape of EGFR-dependent and -independent resistance mechanisms to osimertinib in EGFR-mutant NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 9087)
- Zhang Y et al., Landscape of osimertinib resistant mutations between the two common subtypes of EGFR 19del or L858R in NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 12108)
- Thress KS et al., Complete clearance of plasma EGFR mutations as a predictor of outcome on osimertinib in the AURA trial. J Clin Oncol 35, 2017 (suppl; abstr 9018)
- Shepherd FA et al., Early clearance of plasma EGFR mutations as a predictor of response to osimertinib in the AURA3 trial. J Clin Oncol 36, 2018 (suppl; abstr 9027)
- Yoon S et al., The role of FDG-PET during osimertinib treatment to predict the responsiveness of tumor early in patients with stage IV non-small cell lung cancer: A pilot study. J Clin Oncol 36, 2018 (suppl; abstr e21150)
- Planchard D et al., Efficacy and safety results of ramucirumab in combination with osimertinib in advanced T790M-positive EGFR-mutant NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 9053)
- Kim D-W et al., Preliminary phase II results of a multicenter, open-label study of nazartinib (EGF816) in adult patients with treatment-naïve, EGFR-mutant NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 9094)
More posts
PD-(L)1 单独和联合抑制:近期对免疫疗法的见解
PD-(L)1 单独和联合抑制:近期对免疫疗法的见解 一线,单药派姆单抗:KEYNOTE-042 转移性非小细胞肺癌 (NSCLC) 患者与化疗相比,使用抗-PD-1 单克
前言
前言 作者版权所有 Bruce E. Johnson, MD 美国临床肿瘤学学会主席 首席临床研究官, 达纳法伯癌症研究所, 美国马萨诸塞州波士顿 ASCO 转化研究教授