化学療法:新しいアプローチ、新しいセッティング
SCAT: BRCA1を用いた補助化学療法のカスタマイズ
最新ガイドラインでは、完全切除したリンパ節転移(ステージII~IIIA)NSCLC患者に対し術後プラチナベース化学療法が推奨されている[1]。しかし、生存期間の転帰は依然として限定されており、治療遵守は他の腫瘍での補助療法よりも低い。さまざまな化学療法レジメンの間での直接的な比較は行われていない。
最適な化学療法薬とスケジュールの選択を個別化するために、DNA修復に関与した遺伝子発現の分析を使用することができた[2]。ここで、BRCA1遺伝子は相同的組み換え経路で役割を果たすため重要であり、シスプラチンや抗微小管薬に対する反応の差次的調整因子として機能する。この因子は予後と予測に関連し、、低濃度は低リスクとシスプラチン感受性を意味し、高濃度は高リスクとシスプラチン抵抗性を示すことから、、このような患者にタキサンベースの化学療法に対して感受性であることが示唆される。
無作為化SCAT臨床試験でBRCA1を指標にした治療アプローチを試験した。この試験には切除を受けたNSCLC R0 pN1/ pN2患者を含めた[3]。対照治療群はドセタキセルとシスプラチンの併用治療を受け、試験治療群に無作為に割り当てられた患者はBRCA1発現レベルに応じた治療を受けた。BRCA1発現の少ない患者はゲムシタビン/シスプラチンの治療を受け、発現が中程度の患者はシスプラチン/ドセタキセルを、発現の多い患者はドセタキセル単剤の治療を受けた。21日ごとに4サイクルの投与を受けた。化学療法は術後8週間以内に開始された。治験実施計画書に基づいた治療集団には対照治療群の患者102例と試験治療群の患者354例を含めた。OSが主要評価項目であった。
高発現患者については単剤ドセタキセルで十分であるように思われる
低レベルのBRCA1発現は女性であること、喫煙経験なし、 腺癌組織構造、および縦隔リンパ節転移と有意に関連していた。一方で高レベルは男性であること、扁平上皮組織構造、および現在または過去の喫煙と相関した。
主要解析によると、BRCA1レベルに応じた補助化学療法のカスタマイズによって、試験治療群と対照治療群の間に有意なOSの差は生じなかった(82.4ヶ月対69.3ヶ月;HR,0.946)。5年生存率は両治療群で50%を超えた(それぞれ、56%、54%)。試験群において、OS中央値の著しい変動はなく、74~80.5ヶ月の範囲であった。一方、対照コホートで治療を受けた患者は高いBRCA1レベルを発現した時に最も成績が悪く(OS、40.1ヶ月)、中程度と高いレベルの患者の場合は転帰が著しく改善された(それぞれ、未到達、82.4ヶ月)。多変量Cox分析では、対照群においてBRCA1レベルが予後因子であることが分かった。
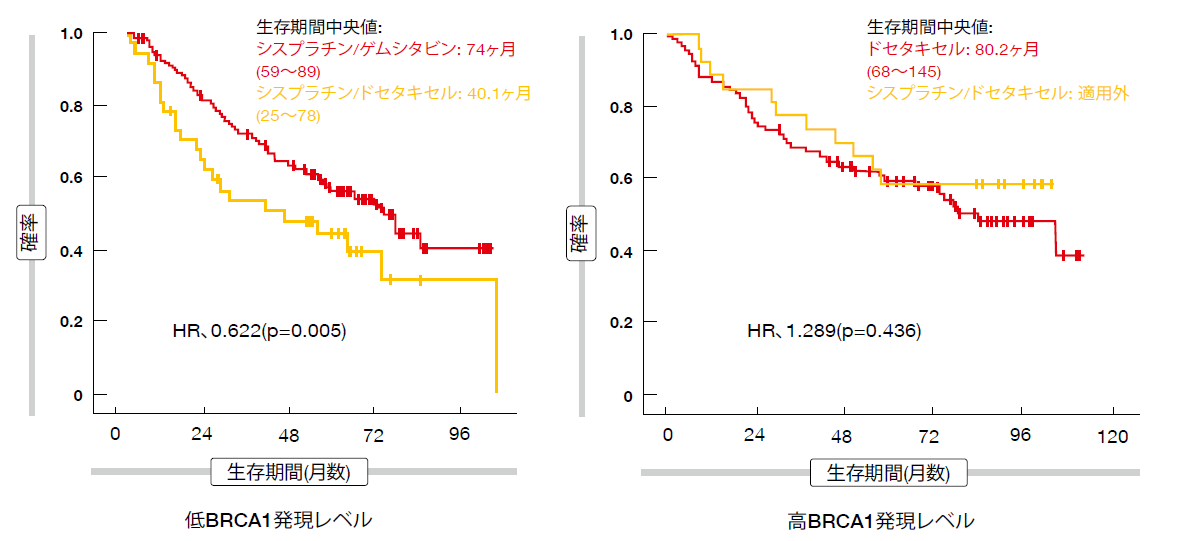
BRCA1サブグループに応じて2つの治療群について分析した結果、低い発現レベルの患者はシスプラチン/ドセタキセルと比較してシスプラチン/ゲムシタビンが有益であることが示された (74ヶ月対40.1ヶ月;HR、0.622;図)。しかし、BRCA1高発現群の場合、試験療法と対照療法の間に差はなかった。すなわち、ドセタキセル単剤によって達成された生存期間は、ドセタキセル/シスプラチンコホートでのOS転帰と類似していた。計画された治療に関連する遵守状況は、試験治療群でシスプラチンを用いない患者で有意に改善された。シスプラチンを用いずに治療を受けた患者は非癌関連死亡率が低い傾向を示した。全般的に、高BRCA1発現レベルの患者を対象として、プラチナ成分を用いないタイキサン補助療法 について評価が行われるかもしれないと著者は結論付けた。ここで、短期と長期のプラチナ毒性の回避が可能である必要がある。
図:SCAT試験: 複数の治療群におけるBRCA1サブグループ別の無再発生存率
ナブパクリタキセルの意外なほど良好な2次治療活性
進行NSCLCの2次治療条件において、効果的で許容し得る化学療法の選択肢が求められる。無作為化非盲検多施設第II相ABOUND.2L+臨床試験では、1回のプラチナベース化学療法を既に受けたが、事前のタキサン治療は受けていない進行非扁平上皮NSCLC患者161例を対象として、単剤ナブパクリタキセル治療をナブパクリタキセルとアザシチジン(CC-486)の併用治療と比較した[4]。患者80例は100 mg/m2のナブパクリタキセル単剤療法を21日サイクルの1日目と8日目に受け、他の80例はナブパクリタキセル(21日サイクルの8日目と15日目)およびCC-486(21日サイクルの1~14日目に200 mgを経口投与)による治療を受けた。
ナブパクリタキセルとCC-486の併用がPFSについて優位性を示さなかったため、試験は主要評価項目を達成しなかった。対照群の患者の成績が意外にも良好で、試験治療群の患者よりもさらに優れたPFSを示した(4.2ヶ月対3.2ヶ月;HR、1.3)。これはOS(13.6ヶ月対8.1ヶ月;HR、1.5)とORR(15.0%対13.6%)にも当てはまった。CR、PRおよびSDの組み合わせとして定義される疾病制御はが生じた割合は67.5%と65.4%であった。QOL分析によると、ナブパクリタキセルは呼吸器系の転帰、症状負荷インデックス、およびQOLスコアを改善した。両方の治療法が良好な忍容性を示した。グレード3以上の有害事象(AE)は両方の治療群で1桁の範囲にとどまった。
患者全員の募集が終わった後に、治験責任医師はCC-486治療を中止するよう勧められた。CC-486との併用投与による付加的な有益性はもたらさなれなかったが、単剤ナブパクリタキセルは進行非扁平上皮NSCLCの治療における2次治療薬として有望であった。継続中の臨床試験からの結果が報告されれば、この条件でのナブパクリタキセルの役割を知る上でさらなる洞察が得られることになる。
免疫療法と化学療法の併用
ナブパクリタキセルへの抗PD-L1抗体デュルバルマブの追加を調査する目的で、2016年3月に第3試験群がABOUND.2L+臨床試験に導入された[5]。進行非扁平上皮または扁平上皮NSCLC患者79例が21日サイクルの1日目と8日目にナブパクリタキセル100mg/m2を投与し21日サイクルの15日目にデュルバルマブ1,125mgを投与する併用治療を受けた。約1/3が扁平上皮組織構造を示した。ABOUND.2L+の他の2つの治療群と同様に、1回の事前のプラチナベースの化学療法が許されたが、事前のタキサン治療は認められなかった。ただし、患者は試験組み入れ前に免疫チェックポイント阻害剤治療を受けることができた。これは集団の11.4%に相当する。主要評価項目はPFSであった。
パクリタキセルとデュルバルマブによる併用療法では、PFS中央値は4.5ヵ月であった。OS中央値にはまだ到達していなかった。やや予測外であるが、、登録前に免疫チェックポイント阻害剤治療を受けた患者は、チェックポイント阻害剤治療を受けていない群と比較して優れたPFSを示したが(6.9ヶ月対4.4ヶ月)、事前治療を受けた患者の数が少ないためにこれらの結果の解釈には注意が必要である。また、扁平上皮組織構造を持つ患者は非扁平上皮組織構造を持つ患者よりも長いPFSを達成した(5.9ヶ月対4.2ヶ月)。集団全体でORRは26.6%であった(表)。この値は2次治療条件で他の治療によって達成される転帰よりも良好である。さらに、サブグループ分析によって、非扁平上皮組織構造を持つ患者よりも扁平上皮組織構造を持つNSCLC患者において比較的優れた所見が得られた(34.8%対23.6%)。全体として、臨床試験では70.9%という優れたDCRが認められた。
毒性は予測可能であり、最も多く見られたAEは末梢感覚神経障害、呼吸困難、および貧血であった。発熱性好中球減少症は生じなかった。ナブパクリタキセルとデュルバルマブの組み合わせは、進行NSCLC患者の2次治療または3次治療において抗腫瘍活性を示し、毒性は管理可能であると著者は結論付けた。これらのデータは、NSCLC治療における免疫チェックポイント阻害剤に対する化学療法パートナーとしてのナブパクリタキセルの使用をさらに支持するものである。
扁平上皮細胞癌でのナブパクリタキセル
扁平上皮細胞肺癌の治療選択肢は依然として限られているため、Paikらが発表した第II相臨床試験では、未治療ステージIV扁平上皮NSCLC患者を対象としてナブパクリタキセルとゲムシタビンの併用の評価が現在行われている。WCLCで発表された所見から、ナブパクリタキセルとゲムシタビンの併用は有望な有効性を有し、プラチナベースの治療法と比較して良好な忍容性を示すことが分かった。21%の患者が2種類の投与レジメンのうちの1つに割り当てられ、治療を受けた。
ORRが試験の主要評価項目と定義されている。分析時に、ORRは58%、奏効期間は7.5ヶ月であった。PFSは6.1か月、OSは13.9か月であった。これと比較すると、ほぼ20年にわたり標準一次治療薬であったプラチナベース化学療法は、ORR 30%~40%、PFS中央値
4~5.7ヶ月、OS中央値9~11.5ヶ月であることが知られている[7-9]。主なAEは倦怠感、浮腫、末梢神経障害、および吐き気であり、その大部分がグレード1であった。重篤なAEには白血球減少症、下痢、および肺感染症が含まれた。PD-L1陰性患者に重点を置いて臨床試験への新規登録は継続中である。
ネダプラチンを含む補助二重化学療法
ネダプラチンは日本で開発されたシスプラチン誘導体である。プロスペクティブ多施設共同第II相試験では、肺葉切除およびリンパ節郭清を含む根治治療を受けたNSCLCステージIB~IIIA患者34例の補助治療として、ドセタキセル・ネダプラチン併用化学療法の実行可能性を評価した[10]。4サイクルの1日目に、それぞれ60 mg/m²と80 mg/m²でドセタキセルとネダプラチンが投与された。実行可能性(すなわち、4サイクルを完了した患者の割合)が主要評価項目とされ、毒性と無再発生存期間(RFS)が副次的評価項目とされた。
ドセタキセルとネダプラチンの併用による補助化学療法は完全切除したNSCLC患者において実行可能で、忍容性を示すことが結果から示された。
全体として、76.5%の患者が4サイクルのすべてを完了した。分析時にRFS
中央値に到達していなかった。5年RFSは65.8%であった。血液学的および
非血液学的AEの発生率は、ANITA試験で評価されたシスプラチンとビノ
レルビンの併用化学療法よりも低かった[11]。
参考文献
- Postmus PE et al., Early and locally advanced non-small-cell lung cancer (NSCLC): ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up.Ann Oncol 2017; 28 (Suppl 4): iv1-iv21
- Karachaliou N et al., Using genetics to predict patient response to platinum-based chemotherapy, Exp Rev Prec Med Drug Develop 2017; 2(1): 21-32
- Massuti B et al., SCAT phase 3 trial: adjuvant CT based on BRCA1 levels in NSCLC N+ resected patients.Final survival results.A Spanish Lung Cancer Group trial.WCLC 2017, PL 02.04
- Morgensztern D et al., nab-Paclitaxel ± CC-486 as second-line treatment of advanced NSCLC: results from the ABOUND.2L+ study.WCLC 2017, MA 03.01
- Govindan R et al., nab-paclitaxel + durvalumab as second- or third-line treatment ad advanced NSCLC: results from ABOUND.2L+.WCLC 2017, MA 03.01
- Paik PK et al., A phase II trial of albumin-bound paclitaxel and gemcitabine in patients with untreated stage IV squamous cell lung cancers.WCLC 2017, P1.03-028
- Scagliotti GV et al., Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced-stage non-small-cell lung cancer.J Clin Oncol 2008; 26(21): 3543-3551
- Socinski MA et al., Weekly nab-paclitaxel in combination with carboplatin versus solvent-based paclitaxel plus carboplatin as first-line therapy in patients with advanced non-small-cell lung cancer: final results of a phase III trial.J Clin Oncol 2012; 30(17): 2055-2062
- Thatcher N et al., Necitumumab plus gemcitabine and cisplatin versus gemcitabine and cisplatin alone as first-line therapy in patients with stage IV squamous non-small-cell lung cancer (SQUIRE): an open-label, randomised, controlled phase 3 trial.Lancet Oncol 2015; 16(7): 763-774
- Teramoto K et al., A phase II study of adjuvant chemotherapy with docetaxel plus nedaplatin for completely resected non-small-cell lung cancer.WCLC 2017, P1.03-37
- Douillard JY et al., Adjuvant vinorelbine plus cisplatin versus observation in patients with completely resected stage IB-IIIA non-small-cell lung cancer (Adjuvant Navelbine International Trialist Association [ANITA]): a randomised controlled trial.Lancet Oncol 2006; 7(9): 719-727
More posts
特定の集団と条件でのEGFR TKI治療
特定の集団と条件でのEGFR TKI治療 第1世代EGFR TKIのエルロチニブとゲフィチニブのほか、第2世代EGFR TKIのアファチニブも、進行EGFR変異陽性NSCL
手術の最新情報 現在のオプションの再定義
手術の最新情報 現在のオプションの再定義 2005年、国際肺癌学会(IASLC)病期判定委員会は肺癌の完全切除の定義を提案し、これには不確実な切除の基準が含まれていた[1]
序文
序文 Fred R. Hirsch, MD, PhD IASLC の CEO 米国コロラド州デンバー コロラド大学薬科大学院教授 親愛なる皆さん、 この10年間を通じて非