免疫检查点阻滞:治疗成功的决定因素
PD-L1表达之外的各种临床因素,已作为对免疫检查点抑制产生反应的预测因子经过探索。具体而言,分析将缺少烟草暴露与 NSCLC 中 PD-1 通路阻滞的反应性降低相关联[1,2]。出现这种情况的一种可能解释是,从不吸烟或很少吸烟的肺癌患者通常显示低 TMB [3]。随着吸烟暴露的增加,每兆碱基的突变数量也会增加。TMB 已被确定为免疫检查点抑制剂反应的独立预测生物标志物,高 TMB 表示更有利的反应 [4,5]。
在回顾性评论中,Gainor 等人探讨了 PD-(L)1 抑制对晚期 NSCLC 和高 PD-L1 表达(TPS≥ 50%)的从不吸烟或轻度吸烟者的治疗作用 [6]。由于在随机研究中,从不吸烟/轻度吸烟者的登记有限,以及在 PD-(L)1 抑制剂的一线临床试验中通常排除特定分子亚群(例如,EGFR 或 ALK 突变),因此迄今尚未明确定义。总共评估了来自 4 个机构的 283 名接受检查点抑制剂治疗的患者;其中 69 人为从不吸烟或轻度吸烟者,33 人为从不吸烟者(一生吸烟少于 100 支),36 人为轻度吸烟者(年吸烟量 ≤10 包;中位年吸烟量,
1.13)。大多数患者在一线接受 PD-(L)1 抑制剂治疗。
吸烟习惯会影响 DOR
从不吸烟/轻度吸烟者中最常见的致癌驱动突变包括 KRAS 和 EGFR 突变以及 MET 外显子 14 跳跃。PD-L1 表达在从不吸烟/轻度吸烟者和重度吸烟者之间没有差异。根据吸烟状况评估 TMB;正如预期的那样,重度吸烟者
(8.2 mut/Mb) 的 TMB 高于从不吸烟/轻度吸烟者 (4.1 mut/Mb;
p = 0.002), 对于从不吸烟者和轻度吸烟者,TMB 中位数相同。
就抗-PD-(L)1 的抗肿瘤活性而言,从不吸烟/轻度吸烟者和重度吸烟者之间没有统计学上显著的 ORR 差异(31.9% 对比 39.6%;
p = 0.386)。在基线状态下,有 24 名从不吸烟者患有可评估的疾病,ORR 在数值上低于 25%,无
统计学显著性。多个致癌驱动
突变发生反应,尽管 8 例 EGFR 突变 NSCLC 患者中只有 1 例有
反应(12.5%),而 11 例 KRAS
突变疾病患者中有 4 例有反应(36.3%)。然而,应谨慎地看待这些结果,因为此类别的患者人数很少。TMB 不会影响从不吸烟/轻度吸烟者对检查点抑制剂的反应。PFS 分析显示有利于重度吸烟者的轻微趋势(从不吸烟/轻度吸烟者为 4.8 个月对比 3.29 个月;HR,1.32;p = 0.105)。
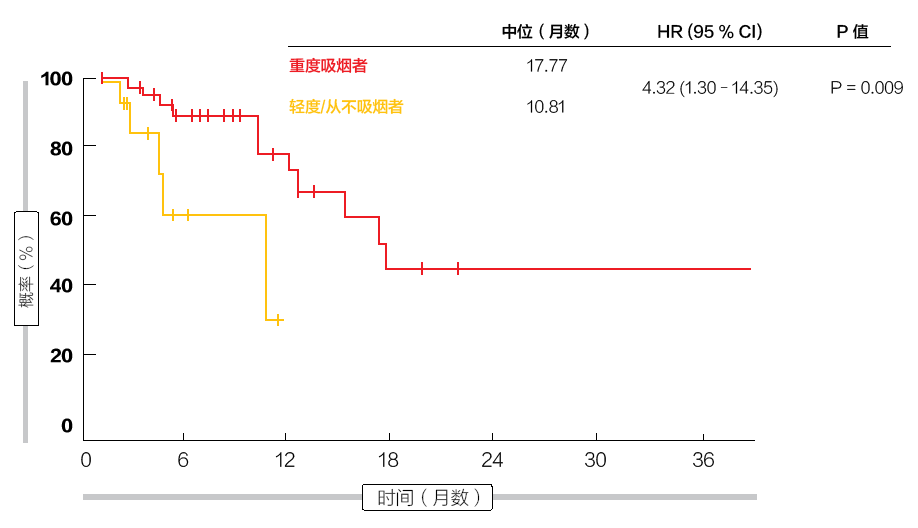
然而,一个引人注目的结果是,与从不吸烟/轻度吸烟者相比,尽管 ORR 相似,观察到重度吸烟者的 DOR 显著改善(17.77 个月对比 10.81 个月;HR 4.32;
p = 0.009;图 1)。作者总结说,确定初始反应对比反应持久性的免疫生物学特征可能不同。鉴于使用 PD-(L)1 单一疗法的 DOR 较短,应在具有高 PD-L1 表达的从不吸烟/轻度吸烟者中考虑化学疗法加 PD-1 组合。
图 1:重度吸烟者对比轻度/从不吸烟者的反应持续时间显著延长
基线类固醇的用途是什么?
皮质类固醇通常用于癌症治疗,因为它们可以减轻并迅速缓解许多癌症相关症状,并且它们是免疫相关 AE 的主要治疗方法。在这种情况下,类固醇似乎不会减少免疫检查点阻滞的活性。然而,PD-(L)1 抑制剂在接受基线类固醇治疗的患者中的疗效曾经是未知的,因为这些患者通常不符合研究免疫疗法的临床试验的资格。
Arbour 等人对来自凯特琳癌症中心(MSKCC)和古斯塔夫鲁西癌症中心(GRCC)的 455 名和 185 名患者的数据进行了回顾性分析,目的是评估 PD-(L)1 抑制对接受基线类固醇治疗的患者(治疗第 1 天使用 ≥ 10mg 泼尼松或同等剂量药物)的效果[7]。在这两个机构中,共有 90 名患者在开始 PD-(L)1 抑制治疗时接受了类固醇治疗。
两个独立同期群中的活性减少
数据清楚地证明了基线类固醇治疗对 PD-(L)1 阻滞的不利影响,例如较低的 ORR。在 MSKCC 同期群中,类固醇组和无类固醇组中发生的完全和部分缓解分别为 6% 对比 19 % (p = 0.02)。对于 GRCC 同期群,分析显示出 8 % 对比 18 % (p = 0.2) 的类似结果。在两个同期群中观察到接受基线类固醇的患者的 PFS 结果较差 (MSKCC: HR, 1.7;p < 0.0001;
GRCC: HR, 1.5;p < 0.0001)。同样,在两个机构的类固醇组中,OS 在开始 PD-(L)1 阻滞治疗后显著降低(MSKCC:HR, 2.1;
p < 0.0001;GRCC: HR, 2.0;
p < 0.001)。使用来自两个同期群的汇总数据的亚组分析显示,在几乎每个亚组中,接受基线类固醇的患者的 PFS 和 OS 结果更差。当然,对有脑转移或状态不佳的患者,类固醇通常用于姑息治疗。然而,根据多变量分析,在调整消极的预后变量后,基线类固醇使用的有害 PFS 和 OS 效应仍然存在。
研究人员指出,观察到的效应是否具有预测性和/或预后性尚不确定。基于这些结果,他们建议在计划接受 PD-(L)1 抑制治疗的患者中谨慎使用类固醇。这包括考虑用于治疗癌症症状的非类固醇替代品,但不应拒绝为患者提供医学上必需的类固醇(例如,用于治疗脑转移瘤)。由于该分析仅包括接受单药 PD-(L)1 抑制治疗的患者,因此对接受化疗和与检查点抑制剂组合治疗的患者的影响尚不明确。
预测长期反应的特征
在选定病例中,使用抗-PD-(L)1 疗法获得的缓解可能持续数年,但预测长期反应 (LTR) 的特征尚未得到描述。因此,Rizvi 等人分析了从 2011 年至 2016 年在 MSKCC 接受抗-PD-(L)1 治疗的 766 例晚期 NSCLC 患者[8]。LTR 被定义为持续超过 18 个月的 PFS。对于 62 名患者(总同期群的 8%),情况确实如此。其中,47 例(76%)达到完全或部分缓解,15 例(24%)达到疾病稳定。在分析时,68% 仍然没有进展。
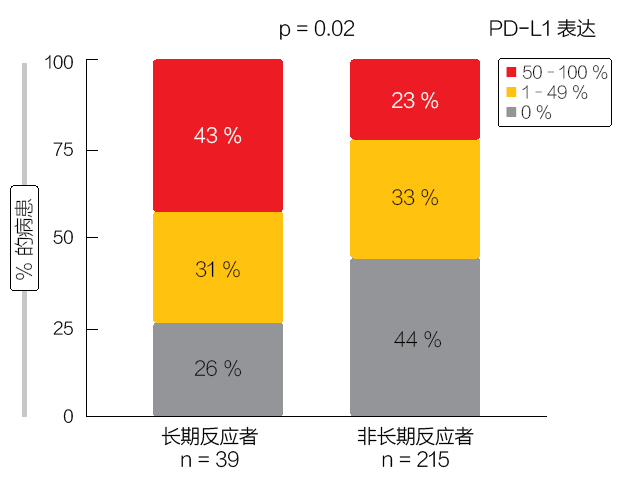
作者确定了 LTR 的一些典型特征。长期反应者的 TMB 明显高于无 LTR 的患者(12.24 对比 6.34 mut/Mb;p <0.001),并且 PD-L1 高表达患者的比例更高 (p = 0.02;图 2)。此外,吸烟者绝大多数
是 LTR 患者,而从不吸烟者是例外;对于没有 LTR 的患者,这种分布更加平衡。在这方面,该分析得出了两组之间的显著差异 (p = 0.03)。EGFR 突变状态显示与 LTR 呈负相关:长期反应者均未携带 EGFR 突变,而 12% 无 LTR 的患者亦是如此 (p = 0.002)。
长期和短期反应者的直接对比表明,两组之间的 TMB(但并非 PD-L1)表达存在显著差异。此外,结果表明缓解深度与 LTR 相关,但与肿瘤负荷无关。长期和短期反应者的基线肿瘤负荷相似。
作者得出结论,预测持久反应的特征可能确实与生物标记物通常关注的预测初始反应的特征不同。
图 2:LTR 患者中高 PD-L1 表达的比例更高
参考
- Borghaei H et al., Nivolumab versus docetaxel in advanced non-squamous non-small cell lung cancer. N Engl J Med 2015; 373(17): 1627-1639
- Gainor JF et al., EGFR mutations and ALK rearrangements are associated with low response rates to PD-1 pathway blockade in non-small cell lung cancer: a retrospective analysis. Clin Cancer Res 2016; 22(18): 4585-4593
- Gibbons DL et al., Smoking, p53 mutation, and lung cancer. Mol Cancer Res 2014; 12(1): 3-13
- Rizvi H et al., Molecular determinants of response to anti-programmed cell death (PD)-1 and anti-programmed death-ligand 1 (PD-L1) blockade in patients with non-small-cell lung cancer profiled with targeted next-generation sequencing. J Clin Oncol 2018; 36(7): 633-641
- Hellmann M et al., Nivolumab plus ipilimumab in lung cancer with a high tumor mutational burden. N Engl J Med 2018; 378(22): 2093-2104
- Gainor JF et al., Response and durability of checkpoint blockade in never- or light-smokers with NSCLC and high PD-L1 expression. J Clin Oncol 36, 2018 (suppl; abstr 9011)
- Arbour KC et al., Deleterious effect of baseline steroids on efficacy of PD-(L)1 blockade in patients with non-small cell lung cancer. J Clin Oncol 36, 2018 (suppl; abstr 9003)
- Rizvi H et al., Clinical and molecular features predicting long-term response (LTR) to anti-PD-(L)1 based therapy in patients with NSCLC. J Clin Oncol 36, 2018 (suppl; abstr 9022)
More posts
PD-(L)1 单独和联合抑制:近期对免疫疗法的见解
转移性非小细胞肺癌 (NSCLC) 患者与化疗相比,使用抗-PD-1 单克隆抗体派姆单抗的单药疗法显著改善了临床疗效指标。除了无进展生存期 (PFS) 获益外,KEYNOTE-024 显示总生存 (OS) 有所提高;此外,接受派姆单抗治疗的患者比接受化疗的患者具有更好的安全性。 由于对转移性 NSCLC 的更有效和可耐受的一线治疗方案未满足部分需求,KEYNOTE-042 研究了派姆单抗在表达 PD-L1 的任何组织学的先前未治疗、局部晚期或转移性肺肿瘤患者中的作用(肿瘤比例评分[TPS]≥1%),但未发现致敏 EGFR 或 ALK 改变。
前言
作为医师和研究人员,我们很幸运能够参与由精准医学带来的癌症研究和治疗的重大创新。虽然精准医学似乎是在一夜之间取得成功,但它实际上是一种经过深思熟虑的战略研究途径,基于来自世界各地的潜心研究的科学家数十年来艰苦、有素的工作。在肺癌中,精准医学帮助确定致癌基因,以便用靶向疗法进行有效治疗,而免疫疗法的兴起,也在过去 10 到 15 年内对许多患者的治疗发挥关键作用。