免疫疗法:毒性管理
免疫检查点抑制剂的毒性从根本上源于它们是以一种生理学方式促进 T 细胞活性。“免疫系统的放大导致自体免疫性疾病,”Ross Soo 解释称(Ross Soo 身为医学博士,FRACP,就职于新加坡国立大学癌症研究所)。
常见不良事件(AE)包括疲劳、厌食和关节痛。表示免疫相关不良事件(irAE)的英文术语通常以-itis 或-opathy 结尾。CTLA-4 抑制剂、PD-1/PD-L1 抑制剂及其联合用药可能引起发烧、寒战和嗜睡[1]。皮疹往往是斑状丘疹型,而肠胃道事件包括腹泻和结肠炎并伴有溃疡。还可能发生肝功能检测指标升高。潜在的内分泌并发症包括垂体炎、甲状腺炎和肾上腺功能不全。罕见情况下可观察到神经病变、肾炎、肺炎、格林-巴利综合征、肉样瘤和重症肌无力。根据所使用免疫治疗剂的作用机制,具体 AE 略有变化。
PD-1/ PD-L1 药物的耐受性提高
对于接受 CTLA-4 抑制剂治疗的患者,irAE 可能在数天或数月内发生,或者甚至在治疗中止后仍有可能发生 ,这就是为什么应当在这些病人治疗停止后仍继续对其进行随访的原因。与 CTLA-4 治疗相关的早期 AE 包括搔痒和皮疹,而垂体炎和肝毒性属于晚期毒性。Soo 博士解释称:“当这些药物与其他药剂联用时,AE 的风险自然而然会增加”。一个覆盖 22 项试验、涉及 1200 名患者的荟萃分析对使用 CTLA-4 抑制剂治疗的全级别 irAE和级别≥3 的 irAE 的发生率进行了评估,得出结果分别为 72 %和 25 % [2]。 与抗 CTLA – 4 治疗相比,PD-
1/PD-L1 抑制剂疗法引起 irAE 的可能性一般较小。此外,在临床研究中,抗 PD-1 抗体经常显示出远高于其化疗对照药的耐受性。在 CheckMate 017试验中,使用多西他赛的任何治疗相关 AE 发生率为 86 %,而在使用纳武单抗的情况下这一数据仅为 58 %。关于 3/4 级事件,其发生率分别为 55 %和 7 %[3]。在调查相同药物在具有不同组织学的患者中的作用的CheckMate 057 研究中,也得出了相似的数字[4]。值得注意的是,PD-1 抑制剂治疗极少出现(发热性)嗜中性粒细胞减少,并且其在非血液毒性方面(如疲劳、恶心、周围神经病变)也有显著优势。纳武单抗的 AE 倾向于 在治疗的前三个月内集中出现[5]。在此之后,发生率明显下降。在很大比例的患者中可观察到 AE 消退。
当出现 irAE 时应当如何处理?
irAE 管理中应当采取的第一步是识别其他原因。有必要进行密切监视。如果找不到明确的其他原因,则应当将所有具有炎症性质的事件视为与免疫相关。Soo 博士称:“医生们只要用谷歌搜索产品夹带说明书,就能获得关于如何管理毒性的简单信息”。另外,还可以获取一些综述文章,这些文章概述一系列毒性反应的管理,并对治疗方法提出建议[6–9]。
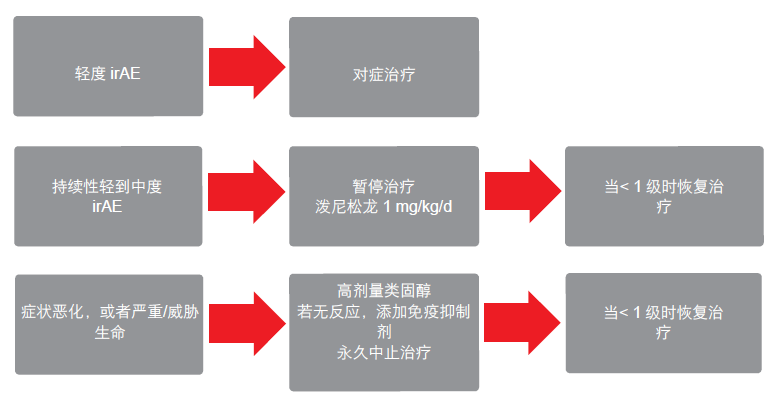
低级别 AE 可以通过对症/局部手段予以控制(图)。如果低级别事件顽固持续,或者发生严重 AE,就应当考虑采用全身皮质类固醇治疗。在患者对全身类固醇治疗无反应时,强效免疫抑制药物是一种选择。Soo 博士 指出:“病人教育具有重要作用”。制药行业提供了关于各种药物的信息
宣传单。
图: AE 管理的总体原则
总而言之,增加对运用免疫检查点抑制剂的专业知识能够起到改善毒性管理的作用。Soo 博士强调称“临 床研究中由治疗相关 AE 造成的治疗中止率很低”。
来源:Educational session “New challenges in immunotherapy for lung cancer”, 18th December 2015
参考文献
- Weber JS et al., Toxicities of immunotherapy for the practitioner. J Clin Oncol 2015; 33(18): 2092-2099
- Bertrand A et al., Immune related adverse events associated with anti-CTLA-4 antibodies: systematic review and meta-analysis. BMC Medicine 2015; 13: 211
- Brahmer J et al., Nivolumab versus docetaxel in advanced squamous-cell non-small-cell lung cancer. N Engl J Med 2015; 373(2): 123-135
- Borghaei H et al., Nivolumab versus docetaxel in advanced non-squamous non-small-cell lung cancer. N Engl J Med 2015; 373(17): 1627-1639
- Reckamp K et al., WCLC 2015
- Gangadhar TC & Vonderheide RH, Mitigating the toxic effects of anticancer immunotherapy. Nat Rev Clin Oncol 2014; 11(2): 91-99
- Fecher LA et al., Ipilimumab and its toxicities: a multidisciplinary approach. Oncologist 2013; 18(6): 733-743
- Howell M et al., Optimal management of immune-related toxicities associated with checkpoint inhibitors in lung cancer. Lung Cancer 2015; 88(2): 117-123
- Naidoo J et al., Toxicities of the anti-PD-1 and anti-PD-L1 immune checkpoint antibodies. Ann Oncol 2015; 26(12): 2375-2391
More posts
免疫疗法:毒性管理
免疫检查点抑制剂的毒性从根本上源于它们是以一种生理学方式促进 T 细胞活性。“免疫系统的放大导致自体免疫性疾病,”Ross Soo 解释称(Ross Soo 身为医学博士,FRACP,就职于新加坡国立大学癌症研究所)。 常见不良事件(AE)包括疲劳、厌食和关节痛。表示免疫相关不良事件(irAE)的英文术语通常以-itis 或-opathy 结尾。
“PD-L1 表达如噩梦般复杂”
在免疫疗法中有两个问题紧密关联于生物标志物这一主题。首先,所有试图定义生物标志物的尝试都主要集中在作为疗效标志的反应性上。但是我们必须认识到,免疫疗法并不是靶向疗法,而且在这种治疗中并不一定能够观察到快速的肿瘤缩小。一种免疫疗法的疗效是由持久的肿瘤稳定所定义的。我们不得不对反应率在此是否为合适的终点提出质疑。 第二个问题是确定在免疫疗法中开发生物标志物的必要性。
免疫疗法:大量预治疗之后令人瞩目的抗肿瘤活性
抗 PD-1 抗体派姆单抗( pembrolizumab )和纳武单抗(nivolumab)已被证明对肺癌具有活性。派姆单抗是一种抗 PD-1 的高亲和力人源化单克隆 IgG4κ 抗体,其能够阻止带有 PD-L1 和 PDL2 的受体发生相互作用。KEYNOTE-001 试验证明,派姆单抗对晚期 NSCLC 具有显著的抗肿瘤活性,其在 PD-L1 肿瘤比例评分(TPS)方面的结果得到提高,达 ≥50% 。TPS 反映了 PD-L1 在肿瘤上的表达。≥50%的界限是利用来自KEYNOTE-001 的独立训练和验证数据集确定的。
寡转移疾病患者的风险与机会
在全身治疗不断进步的背景下,对于患有有限数目血行转移瘤的 NSCLC 患者的潜在治愈期望与日俱增。Suresh Senan 博士(MRCP、FRCR 就职于荷兰阿姆斯特丹 VU 大学医学中心[1])解释称:“大多数研究将寡转移定义为一到三个或者一到五个病灶”。根据临床情况,存在同时性(在原发性肿瘤诊断时检出的)和异时性(在对原发性肿瘤治疗后出现的)寡转移瘤。如 Senan 博士所指出,能够区分这这两者的时间间隔不是标准化的,但通常使用 6-12 个月的时间跨度。
使用 EGFR TKI 疗法后的疾病进展:在埃罗替尼、吉非替尼和阿 法替尼之后还有哪些手段?
获得性耐药的最常见机制是在 EGFR基因的外显子 20 内发生的 T790M 突变(图 1)。当出现这种突变时,通常会发生无痛缓慢肿瘤生长[2]。在ESMO 亚洲大会的一场研讨会上,来自美国波士顿 Dana Farber 癌症研究所 Lowe 胸部肿瘤中心的 Pasi A. Jänne博士解释称:“可能有必要进行反复成像来确定病情进展”。 T790M 通过一种不同寻常的耐药机制而产生作用,在此过程中它会改变 EGFR 受体对其天然基质 ATP 的亲和力。尽管像吉非替尼和埃罗替尼这类药物作为竞争性抑制剂,在结合位点处排挤 ATP 结合,但是在这种突变的存在下,受体表现出对 ATP 的更大亲和力。
EGFR 突变阳性非小细胞肺癌:扩大用于既定治疗方案的数据 池
伴有激活的表皮生长因子受体(EGFR )突变的非小细胞肺癌(NSCLC)代表了肺癌的一个确定的分子亚型,该亚型能够用 EGFR 酪氨酸激酶抑制剂(TKI)疗法进行靶向治疗。埃罗替尼(erlotinib)、吉非替尼(gefitinib)和阿法替尼(afatinib)都已被批准作为 EGFR 突变阳性NSCLC 的一线治疗选择。第一代 TKIs埃罗替尼和吉非替尼通过可逆抑制EGFR 来发挥效用,而第二代 TKI 阿法替尼则通过不可逆抑制更广泛的信号级联来起到 ErbB 家族阻断剂的作用。