罕见驱动突变:BRAF和HER2突变NSCLC
一线达拉菲尼加曲美替尼
BRAF驱动突变在NSCLC中十分罕见,仅占2 % [1, 2],但具有BRAFV600E突变的肿瘤具有暗示侵袭性生物学的组织学特征[3]。当采用铂类化疗进行治疗时,这些患者表现出较为不利的结果[3, 4]。
多队列非随机化II期BRF113928研究使用BRAF抑制剂达拉菲尼和MEK抑制剂曲美替尼在晚期BRAFV600E突变NSCLC患者中探究了靶向方法。该试验包括达拉菲尼单药治疗组(队列A)以及接受每日两次150 mg达拉菲尼加每日一次2 mg曲美替尼的两个联合组(队列B和队列C)。队列B由经过预先治疗的患者组成,而队列C包含初治群体。各队列的主要终点是研究人员评估的ORR。独立审查委员会(IRC)根据RECIST对反应进行了审查。
队列A与队列B之间的间接比较表明,在经过预先治疗的患者中,采用达拉菲尼和曲美替尼联合给药比采用达拉菲尼单药治疗获得更高的ORR和更长的中位PFS [5, 6]。在2017年ESMO大会上,Planchard等人介绍了在由36名IV期NSCLC患者组成的初治队列C中获得的结果[7]。这是对BRAF和MEK抑制剂组合作为BRAFV600E突变转移性NSCLC患者的一线疗法进行的首个研究。
2年时51%存活
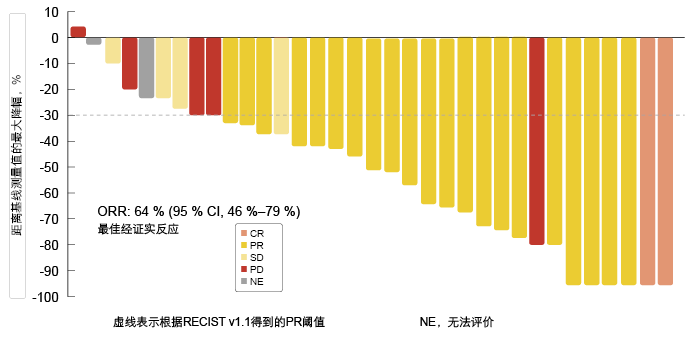
达拉菲尼加曲美替尼方案产生显著的抗肿瘤活性和持久的反应。根据研究人员和IRC评估,ORR为64%。根据研究人员和IRC审查,连同显示SD的患者比例,该方案达到的DCR分别为75%和72%。两名患者经历CR,21名患者达到PR(图)。根据研究人员和IRC评估,反应持续时间分别为10.4个月和15.2个月。中位PFS分别为10.9个月和14.6个月。在第6个月,分别有72%和69%的患者无进展。该联合方案产生了24.6个月的初步中位OS。51%的患者在2年时仍存活。ORR、反应持续时间和PFS与先前在BRF113928中接受过联合治疗的队列所报告的结果类似[5, 6]。
安全特性证明是可控的,并且与先前采用联合治疗的经验相似。所有等级AE需要中止治疗的比率为19%,剂量减少的比率为31%。发热、恶心和腹泻是最常见AE。未观察到新的安全性信号。基于这些结果,达拉菲尼加曲美替尼近期被EMA和FDA批准用于表达BRAFV600E突变的转移性NSCLC患者,而不考虑先前治疗史如何。
图: 研究人员评估的采用达拉菲尼加曲美替尼联合治疗的目标病灶最大变化
接受过大量预先治疗的HER2突变患者中的阿法替尼
约1-4%的肺腺癌携带HER2突变[8],但这些患者仍缺乏经批准的靶向疗法。阿法替尼通过不可逆地抑制来自所有ErbB家族受体同源二聚体和异源二聚体(包括HER2)的信号传导而发挥作用[9, 10]。2010年发起的全球性指定患者使用计划正在提供关于在无确定性治疗选择的NSCLC患者的全球临床实践中使用阿法替尼的真实数据。Peters等人报道了HER2突变NSCLC队列的治疗结果[11]。
在指定患者使用计划中进行治疗的患者接受每天50 mg阿法替尼;较低的起始剂量允许由医师自行决定。截至2017年4月,可获取28名患者的数据。其中一半以上曾接受过三种或更多种前线全身治疗。第一代EGFR TKI单药疗法的给予率达到36%。7名患者曾接受过HER2靶向药物。在外显子20中鉴定出所有特定HER2突变,其中最常见的突变类型是2325/YVMA插入(n = 8)。
分析显示出阿法替尼具有临床意义的疗效。中位治疗失败时间(TTF)为2.9个月;这里,与具有其他特定HER2突变的患者(1.9个月)相比,显示2325/YVMA插入的患者经历显著改善的TTF(9.9个月)。在总群体中,32%的患者TTF > 1年。在16名具有可用反应数据的患者中,ORR和DCR分别为19%和69%。这与来自另一探究阿法替尼在HER2突变NSCLC中作用的国际多中心研究的结果相一致[12]。具有2325/YVMA插入的患者获得100%的疾病控制。未发生意料之外的AE。基于这些结果,在HER2突变NSCLC患者早期治疗线中对阿法替尼进行评估可能是必要的。
参考文献
- Barlesi F et al., Routine molecular profiling of patients with advanced non-small-cell lung cancer: results of a 1-year nationwide programme of the French Cooperative Thoracic Intergroup (IFCT). Lancet 2016; 387: 1415-1426
- Kris MG et al., Using multiplexed assays of oncogenic drivers in lung cancers to select targeted drugs. JAMA 2014; 311: 1998-2006
- Marchetti A et al., Clinical features and outcome of patients with non-small-cell lung cancer harboring BRAF mutations. J Clin Oncol 2011; 29: 3574-3579
- Cardarella S et al., Clinical, pathologic, and biologic features associated with BRAF mutations in non-small cell lung cancer. Clin Cancer Res 2013; 19: 4532-4540
- Planchard D et al., Dabrafenib in patients with BRAF(V600E)-positive advanced non-small-cell lung cancer: a single-arm, multicentre, open-label, phase 2 trial. Lancet Oncol 2016; 17: 642-650
- Planchard D et al., Updated survival of patients (pts) with previously treated BRAF V600E–mutant advanced non-small cell lung cancer (NSCLC) who received dabrafenib (D) or D + trametinib (T) in the phase II BRF113928 study. J Clin Oncol 2017; 35(suppl) abstract 9075
- Planchard D et al., Phase 2 trial (BRF113928) of dabrafenib plus trametinib in patients with previously untreated BRAFV600E-mutant metastatic non-small cell lung cancer. ESMO 2017, abstract LBA51
- Peters S & Zimmermann S, Targeted therapy in NSCLC driven by HER2 insertions. Transl Lung Cancer Res 2014; 3(2): 84-88
- Solca F et al., Target binding properties and cellular activity of afatinib (BIBW 2992), an irreversible ErbB family blocker. J Pharmacol Exp Ther 2012; 343(2): 342-350
- Li D et al., BIBW2992, an irreversible EGFR/HER2 inhibitor highly effective in preclinical lung cancer models. Oncogene 2008; 27(34): 4702-4711
- Peters S et al., Activity of afatinib in heavily pre-treated patients with HER2 mutation-positive advanced NSCLC: findings from a global NPU programme. ESMO 2017, abstract 1355P
- Lai W-C V et al., Afatinib in patients with metastatic HER2-mutant lung cancers: An international multicenter study. J Clin Oncol 2017; 35(suppl) abstr 9071
More posts
免疫刺激作为有希望的SCLC疗法
关于广泛性疾病小细胞肺癌(SCLC)存在较高的未获满足医疗需求,该疾病显示出较差的结果,中位OS为9-11个月。一线化疗通常引起明显反应,而反应者通常仅经历有限的疾病控制期。 基于激活免疫系统可延长这些患者的病情稳定性,从而最终影响其生存期的假设,Thomas等人评估了toll样受体9(TLR9)激动剂lefitolimod的活性。lefitolimod利用在化疗过程中降低的肿瘤负荷和释放的肿瘤抗原通过多种途径来广泛增强先天和获得性免疫系统而进行免疫监视。
免疫疗法:再次处于进步前沿
约三分之一的非小细胞肺癌(NSCLC)患者会出现III期局部晚期疾病。对于具有良好表现状态且不可切除肿瘤的患者,治疗标准为铂类双化疗伴随并行放疗。由于多年来对于该种环境没有发生重大进展,因此对于延长生存期的新型治疗途径存在显著的未满足需求。考虑到检查点抑制剂在转移性疾病中的功效,启动了全球性双盲PACIFIC试验作为首个随机化III期研究,用于评估III期、局部晚期、不可切除NSCLC患者的免疫检查点阻断。
序言
2018年6月28日和29日,面向肿瘤内科医师的Lung Cancer International Preceptorship在中国上海召开。场地提供方为同济大学附属上海市肺科医院。在这两天的时间里,我们举办了讲座和研讨会,旨在提高与会者对中国以及国际肺癌管理的了解。参加指导会议的24名代表中,绝大多数在中国医院工作。会议主题范围涵盖了肺部恶性肿瘤的筛查、诊断和病理学以及各种类型的治疗。会议最后环节为参观上海市肺科医院。