靶向疗法联合放疗用于治疗脑转移
肺腺癌常常转移到脑部,且脑转移患者的预后较差。在相当一部分原发性肺腺癌和脑转移患者,特别是亚洲患者中发生EGFR基因突变。据2017年CSCO年会上的报告,这些脑转移患者中EGFR突变的发生率在中国台湾约为44%,在日本约为63%,远高于美国或欧洲(0%-2%)[1]。在2017年CSCO年会上,这些脑转移治疗的主要进展集中于驱动致癌基因阳性靶向治疗(伴有或不伴有放疗)的功效,以及放疗与EGFR/ALK酪氨酸激酶抑制剂(TKI)在驱动致癌基因阳性非小细胞肺癌(NSCLC)患者中的最佳用药顺序。
驱动致癌基因阳性NSCLC中脑转移的靶向治疗
第一代EGFR/ALK TKI在伴有脑转移的驱动致癌基因阳性NSCLC患者中显示出改善的无进展生存期(PFS)。Kim JE等人[2]进行了一项纳入伴有无症状脑转移的EGFR突变阳性NSCLC患者的研究。患者接受每日一次的吉非替尼(250mg)或厄洛替尼(150mg)作为一线治疗。结果显示,在23名患者中,16名达到部分缓解(PR),3名达到稳定疾病(SD),4名疾病进展。中位PFS和总生存期(OS)分别为7.1和18.8个月[2]。
PROFILE 1005和1007研究回顾性地分析了ALK和ROS1抑制剂克唑替尼在伴有先前未经治疗的无症状脑转移的晚期ALK重排NSCLC患者中的疗效。结果显示,在12周时的全身疾病控制率(DCR)为63%,颅内DCR为56%,中位颅内进展时间(TTP)为7个月。重要的是,在开始克唑替尼治疗后新发生疾病进展的患者中有20%被诊断患有脑转移。因此,第一代TKI(包括EGFR TKI和ALK TKI)对于治疗伴有脑转移的驱动致癌基因阳性NSCLC患者是有效的。然而,只达到相对较短的PFS、OS和TTP延长,以及相对较低的DCR [3]。此外,在ALK TKI治疗后仍有较高比例的患者发生脑转移,这一结果并不令人鼓舞。
中枢神经系统对奥希替尼的应答
奥希替尼和艾乐替尼的出现为治疗伴有脑转移的驱动致癌基因阳性NSCLC患者提供了新选择。AURA3试验是对比奥希替尼与铂-培美曲塞在中枢神经系统(CNS)转移患者中疗效的首个比较性证据试验。与化疗相比,奥希替尼改善了客观缓解率(70%与31%),且奥希替尼组的PFS显著改善(10.1与4.4个月;针对亚洲或非亚洲种族做出调整后风险比[HR],0.30;95% CI,
0.23-0.41;p < 0.001)。奥希替尼的PFS HR优于进行分析的所有预先设定的亚组,包括CNS转移患者(中位PFS,8.5与4.2个月;HR,0.32;95% CI,0.21至0.49)[4]。
与第一代EGFR TKI的数据相比,FLAURA试验随后显示,在伴有脑转移的EGFR突变阳性NSCLC的一线治疗中,奥希替尼的中位PFS与第一代EGFR TKI相比有所改善(15.2与9.6个月;HR 0.47;95% CI,0.30-0.74;p <0.001)[5]。
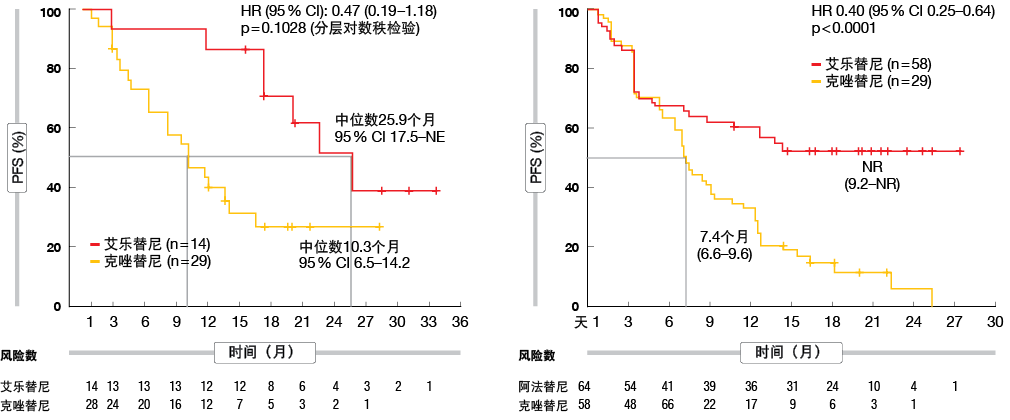
最近发表的J-ALEX和ALEX研究对艾乐替尼与克唑替尼作为ALK突变阳性NSCLC患者的一线治疗的疗效进行了比较。据报道,艾乐替尼显示出血脑屏障渗透性的改善。因此,与克唑替尼相比,艾乐替尼治疗为伴有CNS转移的NSCLC患者提供了改善的PFS(J-ALEX:25.9与10.3个月,P = 0.1028;
ALEX:未达到与7.4个月,p < 0.0001) (图1)。此外,与克唑替尼组相比,艾乐替尼组显示较低的12个月累积CNS转移发生率(16.0%与58.3%)[6]。
图1: 在J-ALEX(左)和ALEX(右)研究中,艾乐替尼与克唑替尼治疗在基线时伴有CNS转移的ALK突变阳性NSCLC患者获得的无进展生存率
对抗脑转移的策略——前期放射外科手术与放疗与酪氨酸激酶抑制剂
酪氨酸激酶抑制剂已证实对脑转移发生率的疗效,并且在脑转移NSCLC患者中可延长PFS。此外,全脑放疗(WBRT)和立体定向放射外科手术(SRS)已被用于治疗脑转移NSCLC患者。WBRT被认为是体积较大肿瘤或具有超过三个病灶的患者的标准治疗方法。常见的副作用包括认知损害和执行功能改变等神经认知功能障碍。SRS适用于预后较好的患者,且根据Shultz DB等人[7]的报道,多疗程SRS和在初始SRS后推迟用于远端脑转移的WBRT似乎是安全和有效的方法。为了进一步延长患者生存期,联合SRS、WBRT和靶向疗法似乎是有效的。
Magnuson WJ等人[8]进行了回顾性研究,比较这些治疗对伴有颅内进展的EGFR突变NSCLC患者的疗效:SRS随后EGFR TKI;WBRT随后EGFR TKI;以及EGFR TKI随后SRS或WBRT。研究结果显示,这些SRS(n = 100)、WBRT(n=120)和EGFR TKI(n = 131)队列的中位OS分别为46、30和25个月(p < 0.001)。前期使用SRS提供了最佳OS,并对WBRT显示出较低的潜在神经认知后遗症。最后,作者还指出,虽然前期SRS似乎是最佳选择,但在靶向疗法的时代仍存在若干不确定性。因此,需要进行前瞻性III期研究[1]。
国内管理驱动致癌基因阳性NSCLC中的中枢神经系统转移的最佳策略
Yang JJ等人[9]在中国进行了3期研究,对EGFR TKI埃克替尼与全脑照射(WBI)在驱动致癌基因阳性NSCLC和脑转移患者中的疗效进行了比较。结果显示,使用埃克替尼的中位颅内PFS与WBI相比有所改善(10与4.8个月;p = 0.014),且在埃克替尼组中高于3级不良事件的发生率与WBI组相比较低(8%与38%)[9]。因此,作者认为,在中国,EGFR TKI应该是伴有脑转移的EGFR突变阳性NSCLC患者的治疗选择。
参考文献
- Lu Y et al., Management of CNS Metastasis in Patients with Driver Oncogene Positive NSCLC. CSCO 2017
- Kim JE et al., Epidermal Growth Factor Receptor Tyrosine Kinase Inhibitors as a First-Line Therapy for Never-Smokers with Adenocarcinoma of the Lung Having Asymptomatic Synchronous Brain Metastasis. Lung Cancer. 2009 Sep;65(3):351-4.
- Costa DB et al., Clinical Experience With Crizotinib in Patients with Advanced ALK-Rearranged Non-Small-Cell Lung Cancer and Brain Metastases. J Clin Oncol. 2015 Jun 10;33(17):1881-8.
- Mok TS et al., Osimertinib or Platinum–Pemetrexed in EGFR T790M-Positive Lung Cancer. N Engl J Med. 2017 Feb 16;376(7):629-640.
- Soria JC et al., Osimertinib in Untreated EGFR-Mutated Advanced Non–Small-Cell Lung Cancer. N Engl J Med. 2018 Jan 11;378(2):113-125. doi: 10.1056/NEJMoa1713137.
- Peters S et al., Alectinib versus Crizotinib in Untreated ALK-Positive Non–Small-Cell Lung Cancer. N Engl J Med. 2017 Aug 31;377(9):829-838.
- Shultz DB et al., Repeat Courses of Stereotactic Radiosurgery (SRS), Deferring Whole-Brain Irradiation, for New Brain Metastases after Initial SRS. Int J Radiat Oncol Biol Phys. 2015 Aug 1;92(5):993-999
- Magnuson WJ et al., Management of Brain Metastases in Tyrosine Kinase Inhibitor-Naïve Epidermal Growth Factor Receptor-Mutant Non–Small-Cell Lung Cancer: a Retrospective Multi-Institutional Analysis. J Clin Oncol. 2017 Apr 1;35(10):1070-1077.
- Yang JJ et al., Icotinib versus Whole-Brain Irradiation in Patients with EGFR-Mutant Non–Small-Cell Lung Cancer and Multiple Brain Metastases (BRAIN): a Multicentre, Phase 3, Open-Label, Parallel, Randomised Controlled Trial. Lancet Respir Med. 2017 Sep;5(9):707-716.
More posts
免疫疗法临床应答的确定
免疫疗法临床应答的确定 在过去13年中,非小细胞肺癌(NSCLC)的治疗发生了翻天覆地的变化。两种新治疗方法(靶向治疗和免疫疗法)的出现推翻了之前医生和患者对NSCLC治疗
ALK突变阳性NSCLC患者治疗新见解
ALK突变阳性NSCLC患者治疗新见解 间变性淋巴瘤激酶(ALK)是一种融合致癌基因,且NSCLC患者中ALK突变的发生率在不同种族间类似。在2017年CSCO年会上,治疗
用于治疗EGFR突变肺癌的最佳策略
用于治疗EGFR突变肺癌的最佳策略 EGFR TKI的出现改变了EGFR突变NSCLC患者的治疗标准。IPASS是在中国EGFR突变NSCLC患者中对第一代EGFR TKI
治疗鳞状细胞癌的不同疗法
治疗鳞状细胞癌的不同疗法 鳞状细胞癌(SqCC)是非小细胞肺癌(NSCLC)的组织病理学亚型之一,并且占到NSCLC患者中的20%至30% [1]。遗憾的是,很少有研究探索
EGFR突变NSCLC的诊断:从指南到现实
EGFR突变NSCLC的诊断:从指南到现实 在过去十年中,对驱动非小细胞肺癌(NSCLC)中肿瘤发生、维持和进展的关键分子和细胞机制的日益了解促进了各种新药物靶点的发现和新
中国NSCLC治疗指南:进展与争议
中国NSCLC治疗指南:进展与争议 肺癌(LC)是全球肿瘤死亡的首要诱因。每年有180万人被诊断出患有LC,并且每年死亡人数达160万。非小细胞肺癌(NSCLC)是最常