悪性中皮腫で前例のない転帰範囲に到達
悪性胸膜中皮腫(MPM)は希ですが、予後不良の侵襲性の強い癌です。ベバシズマブの有無にかかわらず、プラチナおよびペメトレキセドとの併用化学療法が第一選択治療での標準である一方、今まで承認された第二選択法は確立されなかった[1]。この状況ではゲムシタビンまたはビノレルビンが使用されることが多いが、これらは限られた活性だけを示す[2]。
しかし、MPM患者での免疫療法の評価には強い論理的根拠がある。これらの腫瘍の炎症表現型はT細胞の関与をほのめかし、MPM細胞は症例のかなり大きな割合でPD-L1を発現する[3-6]。さらに、PD-L1発現はMPMでの予後不良と相関関係があった[7、8]。
MAPS2:併用免疫療法
MAPS-2無作為化非比較フェーズII臨床試験は独立して、隔週で3mg/kgのニボルマブ(n = 63)と、6週間毎に1mg/kgの抗CTLA-4抗体イピリムマブとのニボルマブの併用(n = 62)を、最長2年間、疾患の進行または毒性まで評価した。切除不能なMPMで、ペメトレキセド/プラチナ二剤を含む1回または2回の化学療法後の進行が記録されている患者を登録した。各群で、PD-L1発現状態が患者の79%にあった。
12週時の疾患制御率(DCR)が統計的計画に基づいて主要評価項目と定義され、療法の群で適合した。最初の108人の有資格患者のうち、併用とニボルマブ単剤療法で治療を受けた患者のそれぞれ50.0%と44.4%が、以前報告された通りに12週時に疾患制御を経験した[9]。ITT集団では、DCRがそれぞれ51.6%と39.7%であった。これらは、病歴データや以前の非免疫療法臨床試験と比較して有意な増加である。
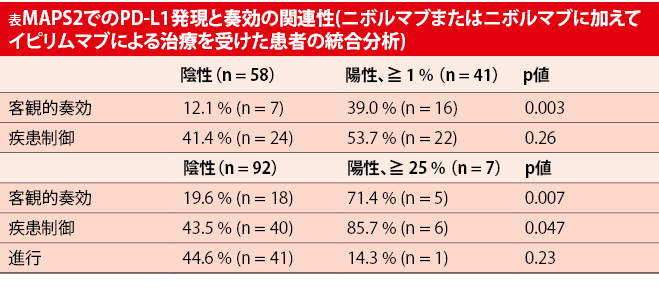
Zalcman等は、2017年ESMO学会でMAPS-2臨床試験からの最新所見を発表した[10]。PD-L1状態にある患者の統合分析によると、1%以上のPD-L1発現は奏効と有意に相関し、高いPD-L1発現(25%以上)は客観的奏効と疾患制御の両方に相関した(表)。奏効期間中央値はそれぞれ、7.9ヶ月と7.4ヶ月であった。すべての組織学的亜型
(すなわち、類上皮、二相性、肉腫様)で長期にわたる寛解が観察された。
悪性胸膜中皮腫(MPM)は希ですが、予後不良の侵襲性の強い癌です。ベバシズマブの有無にかかわらず、プラチナおよびペメトレキセドとの併用化学療法が第一選択治療での標準である一方、今まで承認された第二選択法は確立されなかった[1]。この状況ではゲムシタビンまたはビノレルビンが使用されることが多いが、これらは限られた活性だけを示す[2]。
しかし、MPM患者での免疫療法の評価には強い論理的根拠がある。これらの腫瘍の炎症表現型はT細胞の関与をほのめかし、MPM細胞は症例のかなり大きな割合でPD-L1を発現する[3-6]。さらに、PD-L1発現はMPMでの予後不良と相関関係があった[7、8]。
MAPS2:併用免疫療法
MAPS-2無作為化非比較フェーズII臨床試験は独立して、隔週で3mg/kgのニボルマブ(n = 63)と、6週間毎に1mg/kgの抗CTLA-4抗体イピリムマブとのニボルマブの併用(n = 62)を、最長2年間、疾患の進行または毒性まで評価した。切除不能なMPMで、ペメトレキセド/プラチナ二剤を含む1回または2回の化学療法後の進行が記録されている患者を登録した。各群で、PD-L1発現状態が患者の79%にあった。
12週時の疾患制御率(DCR)が統計的計画に基づいて主要評価項目と定義され、療法の群で適合した。最初の108人の有資格患者のうち、併用とニボルマブ単剤療法で治療を受けた患者のそれぞれ50.0%と44.4%が、以前報告された通りに12週時に疾患制御を経験した[9]。ITT集団では、DCRがそれぞれ51.6%と39.7%であった。これらは、病歴データや以前の非免疫療法臨床試験と比較して有意な増加である。
Zalcman等は、2017年ESMO学会でMAPS-2臨床試験からの最新所見を発表した[10]。PD-L1状態にある患者の統合分析によると、1%以上のPD-L1発現は奏効と有意に相関し、高いPD-L1発現(25%以上)は客観的奏効と疾患制御の両方に相関した(表)。奏効期間中央値はそれぞれ、7.9ヶ月と7.4ヶ月であった。すべての組織学的亜型
(すなわち、類上皮、二相性、肉腫様)で長期にわたる寛解が観察された。
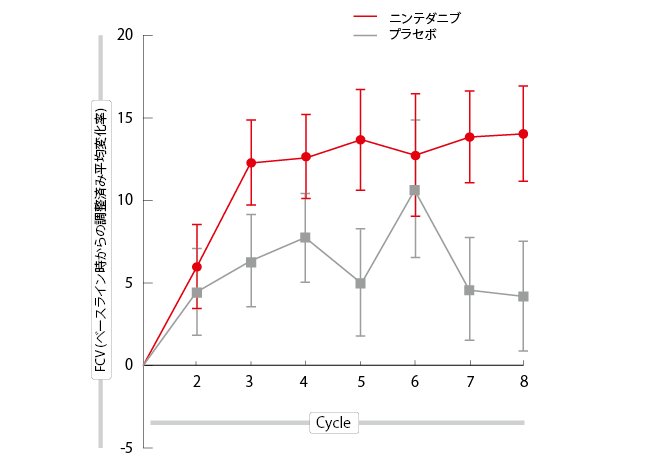
図:ニンテダニブまたはプラセボのいずれかの治療を受けた類上皮組織構造の患者に関するベースライン時からのFVCの調整済み平均割合
一次PFS分析の確認
初期分析に関しては、プラセボと比較してニンテダニブ治療によってPFSを改善したことが最新PFSデータから分かった(9.4ヶ月対5.7ヶ月; HR, 0.54; p = 0.0103)。この改善は、類上皮組織構造の患者で最大であった(9.7ヶ月対5.7ヶ月; HR, 0.49; p = 0.0056)。ニンテダニブ群の患者では、プラセボ群よりも数的に多くの客観的奏効が生じた(56.8%対44.2%)。このすべてが部分奏効であった。
ニンテダニブ治療の安全性プロファイルは管理可能であることを示し、先の試験と一致していた。一般的に血管新生阻害剤に関連するAEは、治療群間で釣り合うか、対照群よりもニンテダニブ群の患者で報告が少なかった。さらに、最後の試験投薬療法の恒久的試験中止につながるAEは、ニンテダニブによる治療でプラセボよりも発生頻度が低くなった(6.8%対17.1%)。ニンテダニブによってバックボーン化学療法の実施に支障を来すことはなかった。LUME-Meso試験のフェーズIII部分では、類上皮組織構造の患者を現在募集している。
参考文献
- Baas P et al., Malignant pleural mesothelioma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up.Ann Oncol.2015; 26 Suppl 5: v31-v39
- Zauderer mg et al., Vinorelbine and gemcitabine as second- or third-line therapy for malignant pleural mesothelioma.Lung Cancer 2014; 84(3): 271-274
- Thapa B et al., The immune microenvironment, genome-wide copy number aberrations, and survival in mesothelioma.J Thorac Oncol 2017; 12(5): 850-859
- Lanteajoul S et al., PD-L1 Testing for Immune checkpoint inhibitors in mesothelioma: for want of anything better? J Thorac Oncol 2017; 12(5): 778-778
- Mansfield AS et al., B7-H1 expression in malignant pleural mesothelioma is associated with sarcomatoid histology and poor prognosis.J Thorac Oncol 2014; 9(7): 1036-1040
- Khanna S et al., Malignant mesothelioma effusions are infiltrated by CD3+ T cells highly expressing PD-L1 and the PD-L1+ tumor cells within these effusions are susceptible to ADCC by the anti-PD-L1 antibody avelumab.J Thorac Oncol 2016; 11(11): 1993-2005
- Cedrés S et al. Analysis of expression of programmed cell death 1 ligand 1 (PD-L1) in malignant pleural mesothelioma (MPM).PLoS One 2015; 10(3): e0121071
- Combaz-Lair C et al., Immune biomarkers PD-1/PD-L1 and TLR3 in malignant pleural mesotheliomas.Hum Pathol 2016; 52: 9-18
- Scherpereel A et al., Second or third-line nivolumab versus nivolumab plus ipilimumab in malignant pleural mesothelioma patients: results of the IFCT-1501 MAPS-2 randomized phase 3 trial.ASCO 2017, abstract LBA8507
- Zalcman G et al., Second or 3rd line nivolumab (nivo) or nivo plus ipilimumab in malignant pleural mesothelioma (MPM) patients: up-dated results of the IFCT-1501 MAPS1 randomized phase 2 trial.ESMO 2017, abstract LBA58_PR
- Alley E et al., Clinical safety and activity of pembrolizumab in patients with malignant pleural mesothelioma (KEYNOTE-028): preliminary results from a non-randomised, open-label, phase 1b trial.Lancet Oncol 2017; 18: 623-630
- Kindler H et al., Phase II trial of pembrolizumab in patients with malignant mesothelioma (MM): interim analysis.WCLC 2016, abstract OA13.02
- Mauti LA et al., Pembrolizumab as second or further line treatment in relapsed malignant pleural mesothelioma; a Swiss registry.ESMO 2017, abstract 1615O
- Quispel-Janssen J et al., A phase II study of nivolumab in malignant pleural mesothelioma NivoMes): with translational research (TR) biopsies.WCLC 2016, OA13.01
- Novello S et al., Overall survival and forced vital capacity results from the LUME-Meso study of nintedanib + pemetrexed/cisplatin versus placebo + pemetrexed/ciusplatin in chemotherapy-naïve patients with malignant pleural mesothelioma.ESMO 2017, abstract 1618PD
- Krug LM et al., Forced vital capacity (FVC) as a reproducible measure of pulmonary function (PF) in chemotherapy-pretreated patients with malignant pleural mesothelioma (MPM).J Clin Oncol 29: 2011 (suppl; abstr 7028)
- Nowak AK et al., Assessing quality of life during chemotherapy for pleural mesothelioma: feasibility, validity, and results of using the European Organization for Research and Treatment of Cancer Core Quality of Life Questionnaire and Lung Cancer Module.J Clin Oncol 2004; 22: 3172-3180
More posts
ALK-陽性NSCLC:クリゾチニブおよびアレクチニブに関する最新情報
PROFILE 1014は、ALK-陽性肺癌患者の第一選択治療でのALK阻害剤クリゾチニブの役割を定義するための最初の研究であった。この研究は、第一選択治療の条件下におけるALK-陽性、局所進行、再発または転移非扁平上皮NSCLC患者への1日2回、250mgのクリゾチニブ(n = 172)と、ペメトレキセドに加えてシスプラチン(n = 171)から構成された。有効性の主要評価項目(すなわち、PFSに関してクリゾチニブ対化学療法の優位性)を0.454のHRで満たした(PFS中央値、クリゾチニブと化学療法に関してそれぞれ、10.9ヶ月対7.0ヶ月; p
形質転換に起因するSCLCの特性および転帰
GFR TKI療法に対する耐性の取得時にEGFR-変異腺癌の少ないが有意な割合がSCLCに形質転換する[1]。さらに、EGFR 変異を隠すデノボ SCLCの例が報告されている[2]。SCLC-形質転換EGFR-変異肺癌の臨床的特徴と臨床経過はほとんど不明であるため、Marcoux等は2006年~2017年に治療を受けたEGFR-変異SCLC患者16人の記録を遡及的に再検討した[3]。この分析によると、腫瘍はその創始者EGFR変異を維持し、T790M.とは相互排他的であった。
悪性中皮腫で前例のない転帰範囲に到達
悪性胸膜中皮腫(MPM)は希ですが、予後不良の侵襲性の強い癌です。ベバシズマブの有無にかかわらず、プラチナおよびペメトレキセドとの併用化学療法が第一選択治療での標準である一方、今まで承認された第二選択法は確立されなかった[1]。この状況ではゲムシタビンまたはビノレルビンが使用されることが多いが、これらは限られた活性だけを示す[2]。 しかし、MPM患者での免疫療法の評価には強い論理的根拠がある。
インタビュー:生存は複数の治療ラインの結果である
FLAURAは、その結果がゲフィチニブおよびエルロチニブよりもオシメルチニブを支持するため、肯定的試験である。現在では、EGFR-変異肺癌の一次選択治療に利用できる複数の選択肢のうちでこの療法を検討する必要がある。オシメルチニブを除いて、第一世代TKIエルロチニブおよびゲフィチニブ、そして第二世代TKIアファチニブがあるが、恐らく近いうちにダコミチニブも含まれ、そのデータは前回のASCO会議で発表された。
EGFR-変異肺癌:新たなデータを考慮した大きな話題としての優先順位付け
第一世代上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR TKI)エルロチニブおよびゲフィチニブのほか、第二世代EGFR TKIアファチニブも、EGFR-変異NSCLC患者の推奨第一選択肢である[1]。しかし、初期奏効の程度に関わらず、患者の60%以上はT790M耐性変異を発症した[2]。EGFR変異とEGFR T790M耐性変異の両方の活性化に対して選択性がある第三世代EGFR TKIオシメルチニブが、進行T790M-陽性NSCLC患者の治療のために米国と欧州で最近承認を受けた。
早期NSCLCの切除後のCTベースの経過観察に関する無作為化所見
早期NSCLCの手術後の最適な経過観察に関して、ESMOガイドラインでは、病歴、身体検査、そしてできれば12ヶ月時と24ヶ月時の造影スパイラル胸部CTを含む通院により、2~3年間、6ヶ月毎に患者観察を実施することを推奨した[1]。その後、二次原発腫瘍(SPC)を発見するために病歴、身体検査、胸部CTを含み年1回の通院を実施する必要があった。しかし、これらの勧告は無作為化臨床試験に基づいたものではなく、そのため、軽度から中等度の証拠だけがある。