SCLCでの有望なアプローチとしての免疫刺激
傾向
9~11ヶ月のOS中央値の悪い転帰を示す進展型小細胞肺癌(SCLC)に関して満たされない高い医学的ニーズがある。第一選択化学療法では一般的に際立った奏効を示すが、奏効者は通常、限られた期間の疾患制御のみを経験する。
免疫系の活性化によってこれらの患者の疾患安定性を延長し、結果として最終的に生存期間に影響を及ぼすという仮定に基づいて、Thomas等はToll様受容体9(TLR9)作動薬Lefitolimodの活性を評価した[1]。Lefitolimodは、化学療法中の腫瘍負荷量削減および放出腫瘍抗原を上手く利用しながら、複数の経路を通じた自然および適応免疫系の広範な増強によって免疫学的監視を開始する[2–4]。
IMPULSE予備的、無作為化、比較フェーズII臨床試験はベルギー、オーストリア、ドイツ、およびスペインの41施設で行われた。4サイクルのプラチナベース導入化学療法後に既にPRまたはCRになった進展型SCLC患者が登録された。これらの患者をLifitolimodに加えて、プラチナベース化学療法(第5/第6サイクル)、続いてLefitolimodの継続による治療を受ける試験群(n = 61)、または対照群(n = 41)のいずれかに3:2の比率で無作為に割り付けた。ここで、患者は現地の慣行に従って第5/第6サイクルの化学療法、続いてその後の治療のみを受けた。Lefitolimodは週2回、60 mgの用量で皮下に投与された。治療意向(ITT)集団のOSが、IMPULSE試験の主要評価項目と定義された。
作用様式の確認
臨床試験の選択された副次的評価項目は、Lefitolimodの作用様式を確認するための薬力学的マーカーの標準化された検出(すなわち、単球の活性化とケモカインIP-10の分泌)から構成された。治療開始前とその後の少なくとも4週目に、比較法で単球とIP-10を評価した。実際、CD169-陽性単球数とIP-10濃度の有意な増加が予想通りに生じた。IMPULSEでは、化学療法との併用でLefitolimodの限定追加毒性を実証した。対照群と比較して試験治療群では咳と頭痛が優勢だった。グレード3のAEは希にしか起こらず、グレード4または5のAEは報告されなかった。
ITT集団のOS分析では生存期間に有意な差は見られなかったが(Lefitolimodベースの投薬計画と化学療法のみで、それぞれ、279.0日対272.0日; HR, 1.27; p = 0.53)、予め計画された分析によると特定のサブグループでLefitolimodの活性の兆候があった。慢性閉塞性肺疾患(COPD)が報告されている患者は、死亡リスクの46%削減を経験した(316.0日対246.0日; HR, 0.54)。
小数での活性化B細胞
存在下での活性
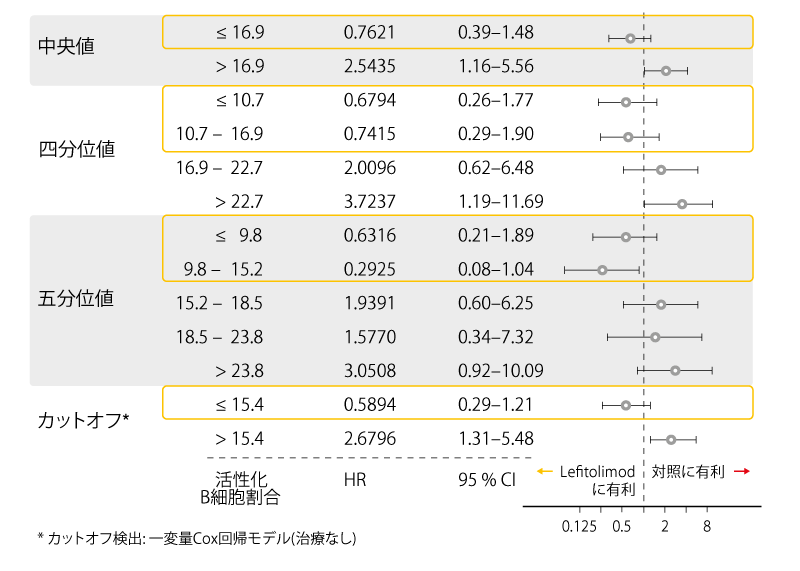
ベースライン時に活性化B細胞数が少ない集団に関して興味深い結果が得られた。このコホートは38人の患者から構成され、そのうちの23人はLefitolimod治療を受けた。OS中央値は、これらの患者にLefitolimodと化学療法のみの治療を行った場合に284.0日対231.5日であった(HR、0.59)。活性化B細胞は、CD19-陽性B細胞のうちのCD86-陽性比率と定義され、15.4 %でカットオフした。低活性化B細胞数の予測値はさまざまな分析にわたって持続した(すなわち、中央値、四分位値、五分位値、線引きカットオフ; 図)。
この現象は、活性化/制御性B細胞によるLefitolimod誘発性の抗腫瘍反応の抑制によるかもしれず、このことはこれらの細胞の数が少ないと、Lefitolimod治療の最大効果を容易にすることを暗示している。次の段階には、活性化B細胞の数が少ない患者集団でのLefitolimodの検証を含む。
図:さまざまな分析にわたる活性化B細胞の数が少ない患者の全生存期間
参考文献
- Thomas M et al., Top-line data from the randomized phase 2 IMPULSE study in small-cell lung cancer (SCLC): immunotherapeutic maintenance treatment with lefitolimod.ESMO 2017, abstract 1527O
- Kapp K et al., Genuine immunomodulation with dSLIM.Mol Ther Nucleic Acids 2014; 3: e710
- Schmidt M et al., Design and structural requirements of the potent and safe TLR-9 agonistic immunomodulator MGN1703.Nucleic Acid Ther 2015; 25(3): 130-134
- Wittig B et al., MGN1703, an immunomodulator and toll-like receptor 9 (TLR-9) agonist: from bench to bedside.Crit Rev Oncol Hematol 2015; 94(1): 31-44
More posts
ALK-陽性NSCLC:クリゾチニブおよびアレクチニブに関する最新情報
PROFILE 1014は、ALK-陽性肺癌患者の第一選択治療でのALK阻害剤クリゾチニブの役割を定義するための最初の研究であった。この研究は、第一選択治療の条件下におけるALK-陽性、局所進行、再発または転移非扁平上皮NSCLC患者への1日2回、250mgのクリゾチニブ(n = 172)と、ペメトレキセドに加えてシスプラチン(n = 171)から構成された。有効性の主要評価項目(すなわち、PFSに関してクリゾチニブ対化学療法の優位性)を0.454のHRで満たした(PFS中央値、クリゾチニブと化学療法に関してそれぞれ、10.9ヶ月対7.0ヶ月; p
形質転換に起因するSCLCの特性および転帰
GFR TKI療法に対する耐性の取得時にEGFR-変異腺癌の少ないが有意な割合がSCLCに形質転換する[1]。さらに、EGFR 変異を隠すデノボ SCLCの例が報告されている[2]。SCLC-形質転換EGFR-変異肺癌の臨床的特徴と臨床経過はほとんど不明であるため、Marcoux等は2006年~2017年に治療を受けたEGFR-変異SCLC患者16人の記録を遡及的に再検討した[3]。この分析によると、腫瘍はその創始者EGFR変異を維持し、T790M.とは相互排他的であった。
悪性中皮腫で前例のない転帰範囲に到達
悪性胸膜中皮腫(MPM)は希ですが、予後不良の侵襲性の強い癌です。ベバシズマブの有無にかかわらず、プラチナおよびペメトレキセドとの併用化学療法が第一選択治療での標準である一方、今まで承認された第二選択法は確立されなかった[1]。この状況ではゲムシタビンまたはビノレルビンが使用されることが多いが、これらは限られた活性だけを示す[2]。 しかし、MPM患者での免疫療法の評価には強い論理的根拠がある。
インタビュー:生存は複数の治療ラインの結果である
FLAURAは、その結果がゲフィチニブおよびエルロチニブよりもオシメルチニブを支持するため、肯定的試験である。現在では、EGFR-変異肺癌の一次選択治療に利用できる複数の選択肢のうちでこの療法を検討する必要がある。オシメルチニブを除いて、第一世代TKIエルロチニブおよびゲフィチニブ、そして第二世代TKIアファチニブがあるが、恐らく近いうちにダコミチニブも含まれ、そのデータは前回のASCO会議で発表された。
EGFR-変異肺癌:新たなデータを考慮した大きな話題としての優先順位付け
第一世代上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR TKI)エルロチニブおよびゲフィチニブのほか、第二世代EGFR TKIアファチニブも、EGFR-変異NSCLC患者の推奨第一選択肢である[1]。しかし、初期奏効の程度に関わらず、患者の60%以上はT790M耐性変異を発症した[2]。EGFR変異とEGFR T790M耐性変異の両方の活性化に対して選択性がある第三世代EGFR TKIオシメルチニブが、進行T790M-陽性NSCLC患者の治療のために米国と欧州で最近承認を受けた。
早期NSCLCの切除後のCTベースの経過観察に関する無作為化所見
早期NSCLCの手術後の最適な経過観察に関して、ESMOガイドラインでは、病歴、身体検査、そしてできれば12ヶ月時と24ヶ月時の造影スパイラル胸部CTを含む通院により、2~3年間、6ヶ月毎に患者観察を実施することを推奨した[1]。その後、二次原発腫瘍(SPC)を発見するために病歴、身体検査、胸部CTを含み年1回の通院を実施する必要があった。しかし、これらの勧告は無作為化臨床試験に基づいたものではなく、そのため、軽度から中等度の証拠だけがある。