检查点抑制在所有治疗线中表现优异
新辅助疗法:NEOSTAR
患有早期和局部晚期(I-IIIA期)非小细胞肺癌(NSCLC)的患者通常需要接受手术,但长期结果仍有待改善。单独手术后的复发率基本上超过 50 %[1]。围手术期化疗是预防疾病复发的一种手段,与单独手术相比,其仅使5年生存率提高5 %[2, 3]。基于这些观察结果,抗PD-1疗法正在新辅助条件下进行测试,目的在于引发特定抗肿瘤应答并根除微转移[4]。 在开放标签随机化II期NEOSTAR试验中,36名接受切除术的I-IIIA期NSCLC患者在手术前接受3剂量 3 mg/kg纳武单抗(nivolumab)单药疗法(A组)或3剂量3 mg/kg纳武单 抗加1剂量1 mg/kg易普利姆玛(ipilimumab)(B组)[5]。将两组中的主要病理缓解(MPR;即≤ 10 %活肿瘤细胞)定义为主要终点。MPR在新辅助疗法后被用作存活的替代指标。据推测,引入纳武单抗和/或纳武单抗加易普利姆玛将产生至少40 %的MPR率,超过引入铂类化疗所达到的MPR率。该研究无法在治疗组之间进行MPR比较。
生物标志物发现证实活性
89 %的患者完成了新辅助疗法,并有 84 %接受了手术治疗。在切除组中, MPR率为31 %。纳武单抗和纳武单抗加易普利姆玛组分别有28 %和33 %的患者达到MPR。切除组中有19 %的患者的样本显示无存活肿瘤细胞(单独纳武单抗和组合分别为14 %和25 %)。 放射照相客观缓解的发生率为22% (分别为31 %和12 %;表)。在放射照 相缓解与MPR之间观察到正相关 (p < 0.002)。总体而言,纳武单抗和纳武单抗加易普利姆玛的新辅助治疗耐受性良好。 根据生物标志物分析,与未经治疗的肺肿瘤相比,两种方案均显著增加了增殖和活化的效应肿瘤浸润淋巴细胞(TIL)的百分比。此外,与未涉及到的肺相比,该治疗增加了肿瘤中的T细胞受体多样性(p = 0.021)。相比单独纳武单抗,组合似乎诱导不同T细胞亚群的更大增殖,但这种差异对于CD8阳性TIL和CD4阳性调节性T细胞不显著。与未涉及到的相邻肺组织相比,纳武单抗加易普利姆玛也显示增加了肿瘤中的T细胞受体同源性(p = 0.048)。 作者在结论中指出,这项研究补充了日益壮大的新辅助单药治疗数据集,并利用组合策略扩展了新辅助疗法的体验。局限在于每组中的样本量较小。探索性生物标志物分析正在进行当中。
PACIFIC的事后分析
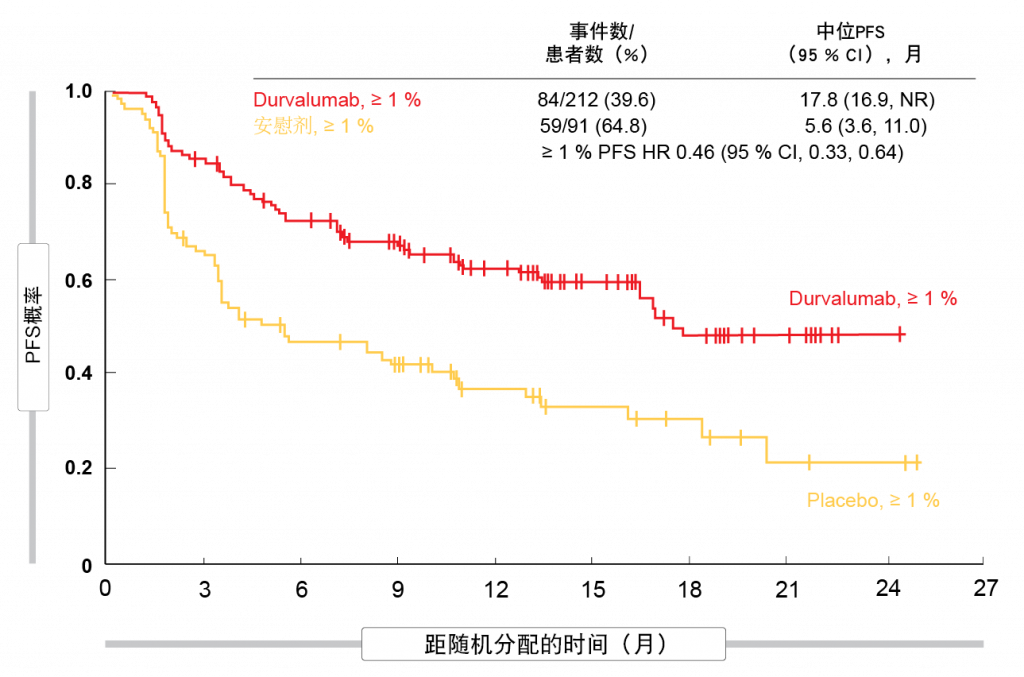
III期PACIFIC试验已将durvalumab确定为在根治性放化疗后未经历进展的不可切除III期NSCLC患者的标准治疗。患者随机接受每2周(Q2W)durvalumab 10 mg/kg达12个月(n = 476)或者安慰剂(n = 237)。对于积极治疗,在无进展生存期(PFS;16.8与5.6个月;HR,0.52;p < 0.001)[6]和总生存期(OS;未达到与28.7个月;HR,0.68;p = 0.0025)[7]方面均观察到显著获益。PACIFIC被设计用于在所有参与者中评估durvalumab,PD-L1测试不强制进行。37 %的患者PD-L1状态未知。根据该试验,durvalumab已经在全球获准用于所有参与者人群,这包括在美国和日本,但欧盟除外,在欧盟批准限于肿瘤细胞表达PD-L1 ≥ 1 %的患者。 在2018年ESMO大会上报告的一项事后分析一方面研究了PACIFIC中基于PD-L1表达的结果,另一方面研究了先前同时放化疗方法的组分[8]。 PD-L1分析证明,在肿瘤细胞表现出PD-L1表达≥1%的患者中, durvalumab在PFS(17.8与5.6个月;HR,0.46;图1)和OS(未达到与29.1个月;HR,0.53)方面带来了获益。在PD-L1表达< 1 %的患者中,注意到PFS改善(10.7与5.6个月;HR,0.73),但OS结果受到安慰剂组表现的困扰。在该组中,生存曲线的轨迹在前12个月有利于durvalumab,这对应于患者接受治疗的时间,而安慰剂治疗的患者在剩余的随访期间表现更好(HR,1.36)。可能解释安慰剂组表现过好的因素包括事件数量较少和亚组数量有限,以及基线特征的不平衡。重要的是,无论PD-L1表达如何,都观察到类似的安全性特征。根据作者的观点,由于在事后探索性亚组分析方面存在局限性,因此无法得出PD-L1状态结果的明确结论。 此外,分析测试了前述治疗对化疗和放射剂量的影响。这些数据显示,无论化疗类型、使用的放射剂量或从放射结束到随机化的时间如何,durvalumab在PFS和OS方面带来一致的获益。同样,无论距放射时间如何,毒性特征均相似。总体而言,这些数据支持将放化疗后使用durvalumab的PACIFIC方案作为不可切除III期NSCLC的新标准治疗。
图1: 在PACIFIC试验中用durvalumab治疗的PD-L1 ≥ 1 %表达组中的无进展生存期改善
IMpower130: atezolizumab加化疗
在随机化开放标签III期IMpower130试验中研究了使用atezolizumab作为化疗之外的添加药物对非鳞状IV期NSCLC的一线治疗[9]。卡铂(carboplatin)加白蛋白结合型紫杉醇(nab-paclitaxel)构成化疗骨干,在实验组中联合atezolizumab(n = 451),而在对照组中单独给予(n = 228)。研究发现支持将atezolizumab加化疗作为晚期非鳞状NSCLC的治疗选择,而不考虑PD-L1状态如何。IMpower130在由随机化患者组成的意向治疗的野生型人群中达到其PFS和OS的共同主要终点,该人群不包括EGFR或ALK基因组改变的患者。Atezolizumab组合使进展和死亡的风险降低36 %(中位PFS,7.0与5.5个月;HR,0.64;p < 0.0001)。死亡风险降低达21 %,并且具有统计上显著且临床相关的4.7个月的OS获益(18.6与13.9个月;HR,0.79 %;p = 0.033)。基于atezolizumab的治疗的12个月PFS率是对照组的两倍(29.1 %与14.1 %)。此外,该分析显示,基于atezolizumab的治疗的客观缓解率(ORR)较高 (49.2 %与31.9 %),并且中位缓解持续时间显著延长(8.4与6.1个月;p = 0.0004)。在分析时,36.8 %与19.4 %的患者具有持续缓解。 除招募时具有肝转移的患者外,所有亚组均发生总生存期和PFS获益。同样,添加atezolizumab可在所有PD-L1队列(高PD-L1、低PD-L1和PD-L1阴性)中均带来PFS获益。对于OS而言,在PD-L1亚组中获得的结果也有利于实验组,但治疗组之间的差异并不显著。EGFR/ALK阳性亚组未获得任何统计上显著的PFS或OS优势。 Atezolizumab加化疗的安全性特征与在单药治疗条件下观察到的不良事件一致。研究未产生新的安全性信号。
bTMB作为预测标志物
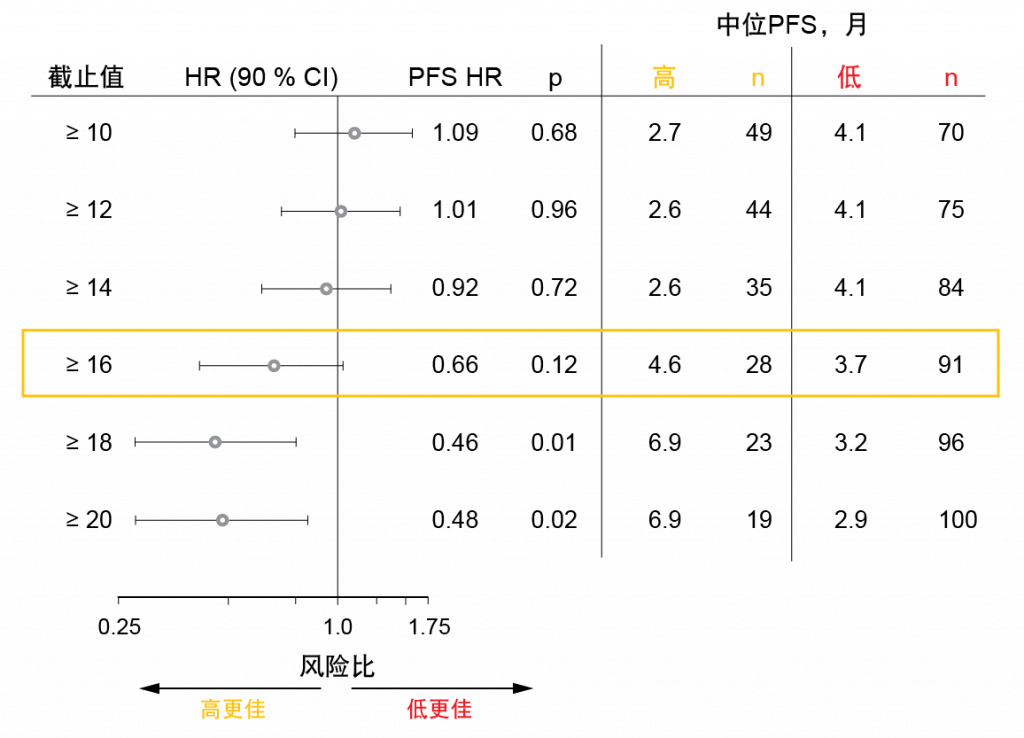
肿瘤突变负荷(TMB)是检查点抑制剂疗法的新兴预测标志物。然而,在诊断时不是总能获得足以用于TMB测试的肿瘤组织。因此,基于血液的TMB(bTMB)构成最近正在接受评估的非侵入性替代物。Kim等人报告了单组II期B-F1RST研究的主要疗效结果,该研究是测试bTMB作为一线NSCLC中atezolizumab单药治疗的预测生物标志物的首项前瞻性试验[10]。具有任何组织学的IIIB/IVA期NSCLC且未进行PD-L1选择的患者(n = 152)接受atezolizumab 1,200 mg Q3W直至进展。将预先设定的bTMB截止值定义为16。总计119名患者组成生物标志物可评估人群(BEP),即基线可评估血液样本显示出足以用于测试的肿瘤含量的人群。其中91名患者和28名患者分别具有低bTMB(< 16)和高bTMB(≥ 16)。 研究人员评估的ORR作为疗效终点,在BEP中达到10.1 %,其中高bTMB亚组的患者相比于低bTMB组的患者显示出显著改善的缓解率(28.6 %与4.4 %; p = 0.0002)。探索性分析显示,改善的缓解具有更高的截止值。当截止值设定为≥ 20时,两组之间的差异更大,为36.8 %与5.0 %(p < 0.0001)。bTMB评分≥ 16的患者尚未达到中位缓解持续时间。同样,在PFS方面,bTMB较高的患者比bTMB较低的患者表现更好,但并不显著如此(4.6与3.7个月;HR,0.66;p = 0.12)。在9个月时,PFS率为37.4 %与9.7 %。对于OS而言,数据尚未成熟。当通过各种bTMB截止值(≥ 10,≥ 16,≥ 20)进行分析时,PFS和OS均随着评分增加而改善 (图2)。对于两个终点而言,预先设定的评分≥ 16似乎是明确区分疗效的拐点。Atezolizumab耐受性良好。bTMB目前正在前瞻性随机化III期试验中进行验证。
图2: B-F1RST研究:根据bTMB评分的无进展生存期森林图
派姆单抗(pembrolizumab)的长期结果:KEYNOTE-010
随机化开放标签II/III期KEYNOTE-010研究显示,在先前接受过治疗的表达PD-L1的晚期NSCLC患者中,两种剂量的派姆单抗单药治疗的OS活性均优于多西他赛(docetaxel)[11]。在2018年ESMO大会上,Herbst等人介绍了另外30个月随访带来的OS和安全性更新结果,以及完成35个周期或2年派姆单抗治疗的患者的结果[12]。 根据该分析,与多西他赛相比,派姆单抗继续延长OS。在PD-L1肿瘤比例评分(TPS)≥ 50 %的人群中,35 %与13 %的患者在36个月时存活(中位OS,16.9与8.2个月;HR,0.53; p < 0.00001)。对于TPS ≥ 1 %的患者,该比例分别为23%和11%(中位OS, 11.8与8.4个月;HR,0.69; p < 0.00001)。 79名患者完成了35个周期或2年的治疗。在该组中,根据独立中心审查,95 %的患者具有完全或部分缓解。在分析时,64 %的患者持续缓解。尚未达到中位缓解持续时间;中位PFS和中位OS同样如此。在36个月时,98.7 %的患者存活,且70.3 %的患者既存活又无进展。25名患者在停止35个周期或2年的治疗后经历疾病进展。其中,14名能够开始第二疗程的派姆单抗治疗,部分缓解达到43 %。稳定疾病的发生率为 36 %。派姆单抗治疗在完成35个周期或2年治疗的患者中的长期安全性特征证明是可控的。
参考文献
- Howington JA et al., Treatment of stage I and II non-small cell lung cancer: Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest 2013; 143(5 Suppl): e278S-e313S
- Pignon JP et al., Lung adjuvant cisplatin evaluation: a pooled analysis by the LACE Collaborative Group. J Clin Oncol 2008; 26(21): 3552-3559
- NSCLC Meta-analysis Collaborative Group, Preoperative chemotherapy for non-small-cell lung cancer: a systematic review and meta-analysis of individual participant data. Lancet 2014; 383: 1561-1571
- Forde PM et al., Neoadjuvant PD-1 blockade in resectable lung cancer. N Engl J Med 2018; 378(21): 1976-1986
- Cascone T et al., NEOSTAR: neoadjuvant nivolumab or nivolumab plus ipilimumab for resectable non-small cell lung cancer. ESMO 2018, abstract LBA49
- Antonia SJ et al., Durvalumab after chemoradiotherapy in stage III non-small-cell lung cancer. N Engl J Med 2017; 377(20): 1919-1929
- Antonia SJ et al., Overall survival with durvalumab after chemoradiotherapy in stage III NSCLC. N Engl J Med 2018 Sep 25. doi: 10.1056/NEJMoa1809697
- Faivre-Finn C et al., Exploratory analyses of overall survival in PACIFIC. ESMO 2018, abstract 13630
- Cappuzzo F et al., IMpower130: efficacy and safety from a randomised phase 3 study of carboplatin and nab-paclitaxel with or without atezolizumab in 1L advanced non-squamous NSCLC. ESMO 2018, abstract LBA53
- Kim ES et al., Primary efficacy results from B-F1RST, a prospective phase II trial evaluating blood-based tumour mutational burden (bTMB) as a predictive biomarker for atezolizumab in 1L non-small cell lung cancer (NSCLC). ESMO 2018, abstract LBA55
- Herbst RS et al., Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial. Lancet 2016; 387(10027): 1540-1550
- Herbst RS et al., Long-term survival in patients with advanced NSCLC in the KEYNOTE-010 study overall and in patients who completed 2 years of pembrolizumab. ESMO 2018, abstract LBA63
More posts
专访:支持EGFR TKI治疗用药顺序的若干原因
有若干原因支持阿法替尼后奥希替尼的用药顺序。原因之一在于在第一代或第二代EGFR TKI发生进展时,耐药突变T790M的发生率高达60 %至75 %。对于已经发生T790M突变的患者,奥希替尼的益处是毫无疑问的。另一个原因在于有利的长期结果。在我们研究中心,常规先使用阿法替尼,随后使用奥希替尼,并且我们已经观察到许多患者得到巨大获益。
EGFR突变肺癌:活性和耐药性方面新发现
在IIIA-N2期NSCLC患者中,当前的多模式治疗选择包括根治性放化疗、手术后辅助化疗或者新辅助治疗后手术切除。标准一线EGFR酪氨酸激酶抑制剂(TKI)厄洛替尼已被证明在IIIA-N2期NSCLC的新辅助治疗条件下具有可行性。因此,开放标签随机化II期CTONG-1103试验在局部晚期EGFR突变NSCLC患者中比较了厄洛替尼与顺铂(cisplatin)类化疗作为新辅助治疗/辅助治疗。
检查点抑制在所有治疗线中表现优异
患有早期和局部晚期(I-IIIA期)非小细胞肺癌(NSCLC)的患者通常需要接受手术,但长期结果仍有待改善。单独手术后的复发率基本上超过 50 %。围手术期化疗是预防疾病复发的一种手段,与单独手术相比,其仅使5年生存率提高5 %。基于这些观察结果,抗PD-1疗法正在新辅助条件下进行测试,目的在于引发特定抗肿瘤应答并根除微转移。
序言
ESMO大会代表了欧洲主办的国际顶级肿瘤学活动。本年度的会议于10月19日至23日在德国慕尼黑举行,口号为“确保获得最佳癌症治疗”。包括各个肿瘤学科的专家、医疗保健决策者和患者权益倡导者在内,来自世界各地的约25,000名参与者讨论了癌症患者治疗中的创新以及将新见解转化为实际改进所面临的主要挑战。许多国家在结构上以及财政上存在的各种障碍仍会阻碍这一进程,因此需要共同作出努力进行克服。

![新辅助疗法:NEOSTAR 患有早期和局部晚期(I-IIIA期)非小细胞肺癌(NSCLC)的患者通常需要接受手术,但长期结果仍有待改善。单独手术后的复发率基本上超过 50 %[1]。围手术期化疗是预防疾病复发的一种手段,与单独手术相比,其仅使5年生存率提高5 %[2, 3]。基于这些观察结果,抗PD-1疗法正在新辅助条件下进行测试,目的在于引发特定抗肿瘤应答并根除微转移[4]。 在开放标签随机化II期NEOSTAR试验中,36名接受切除术的I-IIIA期NSCLC患者在手术前接受3剂量 3 mg/kg纳武单抗(nivolumab)单药疗法(A组)或3剂量3 mg/kg纳武单 抗加1剂量1 mg/kg易普利姆玛(ipilimumab)(B组)[5]。将两组中的主要病理缓解(MPR;即≤ 10 %活肿瘤细胞)定义为主要终点。MPR在新辅助疗法后被用作存活的替代指标。据推测,引入纳武单抗和/或纳武单抗加易普利姆玛将产生至少40 %的MPR率,超过引入铂类化疗所达到的MPR率。该研究无法在治疗组之间进行MPR比较。 生物标志物发现证实活性 89 %的患者完成了新辅助疗法,并有 84 %接受了手术治疗。在切除组中, MPR率为31 %。纳武单抗和纳武单抗加易普利姆玛组分别有28 %和33 %的患者达到MPR。切除组中有19 %的患者的样本显示无存活肿瘤细胞(单独纳武单抗和组合分别为14 %和25 %)。 放射照相客观缓解的发生率为22% (分别为31 %和12 %;表)。在放射照 相缓解与MPR之间观察到正相关 (p < 0.002)。总体而言,纳武单抗和纳武单抗加易普利姆玛的新辅助治疗耐受性良好。 根据生物标志物分析,与未经治疗的肺肿瘤相比,两种方案均显著增加了增殖和活化的效应肿瘤浸润淋巴细胞(TIL)的百分比。此外,与未涉及到的肺相比,该治疗增加了肿瘤中的T细胞受体多样性(p = 0.021)。相比单独纳武单抗,组合似乎诱导不同T细胞亚群的更大增殖,但这种差异对于CD8阳性TIL和CD4阳性调节性T细胞不显著。与未涉及到的相邻肺组织相比,纳武单抗加易普利姆玛也显示增加了肿瘤中的T细胞受体同源性(p = 0.048)。 作者在结论中指出,这项研究补充了日益壮大的新辅助单药治疗数据集,并利用组合策略扩展了新辅助疗法的体验。局限在于每组中的样本量较小。探索性生物标志物分析正在进行当中。](https://memoinoncology.com/wp-content/uploads/2020/03/Grafik-2-esmo-lung-cancer-2018-ch.png)