Antiangiogénesis con nintedanib: actividad en el mesotelioma y posibles biomarcadores
LUME-Meso
El mesotelioma pleural maligno tiene, por lo general, un mal pronóstico, ya que suele diagnosticarse en un estadio avanzado. El único régimen aprobado consiste en la combinación de pemetrexed y cisplatino, que depara una mediana de SG de aproximadamente un año [1]. En el ensayo aleatorizado de fase II, doble ciego y controlado con placebo LUME-Meso se evaluó el uso de nintedanib, un inhibidor de varias cinasas por vía oral, en el tratamiento del mesotelioma. El nintedanib actúa sobre vías proangiógenas mediadas por VEGF1-3, FGFR1-3 y PDGFRα/β, así como sobre las cinasas Src y Abl; todas ellas intervienen en la patogenia del mesotelioma [2, 3]. En comparación con otros fármacos de la misma clase, el nintedanib puede combinarse de forma segura con quimioterapia de uso habitual. El nintedanib ha mostrado eficacia en modelos in vitro e in vivo de mesotelioma [4].
En el estudio LUME-Meso se evaluó la adición de nintedanib, 200 mg dos veces al día, a la quimioterapia convencional con pemetrexed/cisplatino (n = 44), en comparación con placebo más pemetrexed/cisplatino (n = 43), en pacientes con mesotelioma pleural maligno irresecable que no habían recibido quimioterapia previa. Los pacientes que no presentaron progresión de la enfermedad recibieron tratamiento de mantenimiento con nintedanib (grupo experimental) o placebo (grupo de control) hasta la progresión. La SSP se definió como criterio de valoración principal. Se trató de un estudio exploratorio, de modo que todos los estadísticos tenían una finalidad descriptiva.
Ventaja específica en el subtipo epiteloide
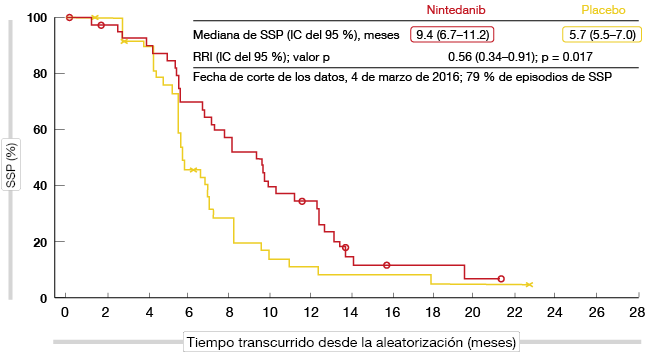
La adición de nintedanib a la quimioterapia produjo una mejoría clínicamente significativa de la SSP de 3,7 meses (9,4 frente a 5,7 meses; RRI, 0,56; p = 0,017; Figura) [5]. Casi todos los subgrupos obtuvieron mayores beneficios de la combinación. Los pacientes tratados con nintedanib también mostraron una mejoría de la tasa de respuesta (59% frente al 44%) y una tendencia a una prolongación de la SG (18,3 frente a 14,5 meses; RRI, 0,78), aunque los resultados aún no son definitivos. Los pacientes con histología epiteloide constituyen casi el 90% de la población del estudio. En este grupo, los resultados de SSP fueron equiparables a los de la población total, mientras que la SG mostró una mayor mejoría (18,3 frente a 15,2 meses; RRI, 0,68), aunque no se alcanzó significación estadística.
Figura: LUME-Meso: SSP con nintedanib o placebo además de quimioterapia convencional en pacientes con mesotelioma pleural maligno
El perfil de seguridad fue coherente con el observado en los estudios de combinación previos, con aparición predominantemente de diarrea y citopenias. Se produjeron acontecimientos adversos de grado ≥ 3 con poca frecuencia. Los acontecimientos adversos notificados con frecuencia con los inhibidores del VEGF/VEGFR, como hipertensión arterial, hemorragia o tromboembolia, fueron raros y estuvieron equilibrados entre los dos grupos. La adición de nintedanib no redujo el número de ciclos de quimioterapia completados ni la intensidad de la dosis de la quimioterapia. A tenor de estos datos, se están reclutando pacientes en la parte de fase III del ensayo de confirmación LUME-Meso. Su diseño es idéntico al de la parte de fase II, pero con reclutamiento exclusivamente de pacientes con histología epiteloide.
Factores angiógenos y estudios de imagen con radiomarcadores
La combinación de nintedanib más docetaxel ha sido autorizada en el tratamiento del adenocarcinoma de pulmón después del fracaso de la quimioterapia, aunque no todos los pacientes se benefician de esta estrategia antiangiógena. Así pues, la identificación de marcadores predictivos de la respuesta es vital. En un ensayo de fase II se evaluó la correlación entre las concentraciones plasmáticas de VEGF, FGF y PDGF y los criterios de valoración clínicos de TCE, SSP y SG en pacientes con CPNM tratados con nintedanib más docetaxel [6]. Se incluyeron 38 pacientes diagnosticados de adenocarcinoma de pulmón en estadio IIIB/IV que habían presentado progresión después de la quimioterapia de primera línea a base de platino. Este ensayo es el primero en el que se han utilizado factores angiógenos como biomarcadores de la respuesta al tratamiento con nintedanib en pacientes con CPNM. El análisis deparó resultados prometedores, ya que las concentraciones de factores angiógenos, especialmente FGF, se correlacionaron con una SG más prolongada. Además, la aparición de hipertensión arterial de grado 1 se asoció a una mejoría de la SSP.
En la misma población de pacientes, Arrieta y cols. evaluaron el uso de PET/tomografía computarizada (TC) con el radiomarcador peptídico [68Ga]-DOTA-E-[c(RGDfK)]2 para medir la expresión de la integrina αvβ3 durante la angiogénesis en tejido tumoral [7]. La integrina αvβ3 constituye una diana molecular para la vigilancia no invasiva de células malignas de crecimiento rápido, así como para la evaluación de la respuesta al tratamiento. Los resultados demostraron que un mayor volumen tumoral basal se asoció a una SSP más prolongada. Una reducción de la variación porcentual (> 11,8%) del índice pulmón/bazo del valor normalizado de captación máximo se asoció a una mejoría de la SG. Según los investigadores, la PET/TC con [68Ga]-DOTA-E-[c(RGDfK)]2 parece una herramienta más útil que la PET/TC con [18F]-FDG para evaluar la respuesta en pacientes con CPNM tratados con nintedanib.
BIBLIOGRAFÍA
- Vogelzang NJ et al., Phase III study of pemetrexed in combination with cisplatin versus cisplatin alone in patients with malignant pleural mesothelioma. J Clin Oncol 2003; 21(14): 2636-2644
- Robinson BW & Lake RA, Advances in malignant mesothelioma. New Engl J Med 2005; 353(15): 1591-1603
- Khusial PR et al., Src activates Abl to augment Robo1 expression in order to promote tumor cell migration. Oncotarget 2010; 1(3): 198-209
- Laszlo V et al., Preclinical investigation of the therapeutic potential of nintedanib in malignant pleural mesothelioma. WCLC 2015, ORAL14.07
- Grosso F et al., Nintedanib plus pemetrexed/cisplatin in patients with MPM: phase II findings from the placebo-controlled LUME-Meso trial, WCLC 2016, OA22.02
- Lee-Cervantes D et al., Soluble angiogenic factors as predictive biomarkers of response to docetaxel plus nintedanib as second-line therapy in NSCLC. WCLC 2016, P2.03b-083
- Arrieta O et al., PET-CT with 68Ga-RGD as biomarker of response to nintedanib plus docetaxel as second-line therapy in NSCLC. WCLC 2016, P2.03b-088
More posts
Mejoras en la estadificación del cáncer de pulmón que pueden modificar la práctica clínica
La octava edición de la clasificación TNM ha entrado en vigor recientemente. En comparación con la séptima edición publicada en 2009, se han hecho varias modificaciones importantes de la estadificación del cáncer de pulmón con el fin de mejorar la pronosticación y la investigación.
Antiangiogénesis con nintedanib: actividad en el mesotelioma y posibles biomarcadores
El mesotelioma pleural maligno tiene, por lo general, un mal pronóstico, ya que suele diagnosticarse en un estadio avanzado. El único régimen aprobado consiste en la combinación de pemetrexed y cisplatino, que depara una mediana de SG de aproximadamente un año. En el ensayo aleatorizado de fase II, doble ciego y controlado con placebo LUME-Meso se evaluó el uso de nintedanib, un inhibidor de varias cinasas por vía oral, en el tratamiento del mesotelioma.
¿Quién es candidato a la inmunoterapia?
Al analizar la inmunoterapia para el CPNM, deberíamos tener presente que aproximadamente el 20% de los pacientes tratados presenta una respuesta. Los biomarcadores podrían resultar útiles para dirigir el tratamiento a los pacientes con una mayor probabilidad de respuesta. Un biomarcador consolidado en la práctica clínica es la expresión tumoral de PD-L1, determinada mediante inmunohistoquímica.
Inmunoterapia: nuevos anticuerpos anti-PD-L1 y diversas pautas de combinación
En comparación con los anticuerpos anti-PD-1, la ventaja de los anticuerpos dirigidos contra PD-L1 radica en que pueden inhibir las interacciones PD-1/PD-L1 dejando intacta la vía de PD-1/PD-L2, con lo que se conserva potencialmente la homeostasis inmunitaria periférica.
Biopsia líquida en el contexto de mutaciones en EGFR y de otro tipo
En comparación con la biopsia tisular y la biopsia repetida, la biopsia líquida ofrece varias ventajas, como mínima invasividad, oportunidad de realizar determinaciones seriadas a lo largo del tiempo para vigilar la respuesta tumoral y detección de mutaciones de resistencia en el plasma antes de la detección radiológica.
Tratamientos emergentes en el CPNM con ALK positivo: nuevas opciones, pero también nuevos desafíos
El tratamiento con crizotinib, un inhibidor de la tirosina cinasa (ITC) ALK, se ha convertido en una opción de primera línea habitual para los pacientes con CPNM avanzado y reordenamiento de ALK. Antes de la aparición del crizotinib, el tratamiento de referencia del CPNM no epidermoide consistía en un doblete de platino-pemetrexed seguido de pemetrexed de mantenimiento.