EGFR-変異肺癌:新たなデータを考慮した大きな話題としての優先順位付け
EGFR TKI治療失敗後のオシメルチニブによる長期結果
第一世代上皮成長因子受容体チロシンキナーゼ阻害剤(EGFR TKI)エルロチニブおよびゲフィチニブのほか、第二世代EGFR TKIアファチニブも、EGFR-変異NSCLC患者の推奨第一選択肢である[1]。しかし、初期奏効の程度に関わらず、患者の60%以上はT790M耐性変異を発症した[2]。EGFR変異とEGFR T790M耐性変異の両方の活性化に対して選択性がある第三世代EGFR TKIオシメルチニブが、進行T790M-陽性NSCLC患者の治療のために米国と欧州で最近承認を受けた。2つの重要なフェーズII AURA延長試験とAURA2試験では、事前のEGFR TKI治療で疾患が進行した後のT790M-陽性NSCLC患者がORRとPFSに関してオシメルチニブ治療から恩恵を受けた[2、3]。
2017年ESMO学会で、Mitsudomi等はAURA延長試験と AURA2試験の統合分析からの長期経過観察とOSデータを発表した[4]。合計411人の患者が進行または試験中止までオシメルチニブ80mg/日の治療を受けた。データカットオフの時点で、オシメルチニブ治療期間の中央値は16.4ヶ月であった。OSおよびPFSの中央値はそれぞれ26.8ヶ月と9.9ヶ月で、ORRは66%であった。奏効期間中央値は12.3ヶ月であった。データカットオフ時点の治験責任医師の評価で患者の41%が新たな病変を有し、よく見られた部位は肺(13%)、CNS(8%)、骨(7%)、肝臓(7%)であった。
オシメルチニブで進行した患者301人のうち、221人(73%)が4.4ヶ月の治療期間中央値の間、治療を継続した。オシメルチニブ治療中止後、患者の69%が他の抗癌治療を受けた。この分析では、グレード3以上のAEの比率が非常に低いため、オシメルチニブの管理可能な安全性プロファイルも確認した。合計で、因果関係がある可能性があるAEのために患者の4%が治療を中止した。
FLAURA:第一選択オシメルチニブ
T790M-変異肺癌条件で有効な治療選択肢としてオシメルチニブが確立された後、FLAURA試験では、 EGFR変異(すなわち、exon 19欠損またはL858R変異)の活性化を隠す進行NSCLC患者でのこの薬剤の第一選択薬としての使用を評価した[5]。FLAURAは二重盲検、 プラセボ対照、無作為化フェーズIII臨床試験実施計画であった。対照群(n = 277)の薬物治療がゲフィチニブ250mg/日またはエルロチニブ150mg/日から構成される一方で、試験治療群では279人の患者がオシメルチニブを80mg/日で投与された。対照群患者の2/3はゲフィチニブによる治療を受けた。安定した中枢神経系(CNS)転移患者の登録が認められたほか、疾患進行およびT790M陽性を集中確認した上で非盲検オシメルチニブ試験への交差も認められた。治験責任医師の評価に基づくRECIST 1.1によるPFSが主要評価項目となった。
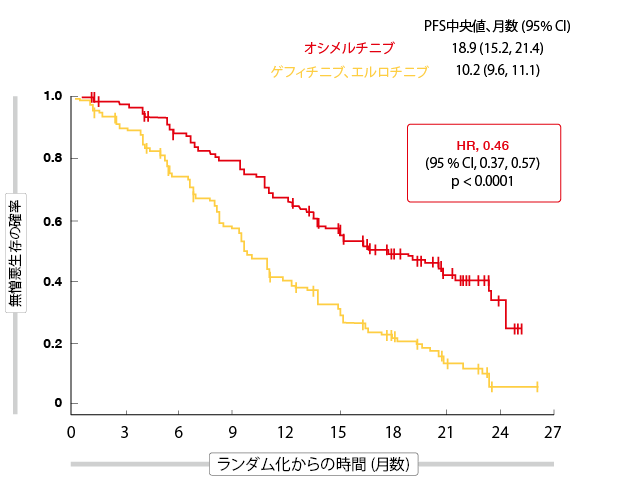
対照群と比較して、オシメルチニブ治療群は、進行または死亡のリスクの54%低減を意味するPFSの有意な改善(18.9ヶ月対10.2ヶ月; HR, 0.46; p < 0.0001; 図1)を経験した。PFSは初期に離れた曲線となり、治療過程全体を通じて離れたままであった。サブグループのすべてが、第一世代EGFR TKIからの転帰よりもオシメルチニブ治療から良好なPFS転帰を得た。
図1:FLAURA臨床試験の主要評価項目:オシメルチニブ対ゲフィチニブおよびエルロチニブによる無増悪生存期間
奏効期間の倍増
ベースライン時の脳転移の存在による分析から、全コホートにわたって一貫したPFS利益が示された:CNS転移患者では、PFSは15.2ヶ月対9.6ヶ月(HR、0.47; p = 0.0009)であり、CNS転移のない患者では19.1ヶ月対10.9ヶ月(HR, 0.46、p < 0.0001)であった。CNS進行事象は全群の6%対15%で発生した。
客観的奏効率は2つの群間で有意に違わなかったが(80%対76%; p = 0.2335)、オシメルチニブは奏効期間を倍増(17.2ヶ月対8.5ヶ月)させた。分析時点で、曲線がオシメルチニブの有効性をほのめかしたが、いずれの群でもOS中央値に到達しなかった(HR, 0.63)。 p値は0.0068に匹敵した;現在の成熟度では、オブライエン・フレミング法で決定される通りの統計的優位性のためには、0.0015未満のp値が求められた。
オシメルチニブのグレード3以上のAEの比率は低く(オシメルチニブとゲフィチニブ/エルロチニブでそれぞれ34%対45%)、中止比率が低かったが(13%対18%)、オシメルチニブの安全性プロファイルは、ゲフィチニブおよびエルロチニブの安全性プロファイルに匹敵した。ざ瘡様皮膚炎およびトランスアミナーゼの上昇が比較的低い割合で表れた一方で、オシメルチニブでは口内炎がわずかに多い頻度で発生した。これらの結果に基づいて、オシメルチニブがEGFR-変異進行NSCLC患者の第一選択療法としての新たな標準治療であると著者は結論付けた。
FLAURAの批評
FLAURA臨床試験の結果の議論において香港中文大学の医学博士、Tony Mokは、FLAURAは明らかに第一選択薬としてのオシメルチニブの有意な利益を示す肯定的な試験であるが、すべてのEGFR-変異陽性患者が実際に第一選択薬としてオシメルチニブ治療を受ける必要があるか疑問を提起した[6]。臨床試験実施計画のいくつかの欠陥について注意が必要である。一例としては、標準治療であるにもかかわらず、対照としてアファチニブが使用されなかった。さらに、ベースライン時に脳転移があった患者で観察されたPFS利益が、頭蓋内PFSではなく全身性のPFSを反映しているため、FLAURAはオシメルチニブのCNS活性を明確に実証しなかった。CNS病変の存在は層別因子ではなかった。このことが2つの群間における罹患率のわずかな不均衡につながり(オシメルチニブ治療群と対照群で、それぞれ19%と23%)、CNS撮像は全患者に必須ではなかった。従って、研究者は有望な方法での頭蓋内CNSの奏効を評価しなかった。さらに、CNS浸透率が異なることが知られているが、ゲフィチニブとエルロチニブで得られた結果は対照群に含まれた。
Mok博士が述べた通り、肺癌治療の最終目標は効果的な薬剤の最適な優先順位付けによるOSの延長である。オシメルチニブのOSデータが不十分で、対照群の64人の患者はゲフィチニブまたはエルロチニブの治療をまだ受けていて、後でオシメルチニブに切り換えるかもしれないことを意味しているため、FLAURA臨床試験の両群での生存期間は不明確なままである。進行した213人の患者のうちの62人だけが今まで第二選択オシメルチニブ治療を受けたため、オシメルチニブへの交差の影響は反映されていない。最終的に、第一選択オシメルチニブ治療に失敗した患者向けの耐性機構と可能な治療方法は現在のところ不明確である。さまざまな標的設定可能変異を調査中であるが、効果的な治療を確立する必要が依然としてある。
LUX-Lung臨床試験からの優先順位付けに関するデータ
フェーズIII LUX-Lung3および6臨床試験では、ステージIIIB/IV EGFR-変異NSCLCの治療未経験患者をアファチニブまたはプラチナベースの二剤化学療法のいずれかに無作為に割り付けた[7、
8]。化学療法と比較して、アファチニブはこれらの臨床試験でPFSとORRを有意に改善した。腫瘍に19欠失変異があるサブグループでOSは有意に延長された[9]。一方で、フェーズIIb LUX-Lung7臨床試験に含まれた患者は無作為化法でアファチニブまたはゲフィチニブのいずれかの治療を受けた。これらの患者は、治療失敗までのPFS時間とORRに関してアファチニブから有意に恩恵を受けた[10]。2つの群の間でOSの差は観察されなかった[11]。
Sequist等は、 EGFR-変異NSCLC患者の最適な治療優先順位付けの確立に寄与することを目的として、LUX-Lung3、6、7での一般的なEGFR変異患者でのその後の治療転帰の後ろ向き解析を行った[12]。アファチニブに無作為に割り付けられた一般的な変異の579人の患者のうち、533人が分析時にアファチニブ治療を中止していた。これらの患者の71%はその後にあらゆる次数の治療を受け、その治療は大部分がプラチナベースの化学療法(50%)、第一世代TKI単剤療法(34%)、単剤化学療法(33%)、またはその他の療法(22%)であった。その後の療法によって治療を受けた患者の割合は、その他のEGFR TKIの臨床試験で観察される割合に似ている[13、14]。19欠失変異とL858R EGFR変異サブグループ全体にわたって治療期間に関連性のある差はなかった。
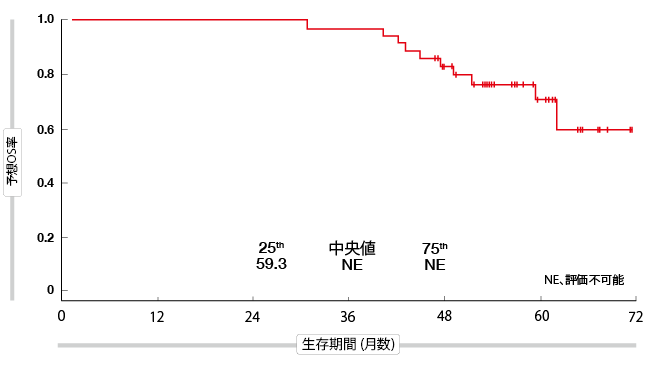
アファチニブを中止した合計37人の患者は、大部分は第三次以降の条件でその後オシメルチニブ治療を受けた。これらの患者では、あらゆる治療次数におけるオシメルチニブでの時間中央値は20.2ヶ月と長く、4年上の経過観察中央値の後、OSにまだ到達していなかった(図2)。
著者によると、これらの有望な転帰は、大規模コホートにおけるこの治療の優先順位をさらに調査する必要があることを根拠づけている。全般的にこれらの所見は、第一選択アファチニブ、続いてオシメルチニブを含むその後の治療による治療優先順位付けを支持する。
図2: アファチニブ治療から始め、その後、何次かでオシメルチニブ治療を受けた患者の生存期間に関する予備解析
参考文献
- Novello S et al., Metastatic non-small-cell lung cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up.Ann Oncol 2016; 27(suppl 5): v1-v27
- Yang JC et al., Osimertinib in pretreated T790M-positive advanced non-small-cell lung cancer: AURA study phase II extension component.J Clin Oncol 2017; 35: 1288-1296
- Goss G et al., Osimertinib for pretreated EGFR Thr790Met-positive advanced non-small-cell lung cancer (AURA2): a multicentre, open-label, single-arm, phase 2 study.Lancet Oncol 2016; 17: 1643-1652
- Mitsudomi T et al., Overall survival in patients with EGFR T790M-positive advanced non-small-cell lung cancer treated with osimertinib: results from two phase II studies.ESMO 2017, abstract 1348P
- Ramalingam SS et al., Osimertinib vs. standard-of-care EGFR-TKI as first-line treatment in patients with EGFRm advanced NSCLC: FLAURA.ESMO 2017 Congress, abstract LBA2_PR
- Mok T, The winner takes it all, ESMO 2017 Congress, Discussion of abstract “ Osimertinib vs. standard-of-care EGFR-TKI as first-line treatment in patients with EGFRm advanced NSCLC: FLAURA.ESMO 2017 Congress, abstract LBA2_PR”
- Sequist LV et al., Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations.J Clin Oncol 2013; 31: 3327-3334
- Wu YL et al., Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations (LUX-Lung 6): an open-label, randomised phase 3 trial.Lancet Oncol 2014; 15: 213-222
- Yang JC et al., Afatinib versus cisplatin-based chemotherapy for EGFR mutation-positive lung adenocarcinoma (LUX-Lung 3 and LUX-Lung 6): analysis of overall survival data from two randomised, phase 3 trials.Lancet Oncol 2015; 16: 141-151
- Park K et al., Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomised controlled trial.Lancet Oncol 2016; 17: 577-589
- Corral J et al., Afatinib (A) vs gefitinib (G) in patients with EGFR mutation-positive (EGFRm+) NSCLC: updated OS data from the phase IIb trial LUX-Lung 7 (LL7).Ann Oncol 2017; 28(suppl_2): ii28-ii51
- Sequist LV et al., Subsequent therapies post-afatinib among patients with EGFR mutation-positive NSCLC in LUX-Lung (LL) 3, 6 and 7.ESMO 2017 Congress, abstract 1349P
- Wu Y-L et al., First-line erlotinib versus gemcitabine/cisplatin in patients with advanced EGFR mutation-positive non-small-cell lung cancer: analyses from the phase III, randomized, open-label, ENSURE study.Ann Oncol 2015; 26: 1883-1889
- Maemondo M et al., Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR.N Engl J Med 2010; 362: 2380-2388
More posts
ALK-陽性NSCLC:クリゾチニブおよびアレクチニブに関する最新情報
ALK-陽性NSCLC:クリゾチニブおよびアレクチニブに関する最新情報 PROFILE 1014は、ALK-陽性肺癌患者の第一選択治療でのALK阻害剤クリゾチニブの役割を定
形質転換に起因するSCLCの特性および転帰
形質転換に起因するSCLCの特性および転帰 GFR TKI療法に対する耐性の取得時にEGFR-変異腺癌の少ないが有意な割合がSCLCに形質転換する[1]。さらに、EGFR
悪性中皮腫で前例のない転帰範囲に到達
悪性中皮腫で前例のない転帰範囲に到達 悪性胸膜中皮腫(MPM)は希ですが、予後不良の侵襲性の強い癌です。ベバシズマブの有無にかかわらず、プラチナおよびペメトレキセドとの併用
インタビュー:生存は複数の治療ラインの結果である
インタビュー:生存は複数の治療ラインの結果である Nicolas Girard, MD, PhD Institut Curie, Institut du Thorax Cu
EGFR-変異肺癌:新たなデータを考慮した大きな話題としての優先順位付け
EGFR-変異肺癌:新たなデータを考慮した大きな話題としての優先順位付け EGFR TKI治療失敗後のオシメルチニブによる長期結果 第一世代上皮成長因子受容体チロシンキナー
早期NSCLCの切除後のCTベースの経過観察に関する無作為化所見
早期NSCLCの切除後のCTベースの経過観察に関する無作為化所見 早期NSCLCの手術後の最適な経過観察に関して、ESMOガイドラインでは、病歴、身体検査、そしてできれば1