ニンテダニブによる抗血管新生:中皮腫における活性、バイオマーカの候補
LUME-Meso
悪性胸膜中皮腫は、一般に進行期に診断されることが多いため、患者の予後が不良である。唯一承認されているレジメンは、ペメトレキセドとシスプラチンの併用であり、約1年のOS中央値が得られる[1]。ランダム化、二重盲検、プラセボ対照、第II相LUME-Meso試験では、中皮腫治療のための経口マルチキナーゼ阻害剤ニンテダニブが評価された。ニンテダニブはVEGF1-3、 FGFR1-3、およびPDGFRα/β、ならびにキナーゼSrcおよびAblによって媒介される血管新生促進経路を標的とする。これらはすべて中皮腫の病因に関与していためである[2, 3]。同クラスの他の薬剤とは対照的に、ニンテダニブは一般的に使用される化学療法と安全に組み合わせることができる。ニンテダニブは、中皮腫のインビトロモデルおよびインビボモデルにおいて有効性が実証されている[4]。
LUME-Meso試験では、化学療法歴がある切除不能な悪性胸膜中皮腫患者を対象に、標準化学療法ペメトレキセド+シスプラチンにニンテダニブ200 mg 1日2回投与を追加した群(44名)を、プラセボ+ペメトレキセド/シスプラチン単独の群(43名)と比較評価した。疾患進行を呈しなかった患者に関しては、進行するまでニンテダニブの維持投与(実験群)またはプラセボの維持投与(対照群)が行われた。主要評価項目はPFSであった。これは探索的試験であり、統計は記述的なものであった。
上皮型サブタイプでの特別な効果
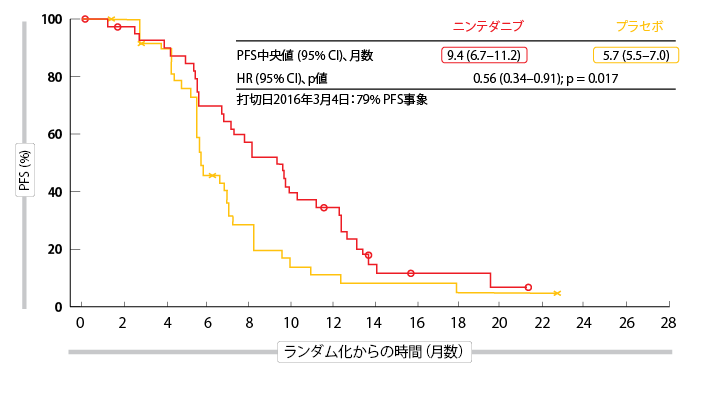
化学療法へのニンテダニブの追加により3.7カ月の臨床的に有意なPFS改善が得られた(9.4カ月対5.7カ月、HR 0.56、p = 0.017、図を参照)[5]。併用療法により、ほとんどのサブグループで大きな効果が認められた。評価はまだ完了していないが、ニンテダニブの治療を受けた患者では、奏効率の改善(59%対44%)、OS延長の傾向(18.3カ月対14.5カ月、HR 0.78)が示された。上皮組織型の患者が試験集団の約90%を占めていた。上皮型グループでは、PFSの結果は全集団のPFSと同等であった。一方で、統計的有意には達していなかったが、OSで改善が認められた(18.3カ月対15.2カ月、HR 0.68)。
安全性プロファイルは、以前の併用試験の結果と一致し、下痢と血球減少が特徴的であった。グレード3以上のAEはまれにしか発生しなかった。高血圧、出血、または血栓塞栓症など、VEGF/VEGFR阻害剤で一般に報告されているAEはまれであり、2群間で大きな差はなかった。ニンテダニブを追加しても、化学療法サイクル完了までの投与回数および用量は減少しなかった。これらのデータをもとに、第III相LUME-Meso確認試験の参加者を現在募集している。第III相の試験デザインは第II相と同一であるが、上皮組織型の患者のみが登録される。
図:LUME-Meso:悪性胸膜中皮腫患者に対する標準化学療法にニンテダニブまたはプラセボ追加投与した場合のPFS
血管新生因子と放射線トレーサー画像
ニンテダニブとドセタキセルの併用は、化学療法の失敗後の肺腺癌の治療に対して承認されているが、肺腺癌のすべてが抗血管新生のアプローチの恩恵を受けるわけではない。したがって、奏功のための予測マーカーの同定が不可欠である。第II相試験では、ニンテダニブとドセタキセルの併用治療を行ったNSCLC患者のVEGF、EGF、およびPDGFの血漿レベルと、ニンテダニブとドセタキセルの併用治療を受けたNSCLC患者のOSとの相関が評価された[6]。プラチナベースの第1選択化学療法後に進行し、ステージIIIB/IVの肺腺癌と診断された患者38名が含まれていた。これは、NSCLC患者におけるニンテダニブ治療に対する反応のバイオマーカとして血管新生因子を利用する最初の試みである。血管新生因子のレベル、特にFGFはOS延長と相関があるので、この解析により有望な結果が得られた。また、グレード1の高血圧の発症はPFS改善と関連していた。
同じ患者集団において、Arrietaらは、腫瘍組織における血管新生中のαvβ3インテグリンの発現を測定するため、ペプチド放射線トレーサー [68Ga]-DOTA-E-[c(RGDfK)]2を用いたPET/コンピュータ断層撮影(CT)の使用を検討した[7]。αvβ3インテグリンは急速に増加する悪性細胞の非侵襲的モニタリングならびに治療応答評価のための分子標的である。結果から、ベースライン時の大きな腫瘍体積は、PFSの延長と関連していることが示された。肺/脾臓の標準化取り込み値指数の変化率減少(11.8%超)はOS改善と関連していた。治験責任医師らによると、ニンテダニブ治療を受けたNSCLC患者の応答性の評価には、[68Ga]-DOTA-E-[c(RGDfK)]2を用いたPET/CTは、[18F]-FDGを用いたPET/CTよりも有用なツールであるようである。
参考文献
- Vogelzang NJ et al., Phase III study of pemetrexed in combination with cisplatin versus cisplatin alone in patients with malignant pleural mesothelioma.J Clin Oncol 2003; 21(14): 2636-2644
- Robinson BW & Lake RA, Advances in malignant mesothelioma.New Engl J Med 2005; 353(15): 1591-1603
- Khusial PR et al., Src activates Abl to augment Robo1 expression in order to promote tumor cell migration.Oncotarget 2010; 1(3): 198-209
- Laszlo V et al., Preclinical investigation of the therapeutic potential of nintedanib in malignant pleural mesothelioma.WCLC 2015, ORAL14.07
- Grosso F et al., Nintedanib plus pemetrexed/cisplatin in patients with MPM: phase II findings from the placebo-controlled LUME-Meso trial, WCLC 2016, OA22.02
- Lee-Cervantes D et al., Soluble angiogenic factors as predictive biomarkers of response to docetaxel plus nintedanib as second-line therapy in NSCLC.WCLC 2016, P2.03b-083
- Arrieta O et al., PET-CT with 68Ga-RGD as biomarker of response to nintedanib plus docetaxel as second-line therapy in NSCLC.WCLC 2016, P2.03b-088
More posts
診療を変える肺癌ステージ分類の変更
診療を変える肺癌ステージ分類の変更 TNM分類が最近第8版に改定された。2009年に発刊された第7版[1]と比較して、予後と研究の改善を目的として、肺癌のステージ分類にいく
ニンテダニブによる抗血管新生:中皮腫における活性、バイオマーカの候補
ニンテダニブによる抗血管新生:中皮腫における活性、バイオマーカの候補 LUME-Meso 悪性胸膜中皮腫は、一般に進行期に診断されることが多いため、患者の予後が不良である。
インタビュー:「免疫療法の対象者は誰か?」
免疫療法の対象者は誰か Johan Vansteenkiste, MD, PhD, Respiratory Oncology Unit/Pulmonology, Unive
免疫療法:新規抗PD-L1抗体およびさまざまな併用レジメン
免疫療法:新規抗PD-L1抗体およびさまざまな併用レジメン OAKサブグループ解析 抗PD-1抗体と比較した抗PD-L1抗体の利点は、PD-1/PD-L2経路をそのまま残し
EGFRおよび他の変異における液体生検
EGFRおよび他の変異における液体生検 組織生検および再生検と比較して、液体生検では最少の侵襲性、腫瘍奏功をモニタリングするための経時的に連続測定が可能、X線検査に先立って
ALK陽性NSCLCにおける新たな治療法:新しい選択肢と新たな課題
ALK陽性NSCLCにおける新たな治療法:新しい選択肢と新たな課題 ALK融合遺伝子陽性NSCLC患者における標準的な第1選択肢として、ALKチロシンキナーゼ阻害薬 (TK