早期肺癌:免疫治疗标准
IMpower010:阿特珠单抗(atezolizumab)的辅助给予
尽管已经有确立的策略,例如,铂类化疗和EGFR靶向药物,但在完全切除的早期NSCLC(IB-IIIA期)条件下对改进的辅助治疗的需求仍远未得到满足。因此,全球III期IMpower010试验在接受了肺叶切除术或全肺切除术以及随后1-4个化疗周期的IB-IIIA期肺癌患者中测试了每21天1200 mg持续16个周期的抗PD-L1抗体阿特珠单抗,并与最佳支持性护理(BSC)相比较。EGFR突变和ALK重排不属于该研究中的排除标准。无病生存期(DFS)定义为主要终点。在三个主要分析群体中进行了分层测试:PD-L1肿瘤细胞(TC)≥1 % II-IIIA期群体(n=476);全随机II-IIIA期群体(n=882);和ITT群体(IB-IIIA期;n=1,005)。
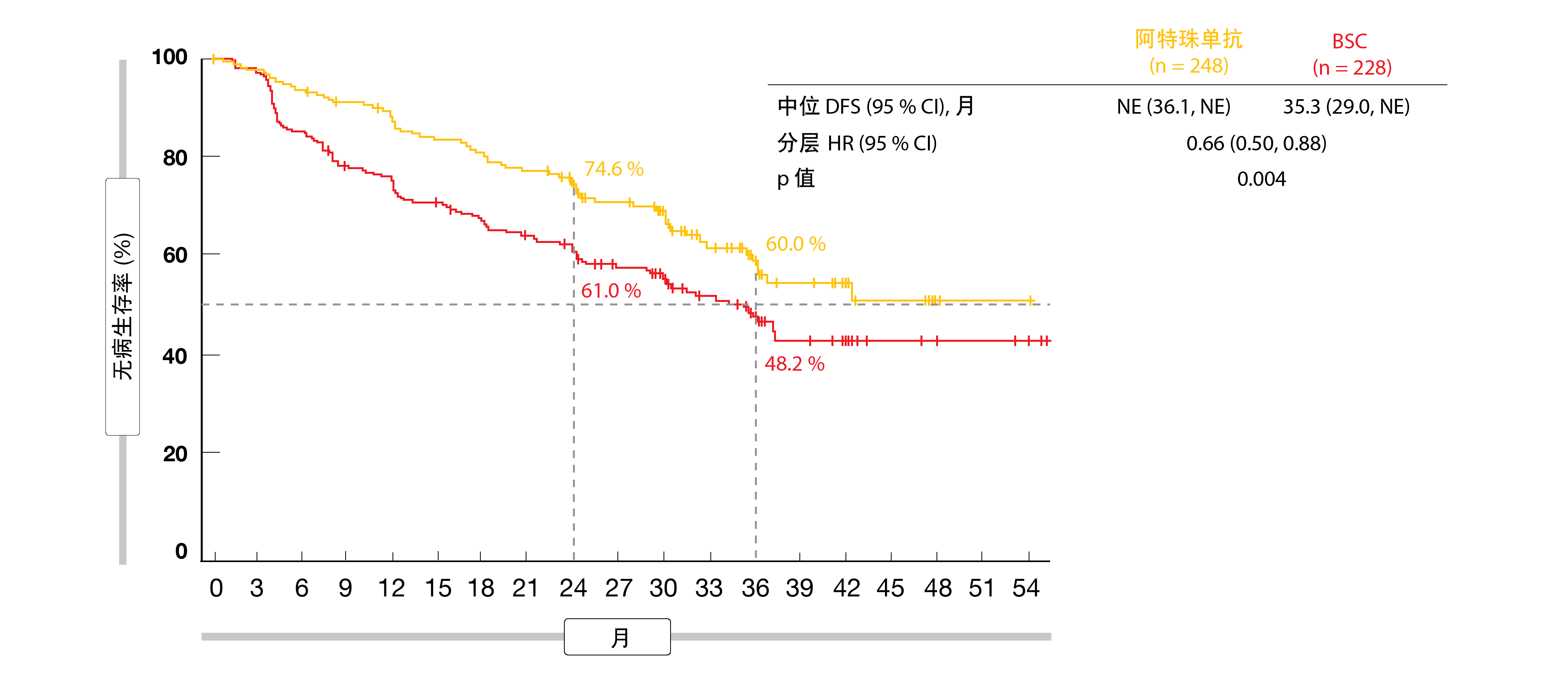
根据由Wakelee等人在ASCO 2021年会上介绍的预先计划的中期分析,阿特珠单抗在PD-L1 TC≥1 % II-IIIA期群体(未达到与35.3个月;HR, 0.66;p=0.004;图1)和全随机II-IIIA期群体(42.3与35.3个月;HR, 0.79;p=0.02)中都产生了显著DFS获益[1]。曲线在早期分离并且在两个群体中保持分离。全随机队列的亚组分析显示DFS获益随PD-L1表达增加,因为PD-L1≥50 %、≥1和< 1 %的组的风险降低分别为57 %、34 %和3 %。在包括患有IB期疾病的患者的ITT群体中,DFS在分析时未越过显著性边界(未达到与37.2个月;HR, 0.81)。测试将会在该组中继续进行。
总体生存期(OS)数据尚不成熟,并且未正式经统计学计划评估。然而,在PD-L1≥1 % II-IIIA期群体中出现了OS改善的趋势(HR, 0.77)。在诸多适应症和治疗线中,阿特珠单抗的安全特性与先前该治疗作为单一药剂的经验相一致。总之,IMpower010是首个在铂类化疗后的辅助NSCLC条件下显示出DFS改善的癌症免疫疗法III期研究。作者的结论是,可以考虑将阿特朱单抗作为PD-L1 TC≥1 % II-IIIA期非小细胞肺肿瘤患者的一种改变实践的辅助治疗选择。
图1: 阿特珠单抗与BSC相比在PD-L1肿瘤细胞≥1 % II-IIIA期群体中的无进展存活率的优越性
新辅助纳武单抗(nivolumab)的加入
随机化III期CheckMate 816试验在患有新诊断的、可切除的II-IIIA NSCLC的患者中测试了纳武单抗外加化疗的新辅助使用,并与单独化疗相比较。Forde等人证明,该组合显著改善了主要终点病理完全缓解(pCR),同时保持可耐受的安全特性[2]。在ASCO 2021上,报告了其他疗效数据和关键的手术结果[3]。
在随机分配至各组的179名患者中,用纳武单抗治疗的患者中接受根治性手术的比例在数值上更高(83%与75%);在该组中,较少的患者接受全肺切除术,微创手术使用得更多。疾病的基线状态不影响pCR改善。在IB/II期中,纳武单抗外加化疗相比于化疗的中位残留存活肿瘤百分比分别为28 %与79 %;对于IIIA期,该值为8 %与70 %。尽管在R0切除的实验组中存在数值优势,但在切除的彻底性方面没有发生差异。
证明新辅助纳武单抗外加化疗方案是可耐受的,并且加入PD-1抑制剂未增加术后并发症的发生率。观察到全级别的手术相关不良事件的发生率为41%与47%。总之,目前CheckMate 816所报告的安全性和手术结果数据以及pCR的显著改善支持纳武单抗与化疗的组合作为潜在的新辅助选择,用于患有可切除NSCLC的患者。将继续推进该研究以获得无事件生存的其他主要终点和进一步的结果。
EGFR突变型NSCLC中的吉非替尼(gefitinib)与化疗
尽管基于顺铂的辅助化疗是完全切除的II-III期NSCLC患者的标准护理,但复发率很高。在日本进行的随机化III期IMPACT试验检验了EGFR-TKI辅助治疗改善EGFR突变型肿瘤患者的结果这一假设[4]。在该研究中,II-III期肿瘤完全切除后的患者被随机分配至250 mg/d持续24个月的吉非替尼或每3周1次持续4个周期的顺铂外加长春瑞滨(vinorelbine)。每组包含116人。
由于吉非替尼相比化疗未显著延长DFS(35.9与25.0个月;HR, 0.92;p=0.63),IMPACT未达到其主要终点。31.8%和34.1%的患者5年无疾病。然而,根据探索性亚组分析,一些患者,例如年龄≥70岁的患者,获益于吉非替尼。OS分析未显示出差别,曲线几乎重合。但亚组分析同样证明在年龄≥70岁的组中有EGFR抑制获益。
辅助吉非替尼的毒性可接受。3/4级中性粒细胞减少症和白细胞减少症在顺铂/长春瑞滨治疗组中频发,但在吉非替尼组中可以忽略,吉非替尼组中转氨酶升高和皮疹最为常见。由于脑梗塞、自杀和肺炎,顺铂/长春瑞滨组发生了3例治疗相关的死亡。正如作者在其结论中指出的,辅助吉非替尼在DFS和OS方面的明显非劣效性可以证明其可用于选定的患者亚组,尤其是那些被认为不适合使用顺铂/长春瑞滨进行辅助化疗的患者。
5年时的持久获益:PACIFIC
随机化、双盲、安慰剂对照的III期PACIFIC试验改变了患有不可切除的III期NSCLC且在铂类放化疗后疾病没有进展的患者的治疗。在该条件下,抗PD-L1抗体度伐鲁单抗(durvalumab)与安慰剂相比显著改善了OS(p=0.00251)和PFS(p < 0.0001),因此被确立为标准护理[5, 6]。在最后一名患者进行随机化后约5年,进行了探索性生存分析[7]。
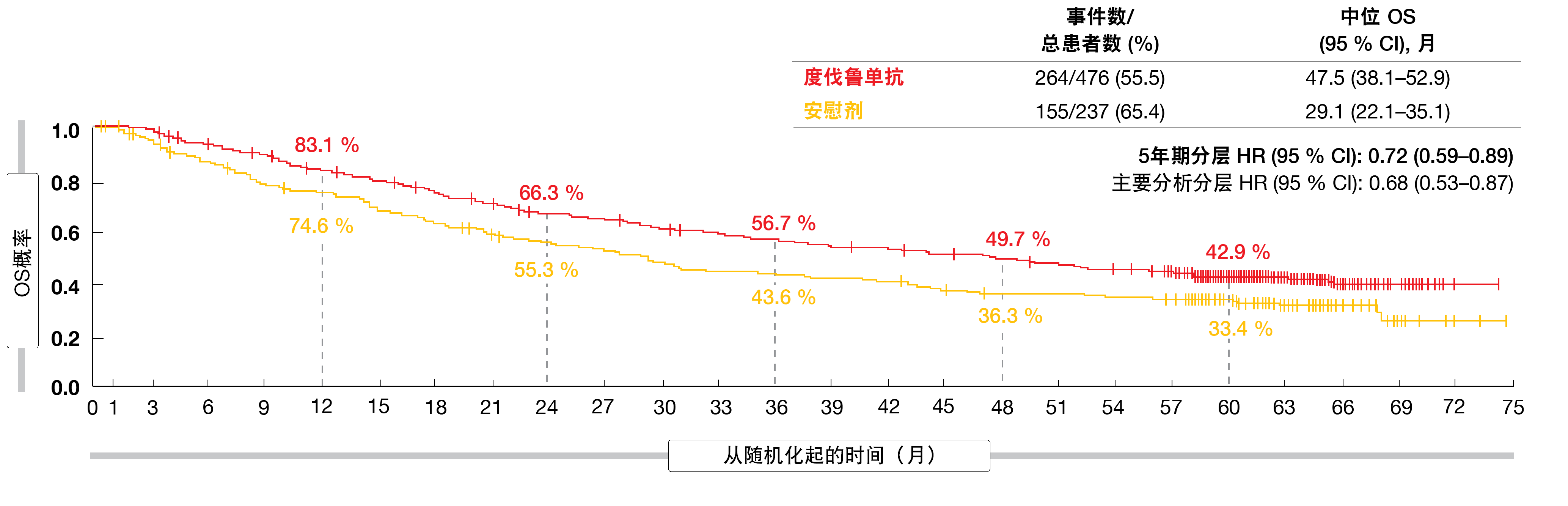
此时,全部随机化患者的中位随访时间为34.2个月。数据显示,度伐鲁单抗与安慰剂的OS和PFS益处与初步分析一致[5, 6]。5年时,实验组中的患者仍有28 %的死亡风险降低,OS率分别为42.9%与33.4%(图2)。5年PFS率分别为33.1%与19.0%,对应于进展或死亡风险降低45%。类似地,亚组的最新OS和PFS与初步分析时报告的结果一致。
作者指出,这些发现证明PACIFIC方案具有稳健持久的OS益处和持续的PFS益处。度伐鲁单抗治疗的患者中有约三分之一仍存活且在5年时无疾病进展,这为该条件下的标准护理确立了新的基准。
图2: PACIFIC试验中度伐鲁单抗与安慰剂的长期总体生存益处
ctDNA作为早期复发的预测因子
研究了基于循环肿瘤DNA(ctDNA)分析的液体活检物以检测局限性NSCLC患者的残留病和复发。微小残留病的评估可以帮助鉴别出可获益于辅助疗法的患者。因此,Gale等人使用个性化测序测定评估了系列血浆样品中的ctDNA以探索在经治愈性治疗的IA-IIIB期NSCLC患者中在复发时或复发之前进行ctDNA检测的可行性和预后价值[8]。纳入了88人;其中78.4%接受了手术,21.6%接受化疗。进行肿瘤外显子组测序以鉴别体细胞突变,并为每位患者开发了个性化ctDNA测定。在治疗前后以及在 3、6 和 9 个月时收集血浆样品。对于17名患者,在疾病进展时收集了额外的血浆。这些患者的中位随访时间为3年。
根据发现,残留ctDNA能预测早期复发。使用敏感的患者特异性血浆测序测定来监测复发时或复发前的ctDNA被证明可行。治疗结束后2周至4个月时检测出ctDNA与更短的无复发生存(HR, 14.8;p < 10-5)和OS(HR, 5.48;p < 0.0003)有关。在疾病进展的患者中,检测出ctDNA先于临床进展,平均提前期为212.5天。
总之,这些结果支持新出现的证据,即ctDNA监测可以在临床进展前数月可靠地检测出治愈性治疗后的残留病,并提供鉴别可能从辅助疗法获益的患者的机会。
参考文献
- Wakelee HA et al., IMpower010: primary results of a phase 3 global study of atezolizumab vs best supportive care after adjuvant chemotherapy in resected stage IB-IIIA non-small cell lung cancer. J Clin Oncol 39, 2021 (suppl 15; abstr 8500)
- Forde PM et al., Nivolumab + platinum-doublet chemotherapy vs chemo as neoadjuvant treatment for resectable (IB-IIIA) non-small cell lung cancer in the phase 3 CheckMate 816 trial. AACR Annual Meeting 2021, abstract CT003
- Spicer J et al., Surgical outcomes from the phase 3 CheckMate 816 trial: nivolumab + platinum-doublet chemotherapy vs. chemotherapy alone as neoadjuvant treatment for patients with resectable non-small cell lung cancer. J Clin Oncol 39, 2021 (suppl 15; abstr 8503)
- Tada H et al., Adjuvant gefitinib versus cisplatin/vinorelbine in Japanese patients with completely resected, EGFR-mutated, stage II-III non-small cell lung cancer (IMPACT. WJOG6410L): a randomized phase 3 trial. J Clin Oncol 39, 2021 (suppl 15; abstr 8501)
- Antonia SJ et al., Durvalumab after chemoradiotherapy in stage III non-small-cell lung cancer. N Engl J Med 2017; 377(20): 1919-1929
- Antonia SJ et al., Overall survival with durvalumab after chemoradiotherapy in stage III NSCLC. N Engl J Med 2018; 379(24): 2342-2350
- Spiegel DR et al., Five-year survival outcomes with durvalumab after chemoradiotherapy in unresectable stage III NSCLC – an update from the PACIFIC trial. J Clin Oncol 39, 2021 (suppl 15; abstr 8511)
- Gale D et al., Residual ctDNA after treatment predicts early relapse in patients with early-stage NSCLC. J Clin Oncol 39, 2021 (suppl 15; abstr 8517)
© 2021 Springer-Verlag GmbH, Impressum
More posts
为SCLC患者开辟新路径
为SCLC患者开辟新路径 LS-SCLC中的顺铂与卡铂 采用铂-依托泊苷骨架的同步放化疗构成了局限期小细胞肺癌(LS-SCLC)的标准护理。在这里,顺铂传统上
经由抗血管发生来增强免疫支持机制
经由抗血管发生来增强免疫支持机制 使用抗血管生成剂的治疗有潜力管控接受免疫检查点抑制剂后进展的患者,因为已经证明过量的VEGF产生可通过调节免疫细胞功能和减少
检查点抑制在致癌基因驱动的肺癌中表现如何?
检查点抑制在致癌基因驱动的肺癌中表现如何? 各种畸变的影响 回顾性分析显示,免疫检查点抑制剂(CPI)在带有可操作致癌驱动突变的患者中的活性有限[1, 2]。
免疫疗法:从预测因子到抗生素
免疫疗法:从预测因子到抗生素 CheckMate 9LA的更新结果 基于随机化III期CheckMate9LA研究,纳武单抗外加伊匹单抗(ipilimumab
KRAS、MET、ROS1、HER2:当前观点
KRAS、MET、ROS1、HER2:当前观点 CodeBreaK100:索托拉西(sotorasib) 大约13%的肺腺癌患者携带KRASG12C突变[1]
EGFR突变型疾病:针对敏感突变和耐药性介导突变的策略
EGFR突变型疾病:针对敏感突变和耐药性介导突变的策略 靶向HER3:帕曲妥单抗-德卢替康(patritumab deruxtecan) EGFR酪氨酸激酶抑