非小細胞肺がんへの免疫チェックポイント阻害薬:広がる選択肢
IMpower110試験:OSに関する中間解析結果
第Ⅲ相ランダム化比較IMpower110試験では、腫瘍の組織型を問わず、Ⅳ期のPD-L1陽性非小細胞肺がん(NSCLC)患者にファーストライン治療として投与した抗PD-L1抗体薬のアテゾリズマブの有効性などを評価している。アテゾリズマブ群には病勢が進行するまでアテゾリズマブを投与し、対照の化学療法群にはプラチナ製剤ベースの化学療法を組織型に応じて4~6コース行った。腫瘍浸潤免疫細胞(IC1/2/3)と腫瘍細胞(TC1/2/3)に発現したPD-L1の発現率に応じて患者を層別化したが、およそ3割強の患者でPD-L1の発現率が最高レベルに達していた(TC3またはIC3)。
主要評価項目とした、野生型の患者集団(EGFR変異もALK融合遺伝子変異も陰性の患者)の全生存期間(OS)の中間解析結果を、Spigelらが本総会で発表した[1]。階層的検定法でOSの評価を行った。まずTC3集団またはIC3集団を評価し、次いでTC2/3集団もしくはIC2/3集団、最後にTC1/2/3集団またはIC1/2/3集団(全患者)の順に評価した。
全組織型にみられた延命効果
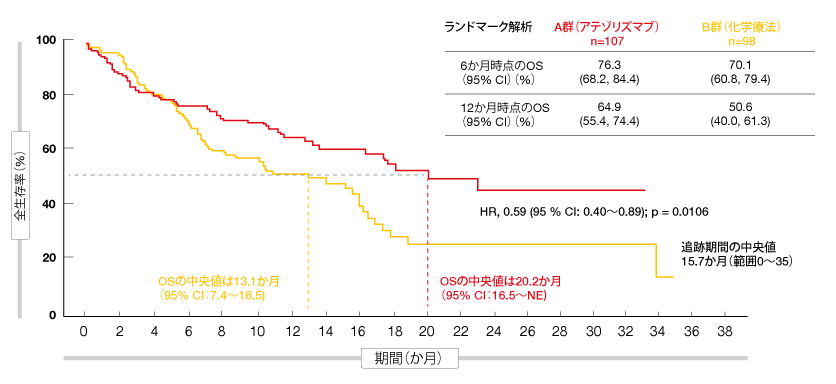
TC3またはIC3集団(n=205)では、化学療法よりもアテゾリズマブに臨床的意義のある有益性が認められた。OSの中央値はアテゾリズマブ群が20.2か月、化学療法群が13.1か月(HR:0.59、p=0.0106、
図1)、12か月時点の生存率は前者が64.9%、後者が50.6%となった。奏効の判定を受けたのは前者が38.3%、後者が28.6%である。奏効期間の中央値についてはアテゾリズマブ群でまだその時期に達していないが、化学療法群では6.7か月だった。TC2/3またはIC2/3の患者集団(n=328)の場合、アテゾリズマブ群に良好な結果がみられてはいたが(前者は18.2か月、後者は14.9か月)、事前に定めたOSの境界を解析時に超えていなかったため、TC1/2/3またはIC
1/2/3の患者集団のOSを正式に解析しなかった。
無増悪生存期間(PFS)についても、
3集団すべての主要評価項目に良好な結果がみられれば正式に解析することとした。現時点では、TC3またはIC3の患者集団のPFSはアテゾリズマブ群が8.1か月、化学療法群が5.0か月(HR: 0.63)となっており、 TC2/3またはIC2/3の患者集団と患者全体でもアテゾリズマブ群に優れた結果が生じている。奏効率については、TC2/3またはIC2/3の患者集団、TC1/2/3またはIC1/2/3の患者集団とも、どちらの治療群でも差異はなかった。前述以外のバイオマーカーに関する解析結果は、今後の総会で発表がある。アテゾリズマブは、PD-L1発現率が高レベルのNSCLC患者への第一選択薬として期待が持てると、著者らは述べた。
図1:IMpower110試験のTC3集団(またはIC3集団)にみられた化学療法に対するアテゾリズマブによる延命効果
B-F1RST試験の最終解析結果
第Ⅱ相B-F1RST試験は、アテゾリズマブの単独療法をファーストライン治療として受ける転移性NSCLC患者への治療効果の予測に、血液中の遺伝子変異量(bTMB)を指標として用いた初の試験である。昨年の総会で発表のあった一次解析結果によると[2]、規定していたbTMBのカットオフ値16と、数値上の臨床的有用性とに相関性があった。
18か月以上に及んだ追跡調査期間を経た同試験の最終解析結果を、Socinskiらが本年度の総会で発表した[3]。
アテゾリズマブ単独療法により実臨床ですべての患者の転帰が改善したことが、データから見てとれた。奏効率(ORR)は、ITT解析対象集団(n=152)では17.1%、バイオマーカーの評価が可能な患者集団(n=119)では12.6%となった。ITT解析対象集団の奏効期間の中央値は16.3か月、OSの中央値は現在も追跡中である。また、bTMBのカットオフ値を16にすると治療効果の予測が可能になることを解析結果が裏付けていて、これがPFS(bTMB高値群は5.0か月、同低値群は3.5か月、HR:0.80、p=0.35)、 ORR(前者は35.7%、後者は5.5%、
p<0.0001)、OS(前者は23.9か月、後者は13.4か月、HR:0.66、p=0.18)に当てはまっている。bTMBのカットオフ値が高くなると臨床的有用性が改善することを探索的解析も示している。
TMBを測定できるほど腫瘍組織がない場合や、化学療法以外のファーストライン治療を行う予定で、PFSとOSを推測する場合、血液検体を用いればTMBを測定できると著者らは結論づけた。最終解析のもうひとつの評価項目はC反応性タンパク(CRP)である。これをベースライン時と、アテゾリズマブの投与開始後は3コース目の初日に測定した。この間のCRPの低下とOSの改善には相関性がみられた。
バイオマーカーとしてのTMB:ペムブロリズマブ単独療法
抗PD-1抗体薬のペムブロリズマブによる治療では、TMB高値とOSの改善との間にはっきりとした相関性が認められなかったため、Herbstらは非盲検試験のKEYNOTE-010、KEYNOTE-042両試験で全エクソーム解析を行い、腫瘍組織中の遺伝子変異量(tTMB)の予測検出力を評価した[8]。PD-L1陽性(TPSが1%以上)進行NSCLC患者を対象に、
KEYNOTE-010試験ではセカンドラインのペムブロリズマブ単独療法を、
KEYNOTE-042試験ではファーストラインの同療法を化学療法と比較した[5、6]。
KEYNOTE-010試験の対象患者で、tTMBが測定可能だったのは253人だった。探索解析結果を見ると、ペムブロリズマブ単独療法ではtTMBがOS、
PFS、ORRと連続変数として関連を示したが、化学療法ではそれがなかった。第Ⅲ相KEYNOTE-042試験にはtTMBが測定可能な患者793人を組み入れている。KEYNOTE-010試験の場合、ペムブロリズマブへの治療反応に対してtTMBが連続変数としてぺムブロリズマブのOS、PFS、ORRとの関連性を示したが、化学療法への治療反応ではおおむねそれがみられなかった。どちらの試験でも、各治療群はもとより全患者のベースライン時の特性もその後の転帰もほぼ同じだったので、tTMBが測定可能な患者から採取した検体は代表的なものとみなした。
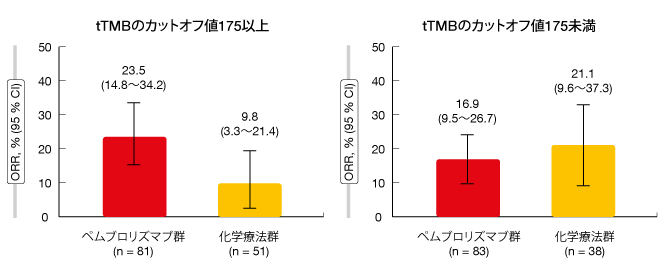
両試験とも、エクソンごとにtTMBのカットオフ値を175以上に設定すると臨床的有用性があった。カットオフ値を175以上にすることで、ペムブロリズマブと化学療法を比較するとOS、PFS、ORRに明確な差異が生じた(図2)。どちらの試験でも、ペムブロリズマブ単独療法にも化学療法にもtTMBとPD-L1発現率との間の相関性はみられなかった。治療経験のあるPD-L1陽性進行NSCLC患者へのファーストライン治療にペムブロリズマブ単独療法を行う場合、tTMBが臨床的有用性の予測に寄与する可能性があると著者らは語った。これで、個別化がん免疫療法にまた一歩踏み出したと言える。
図2:KEYNOTE-010試験で認めた、1エクソンにつき遺伝子変異量のカットオフ値を175に設定した場合の奏効率予測の臨床的有用性
ペムブロリズマブと化学療法の併用療法
ペムブロリズマブと化学療法を併用した患者の転帰とtTMBとの相関性に関する別の探索解析では、異なる結果が生じている。異なる結果が生じたのはKEYNOTE-21試験のコホートCとG、そしてKEYNOTE-189と-407の両試験である[7]。この3試験ではいずれもペムブロリズマブとプラチナ製剤ベースの化学療法を、ファーストライン治療として行っている。KEYNOTE-21試験のコホートCでは2通りの用量のペムブロリズマブを評価[8]したのに対して、同試験のコホートG[9、10]、KEYNOTE-189試験[11]、
KEYNOTE-407試験[12]では対照群に化学療法を単独で行い、評価している。KEYNOTE-407試験の対象患者の中には扁平上皮NSCLCの患者もいたが、それ以外の試験の対象患者はすべて非扁平上皮NSCLCの診断を受けている。全エクソーム解析でtTMBを測定した。3試験の全対象患者を代表する、tTMBが測定可能な患者675人が探索解析の対象になった。
いずれの試験でも、ペムブロリズマブと化学療法の併用療法の有効性もしくはプラチナ製剤ベースの化学療法単独の有効性とtTMBとの間に、統計学的に有意な相関性はみられなかった。tTMBの高値群でも低値群でも、ペムブロリズマブに組織型別の化学療法を併用した患者にOS、PFS、ORRへの延長効果がみられた。ここでもtTMBとPD-L1の発現に相関性はなかった。転移性扁平上皮NSCLC、非扁平上皮NSCLCの両患者にペムブロリズマブとプラチナ製剤ベースの化学療法を併用するファーストライン治療を行う場合、tTMBの臨床的有用性は限定的であることが、この探索解析結果から読み取れた。
KEYNOTE-407試験での安定した効果
前述したように、第Ⅲ相KEYNOTE-407試験では治療経験のない転移性の進行扁平上皮NSCLC患者を対象に、ペムブロリズマブと化学療法の併用と化学療法単独とを比較している。ペムブロリズマブを追加したことが、OSとPFSに統計学的に有意な効果をもたらした[12]。
本総会で発表のあった、治験実施計画書で定めた最終解析結果によると、化学療法単独群に比べて、ペムブロリズマブとカルボプラチン・パクリタキセル
/nab-パクリタキセルの併用療法群では転帰の改善した状態が続いていた[13]。中央値にして14.3か月間追跡したところ、OSの中央値はペムブロリズマブ併用群が17.1か月、化学療法単独群が11.6か月(HR:0.71)、PFSの中央値は前者が8.0か月、後者が5.1か月(HR:0.57)となった。奏効率の差は24.1%(前者は62.6%、後者は38.4%)となり、ペムブロリズマブ併用群で奏効期間が大幅に延びていた(前者は8.8か月、後者は4.9か月)。PD-L1 TPSが1%未満の患者も含めて、すべてのPD-L1 TPSの群で結果は一致していた。
著者らはPFS2(ランダム割り付けから二度目の病勢進行または死因を問わない死亡の、どちらか先に起きるまでの期間)も推測している。ここでもペムブロリズマブ併用群に生じた著しい効果が解析結果に現れていた(前者は13.8か月、後者は9.1か月、HR:0.59)。PD-L1の発現率を問わず、転移性扁平上皮NSCLC患者にペムブロリズマブとカルボプラチン・パクリタキセル/nab-パクリタキセルの併用療法をファーストラインの標準治療として行うことの有効性を、KEYNOTE-407試験成績がまたしても裏付ける結果となった。
CheckMate 227試験:ファーストライン治療になる可能性
第Ⅲ相非盲検ランダム化比較CheckMate 227試験ではPD-L1の発現率が1%以上の進行NSCLC患者(Part 1a)、そして1%未満の同患者(Part 1b)を対象に、抗PD-1抗体薬のニボルマブと抗CTLA-4抗体薬のイピリムマブを併用するファーストライン治療を評価している。Part 1a試験では患者をニボルマブ+低用量イピリムマブ併用療法群、化学療法群、ニボルマブ単独療法群のいずれかにランダムに割り付けた。Part 1b試験ではニボルマブ+低用量イピリムマブ併用療法群を、化学療法群とニボルマブ+化学療法併用群と比較した。同試験ではTMB高値群(10 mut/Mb以上)のPFSと、PD-L1が1%以上の群のOSを主要評価項目とした。両項目ともニボルマブ+低用量イピリムマブ併用療法群と化学療法群とで比較している。
Petersらが本総会でOSの最終結果を発表した[14]。PD-L1の発現率を問わず、併用療法群、化学療法に583人ずつランダムに割り付け、Part 1a試験では396人がニボルマブ単独療法群に割り付けられた。
成功を収めた併用療法
PD-L1が1%以上の群の主要評価項目であるOSの基準を満たすことができ、同試験は抗PD-L1抗体薬と抗CTLA-4抗体薬との併用がNSCLCに有効であることを示した、初の第Ⅲ相試験となった。OSの中央値はニボルマブ+イピリムマブ併用療法群で17.1か月、それに対して化学療法群では14.9か月となった(HR:0.79、
p=0.007、表)。24か月時点で生存していた患者の割合は前者で40%、後者で33%だった。病勢進行および死亡のリスクは18%低下(HR:0.82)し、24か月時点での無増悪生存率は前者が22%、後者が7%だった。ニボルマブとイピリムマブを併用したことが強く安定した効果をもたらした。ORRは前者で35.9%、後者で30%に上り、奏効期間も前者で長く続いた
(前者は23.2か月、後者は6.2か月)。
化学療法群に比べてニボルマブ+イピリムマブ併用療法群にはPD-L1の発現率を問わず、臨床的意義のある全生存期間の延長効果が認められた。
PD-L1の発現率が50%以上の群にも1%未満の群にも効果がみられたことで、それが分かる(表)。ランダム割り付けした全患者のOSの中央値はニボルマブ+イピリムマブ併用療法群が17.1か月、化学療法群が13.9か月である(HR:0.73)。生存期間と、PD-L1の発現率もしくはTMBのどちらかあるいは両方の組み合わせとの間に一貫した相関性はなかった。なお、この試験ではニボルマブ+イピリムマブ併用療法に関して新たな安全性の問題点は認められていない。ニボルマブとイピリムマブとの併用療法が、進行NSCLC患者へのファーストライン治療の新たな選択肢になりうると、著者らは締めくくった。
参考文献:
- Spigel DR et al., IMpower110: interim OS analysis of a phase III study of atezolizumab vs platinum-based chemotherapy as 1L treatment in PD-L1–selected NSCLC.ESMO 2019, abstract LBA78
- Kim ES et al., Primary efficacy results from B-F1RST, a prospective phase II trial evaluating blood-based tumour mutational burden as a predictive biomarker for atezolizumab in 1L non-small cell lung cancer (NSCLC).ESMO 2018, abstract LBA55
- Socinski MA et al., Final efficacy results from B-F1RST, a prospective phase II trial evaluating blood-based tumor mutational burden as a predictive biomarker for atezolizumab in first-line non-small cell lung cancer.ESMO 2019, abstract LBA83
- Herbst RS et al., Association between tissue TMB and clinical outcomes with pembrolizumab monotherapy in PD-L1-positive advanced NSCLC in the KEYNOTE-010 and 042 trials.ESMO 2019, abstract LBA79
- Herbst RS et al., Pembrolizumab versus docetaxel for previously treated, PD-L1-positive, advanced non-small-cell lung cancer (KEYNOTE-010): a randomised controlled trial.Lancet 2016; 387(10027): 1540-1550
- Mok TSK et al., Pembrolizumab versus chemotherapy for previously untreated, PD-L1-expressing, locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomised, open-label, controlled, phase 3 trial.Lancet Oncol 2019; 393(10183): 1819-1830
- Paz-Ares L et al., Pembrolizumab plus platinum-based chemotherapy for metastatic NSCLC: tissue TMB and outcomes in KEYNOTE-021, 189, and 407.ESMO 2019, abstract LBA80
- Gageel SM et al., Pembrolizumab and platinum-based chemotherapy as first-line therapy for advanced non-small-cell lung cancer: Phase 1 cohorts from the KEYNOTE-021 study.Lung Cancer 2018; 125: 273-281
- Langer CJ et al., Carboplatin and pemetrexed with or without pembrolizumab for advanced, non-squamous non-small-cell lung cancer: a randomised, phase 2 cohort of the open-label KEYNOTE-021 study.Lancet Oncol 2016; 17(11): 1497-1508
- Borghaei H et al., 24-month overall survival from KEYNOTE-021 cohort G: pemetrexed and carboplatin with or without pembrolizumab as first-line therapy for advanced non-squamous non-small cell lung cancer.J Thorac Oncol 2019; 14(1): 124-129
- Gandhi L et al., Pembrolizumab plus chemotherapy in metastatic non-small-cell lung cancer.N Engl J Med 2018; 378(22): 2078-2092
- Paz-Ares et al., Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer.N Engl J Med 2018; 379(21): 2040-2051
- Paz-Ares L et al., Pembrolizumab plus chemotherapy in metastatic squamous NSCLC: final analysis and progression after the next line of therapy (PFS2) in KEYNOTE-407.ESMO 2019, abstract LBA82
- Peters S et al., Nivolumab + low-dose ipilimumab versus platinum-doublet chemotherapy as first-line treatment for advanced non-small cell lung cancer: CheckMate 227 part 1 final analysis.ESMO 2019, abstract LBA4_PR
More posts
まれなドライバー変異であっても重要性は高い
まれなドライバー変異であっても重要性は高い Stephen Liu, MD, Lombardi Comprehensive Cancer Center at Georget
CNS病変の存在は治療成功の妨げにならない
CNS病変の存在は治療成功の妨げにならない 診断時にあった神経症状の負担が生存率に及ぼす影響 転移性NSCLC患者の約35%に脳転移を認めており、これがさまざまな神経症状の
ALK、ROS1、NTRK、NRG1といったまれな遺伝子変異陽性肺がんへの画期的な検査法
ALK、ROS1、NTRK、NRG1といったまれな遺伝子変異陽性肺がんへの画期的な検査法 BFAST試験:血液検体を用いたNGS解析の有用性を評価 分子標的治療には遺伝子検
血管新生阻害薬と免疫チェックポイント阻害薬とのシナジー効果に関する調
血管新生阻害薬と免疫チェックポイント阻害薬とのシナジー効果に関する調 主立ったドライバー変異のない進行非扁平上皮NSCLCにとっては、免疫チェックポイント阻害薬が登場したこ
EGFR TKIと血管新生阻害薬を併用するフロントライン治療
EGFR TKIと血管新生阻害薬を併用するフロントライン治療 EGFR遺伝子変異陽性肺がんの治療を受けていない患者には、第一世代のEGFR TKIに抗VEGF抗体のベバシズ
EGFR遺伝子変異陽性肺がん:あらゆる治療ラインにわたる至適治療にかかわる問題点
EGFR遺伝子変異陽性肺がん:あらゆる治療ラインにわたる至適治療にかかわる問題点 FLAURA試験:オシメルチニブを用いたファーストライン治療後のOS EGFR遺伝子変異陽


![ペムブロリズマブと化学療法の併用療法 ペムブロリズマブと化学療法を併用した患者の転帰とtTMBとの相関性に関する別の探索解析では、異なる結果が生じている。異なる結果が生じたのはKEYNOTE-21試験のコホートCとG、そしてKEYNOTE-189と-407の両試験である[7]。この3試験ではいずれもペムブロリズマブとプラチナ製剤ベースの化学療法を、ファーストライン治療として行っている。KEYNOTE-21試験のコホートCでは2通りの用量のペムブロリズマブを評価[8]したのに対して、同試験のコホートG[9、10]、KEYNOTE-189試験[11]、 KEYNOTE-407試験[12]では対照群に化学療法を単独で行い、評価している。KEYNOTE-407試験の対象患者の中には扁平上皮NSCLCの患者もいたが、それ以外の試験の対象患者はすべて非扁平上皮NSCLCの診断を受けている。全エクソーム解析でtTMBを測定した。3試験の全対象患者を代表する、tTMBが測定可能な患者675人が探索解析の対象になった。 いずれの試験でも、ペムブロリズマブと化学療法の併用療法の有効性もしくはプラチナ製剤ベースの化学療法単独の有効性とtTMBとの間に、統計学的に有意な相関性はみられなかった。tTMBの高値群でも低値群でも、ペムブロリズマブに組織型別の化学療法を併用した患者にOS、PFS、ORRへの延長効果がみられた。ここでもtTMBとPD-L1の発現に相関性はなかった。転移性扁平上皮NSCLC、非扁平上皮NSCLCの両患者にペムブロリズマブとプラチナ製剤ベースの化学療法を併用するファーストライン治療を行う場合、tTMBの臨床的有用性は限定的であることが、この探索解析結果から読み取れた。 KEYNOTE-407試験での安定した効果 前述したように、第Ⅲ相KEYNOTE-407試験では治療経験のない転移性の進行扁平上皮NSCLC患者を対象に、ペムブロリズマブと化学療法の併用と化学療法単独とを比較している。ペムブロリズマブを追加したことが、OSとPFSに統計学的に有意な効果をもたらした[12]。 本総会で発表のあった、治験実施計画書で定めた最終解析結果によると、化学療法単独群に比べて、ペムブロリズマブとカルボプラチン・パクリタキセル /nab-パクリタキセルの併用療法群では転帰の改善した状態が続いていた[13]。中央値にして14.3か月間追跡したところ、OSの中央値はペムブロリズマブ併用群が17.1か月、化学療法単独群が11.6か月(HR:0.71)、PFSの中央値は前者が8.0か月、後者が5.1か月(HR:0.57)となった。奏効率の差は24.1%(前者は62.6%、後者は38.4%)となり、ペムブロリズマブ併用群で奏効期間が大幅に延びていた(前者は8.8か月、後者は4.9か月)。PD-L1 TPSが1%未満の患者も含めて、すべてのPD-L1 TPSの群で結果は一致していた。 著者らはPFS2(ランダム割り付けから二度目の病勢進行または死因を問わない死亡の、どちらか先に起きるまでの期間)も推測している。ここでもペムブロリズマブ併用群に生じた著しい効果が解析結果に現れていた(前者は13.8か月、後者は9.1か月、HR:0.59)。PD-L1の発現率を問わず、転移性扁平上皮NSCLC患者にペムブロリズマブとカルボプラチン・パクリタキセル/nab-パクリタキセルの併用療法をファーストラインの標準治療として行うことの有効性を、KEYNOTE-407試験成績がまたしても裏付ける結果となった。 CheckMate 227試験:ファーストライン治療になる可能性 第Ⅲ相非盲検ランダム化比較CheckMate 227試験ではPD-L1の発現率が1%以上の進行NSCLC患者(Part 1a)、そして1%未満の同患者(Part 1b)を対象に、抗PD-1抗体薬のニボルマブと抗CTLA-4抗体薬のイピリムマブを併用するファーストライン治療を評価している。Part 1a試験では患者をニボルマブ+低用量イピリムマブ併用療法群、化学療法群、ニボルマブ単独療法群のいずれかにランダムに割り付けた。Part 1b試験ではニボルマブ+低用量イピリムマブ併用療法群を、化学療法群とニボルマブ+化学療法併用群と比較した。同試験ではTMB高値群(10 mut/Mb以上)のPFSと、PD-L1が1%以上の群のOSを主要評価項目とした。両項目ともニボルマブ+低用量イピリムマブ併用療法群と化学療法群とで比較している。 Petersらが本総会でOSの最終結果を発表した[14]。PD-L1の発現率を問わず、併用療法群、化学療法に583人ずつランダムに割り付け、Part 1a試験では396人がニボルマブ単独療法群に割り付けられた。 成功を収めた併用療法 PD-L1が1%以上の群の主要評価項目であるOSの基準を満たすことができ、同試験は抗PD-L1抗体薬と抗CTLA-4抗体薬との併用がNSCLCに有効であることを示した、初の第Ⅲ相試験となった。OSの中央値はニボルマブ+イピリムマブ併用療法群で17.1か月、それに対して化学療法群では14.9か月となった(HR:0.79、 p=0.007、表)。24か月時点で生存していた患者の割合は前者で40%、後者で33%だった。病勢進行および死亡のリスクは18%低下(HR:0.82)し、24か月時点での無増悪生存率は前者が22%、後者が7%だった。ニボルマブとイピリムマブを併用したことが強く安定した効果をもたらした。ORRは前者で35.9%、後者で30%に上り、奏効期間も前者で長く続いた (前者は23.2か月、後者は6.2か月)。 化学療法群に比べてニボルマブ+イピリムマブ併用療法群にはPD-L1の発現率を問わず、臨床的意義のある全生存期間の延長効果が認められた。 PD-L1の発現率が50%以上の群にも1%未満の群にも効果がみられたことで、それが分かる(表)。ランダム割り付けした全患者のOSの中央値はニボルマブ+イピリムマブ併用療法群が17.1か月、化学療法群が13.9か月である(HR:0.73)。生存期間と、PD-L1の発現率もしくはTMBのどちらかあるいは両方の組み合わせとの間に一貫した相関性はなかった。なお、この試験ではニボルマブ+イピリムマブ併用療法に関して新たな安全性の問題点は認められていない。ニボルマブとイピリムマブとの併用療法が、進行NSCLC患者へのファーストライン治療の新たな選択肢になりうると、著者らは締めくくった。](https://memoinoncology.com/wp-content/uploads/2020/03/Grafik-3-esmo-lung-cancer-2019-jp.png)


